
【题目】判断下列元素中不属于主族元素的是()
A. 磷 B. 钙 C. 铁 D. 碘
科目:高中化学 来源: 题型:
【题目】以有机物A为原料合成重要精细化工中间体TMBA(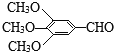 )和抗癫痫药物H(
)和抗癫痫药物H(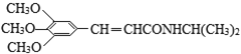 )的路线如图(部分反应略去条件和试剂):
)的路线如图(部分反应略去条件和试剂):
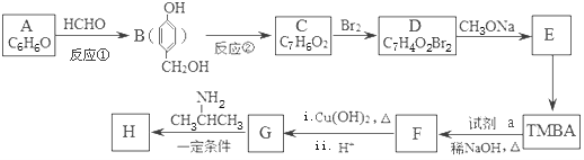
已知:I.RONa+R′X→ROR′+NaX;
II.RCHO+ R′CH2CHO ![]()
![]() +H2O(R、R′表示烃基或氢)
+H2O(R、R′表示烃基或氢)
(1)A的名称是 ;
C能发生银镜反应,则C分子中含氧官能团的名称 .
(2)①和②的反应类型分别是 、 .
(3)E的结构简式是 ,试剂a的分子式是 .
(4)C→D的化学方程式是 .
(5)D的同分异构体有多种,其中属于芳香族酯类化合物的共有 种.
(6)F与新制Cu(OH)2悬浊液发生反应的化学方程式是 .
(7)已知酰胺键(![]() )有类似酯基水解的性质,写出抗癫痫病药物H与足量NaOH溶液发生反应的化学方程式 。
)有类似酯基水解的性质,写出抗癫痫病药物H与足量NaOH溶液发生反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求回答下列问题。
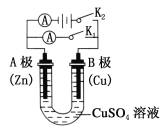
(1)①打开K2,合并K1。A电极可观察到的现象是_____________;B极的电极反应式为________________。
②打开K1,合并K2。A电极可观察到的现象是____________;B极的电极反应为________________________。
(2)判断原电池的正负极时,不仅要看金属活泼性顺序,还要注意此金属在电解质溶液中的活泼性。试回答下列问题:将铝片和铜片用导线连接,若插入浓硝酸中形成原电池,负极是 ,若插入氢氧化钠溶液中形成原电池,负极是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分类的正确组合是
选项 | 纯净物 | 盐 | 碱性氧化物 | 酸性氧化物 |
A | 碱石灰 | 烧碱 | 氧化铝 | 二氧化碳 |
B | NH3·H2O | 小苏打 | 氧化镁 | 二氧化氮 |
C | 五水硫酸铜 | 纯碱 | 氧化钠 | 三氧化硫 |
D | H2O2 | 苏打 | 过氧化钠 | 二氧化硫 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连可以组成几个原电池。若a、b 相连时a为负极;c、d相连时电流由d到c;a、c相连时c极上产生大量气泡;b、d相连时b上有大量气泡产生,则四种金属的活动性顺序由强到弱为
A. a>b>c>d B. c>a>b>d C. a>c>d>b D. b>d>c>a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关。下列叙述中正确的是( )
A.用活性炭为糖浆脱色和用臭氧漂白纸浆,原理相似
B.石油裂化的主要目的是为了提高轻质液体燃料的产量
C.2014年在西非国家爆发了埃博拉疫情,埃博拉病毒对化学药品敏感,乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的
D.煎炸食物的花生油和牛油都是可皂化的饱和酯类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工业废水中含有CN-和Cr2O72-等离子,需经污水处理达标后才能排放,污水处理厂拟用下列流程进行处理,回答下列问题:
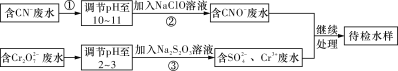
(1)步骤②中,CN-被ClO-氧化为CNO-的离子方程式为:________________________。
(2)步骤③的反应为S2O32-+Cr2O72-+H+―→SO42-+Cr3++H2O(未配平),则每消耗0.4 mol Cr2O72-转移____________mol e-。
(3)含Cr3+废水可以加入熟石灰进一步处理,目的是_____________________。
(4)在25 ℃下,将a mol·L-1的NaCN溶液与0.01 mol·L-1的盐酸等体积混合,反应后测得溶液pH=7,则a__________0.01(填“>”、“<”或“=”);用含a的代数式表示HCN的电离常数Ka=______________。
(5)取工业废水水样于试管中,加入NaOH溶液观察到有蓝色沉淀生成,继续加至不再产生蓝色沉淀为止,再向溶液中加入足量Na2S溶液,蓝色沉淀转化成黑色沉淀。该过程中反应的离子方程是:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下CO2、H2、CO的混合气体与氮气的密度相同,则该混合气体中CO2、H2、CO的质量之比可能为
A. 13:8:27 B. 13:9:27
C. 26:16:27 D. 286:8:27
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学化学中常见的几种物质存在如图所示的转化关系。其中,A是一种黑色粉末状固体,C是一种黄绿色气体,实验室中常用E溶液吸收多余的C(图中部分产物和反应条件已略去)。
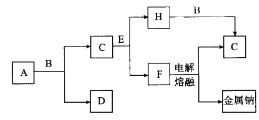
回答下列问题:
(1)写出A与B的浓溶液反应的化学方程式:_________。
(2)将ag粉未A加入bmol/L的B的浓溶液cL中加热完全溶解,反应中转移电子d个,设NA为阿伏加德罗常数的值,NA可表示为_____________。
(3)将B的浓溶液与H的浓溶液混合,立即产生大最气体C,该反应的离子方程式为_______。
(4)某课外小组的同学用E溶液吸收C,利用下图所示装置向吸收液中持续通入SO2气体。
实验过程中观察到如下现象: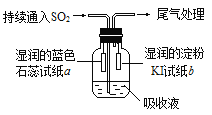
①开始时,溶液上方出现白雾,试纸a变红。甲同学认为是HCl使a变红,乙同学不同意甲的观点,乙同学认为使a变红的是_______(写出一种即可)。
②片刻后,溶液上方出现黄绿色气体,试纸b变蓝。用离子方程式解释b变蓝的原因:_____________
③最终试纸b褪色。同学们认为可能的原因有两种:一是I2有还原性,黄绿色气体等物质将其氧化成IO3-,从而使蓝色消失;二是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com