
【题目】a、b、c、d 四种短周期元素在周期表中的位置如图所示,a 和 b 分别位于周期表的第 2 列和第 13 列, 下列叙述正确的

A.离子半径 b>d
B.b 可以和强碱溶液发生反应
C.c 的氢化物空间结构为三角锥形
D.a 的最高价氧化物对应水化物是强碱
 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:
【题目】25℃时,用0.1000mol·L-1的NaOH溶液分别滴定20.00mL均为0.1000mol·L-1的三种酸HX、HY、HZ ,滴定曲线如图所示。下列说法错误的是
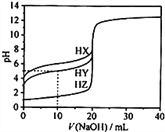
A. HZ是强酸,HX、HY是弱酸
B. 根据滴定曲线,可得Ka(HY)≈10-5
C. 将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+)
D. 将上述HY与HZ溶液等体积混合达到平衡时:C(H+)=c(OH-)+c(Z-)+c(Y-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间。下列有关描述错误的是
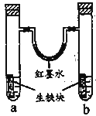
A.生铁块中的碳是原电池的正极
B.红墨水柱两边的液面变为左低右高
C.两试管中相同的电极反应式是:![]()
D.a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物![]() 分子中含有多种官能团,其结构简式为:
分子中含有多种官能团,其结构简式为: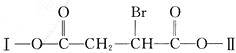
![]() 其中Ⅰ、Ⅱ为未知部分
其中Ⅰ、Ⅱ为未知部分![]() 。为推测X的分子结构,进行如图转化:
。为推测X的分子结构,进行如图转化:
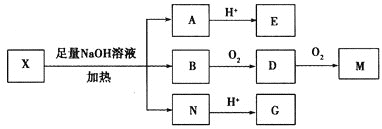
已知![]() 核磁共振氢谱显示有两组峰,峰面积之比为
核磁共振氢谱显示有两组峰,峰面积之比为![]() ;向G的水溶液中滴入
;向G的水溶液中滴入![]() 溶液发生显色反应;E、M都能与
溶液发生显色反应;E、M都能与![]() 溶液反应。请回答:
溶液反应。请回答:
![]() 的结构简式为________________________;D分子中所含官能团的结构简式是____________。B的系统命名法名称为________。
的结构简式为________________________;D分子中所含官能团的结构简式是____________。B的系统命名法名称为________。
![]() 可以发生的反应有
可以发生的反应有![]() 选填序号
选填序号![]() ________。
________。
①加成反应 ②消去反应 ③氧化反应 ④取代反应
![]() 两分子E在一定条件下可生成含有六元环的有机化合物,写出E发生此反应的化学方程式:_____________________________________。
两分子E在一定条件下可生成含有六元环的有机化合物,写出E发生此反应的化学方程式:_____________________________________。
![]() 若在X分子结构中,Ⅱ里含有能与氯化铁溶液发生显色反应的官能团,且G与溴水反应生成的一溴代物有2种,则X与足量NaOH溶液反应的化学方程式为:______________________________________。
若在X分子结构中,Ⅱ里含有能与氯化铁溶液发生显色反应的官能团,且G与溴水反应生成的一溴代物有2种,则X与足量NaOH溶液反应的化学方程式为:______________________________________。
![]() 是相对分子质量比E大14的链状有机化合物,组成元素和E相同,F分子中只含2种官能团,
是相对分子质量比E大14的链状有机化合物,组成元素和E相同,F分子中只含2种官能团,![]() 与足量金属钠反应能放出
与足量金属钠反应能放出![]() 氢气,核磁共振氢谱显示F有四组吸收峰,则符合条件的F的结构简式为
氢气,核磁共振氢谱显示F有四组吸收峰,则符合条件的F的结构简式为![]() 说明:同一个碳上不能连有多个羟基
说明:同一个碳上不能连有多个羟基![]() __________________。
__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。
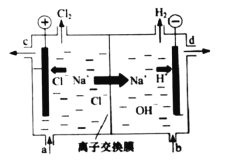
完成下列填空:
(1)写出电解饱和食盐水的离子方程式_______。
(2)离子交换膜的作用为:______、______。
(3)精制饱和食盐水从图中_____位置补充,氢氧化钠溶液从图中_____位置流出(选填“a”、“b”、“c”或“d”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的Cu和浓硫酸反应(装置中的夹持、加热仪器省略),反应后,圆底烧瓶内的混合液倒入水中,得到蓝色溶液与少量黑色不溶物。

(1)反应后蓝色溶液呈酸性的原因有①______________,②______________。
(2)为检验反应产生气体的还原性,试剂 a 是______________。
(3)已知酸性:H2SO3>H2CO3>H2S。反应后测得 Na2S 和 Na2CO3 混合溶液中有新气体生成。该气体中 ______________ (填“含或不含”) H2S,理由是______________;
(4)少量黑色不溶物不可能是 CuO 的理由是______________。
查阅资料后发现该黑色固体可能是 CuS 或 Cu2S 中的一种或两种,且 CuS 和 Cu2S 在空气中煅烧易转 化成 Cu2O 和 SO2。称取 2.000g 黑色固体,灼烧、冷却、……最后称得固体 1.680g。
(5) 灼烧该固体除用到酒精灯、坩埚、坩埚钳、三脚架等仪器,还需要______________。 确定黑色固体灼烧充分的依据是______________,黑色不溶物其成分化学式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是有机物 H 的合成路径。
已知: 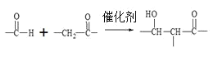
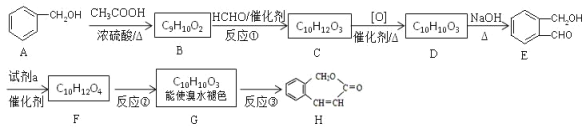
(1)①的反应类型是________。②的反应条件是_____________。
(2)试剂 a 是_________。F 的结构简式是_________。
(3)反应③的化学方程式_________。 与E互为同分异构体,能水解且苯环上只有一种取代基的结构简式是_________。(写出其中一种)
(4)A合成E为何选择这条路径来合成,而不是A和HCHO直接合成,理由是_________。
(5)根据已有知识,设计由![]() 为原料合成
为原料合成![]() 的路线_________,无机试剂任选(合成路线常用的表示方法为:X
的路线_________,无机试剂任选(合成路线常用的表示方法为:X![]() Y……
Y……![]() 目标产物)
目标产物)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿司匹林(化合物L)是人们熟知的解热镇痛药物。一种长效、缓释阿司匹林(化合物P)的合成路线如下图所示:

已知:①HC≡CH+RCOOH![]()
![]()
②RCOOR’+R”OH![]() RCOOR”+R’OH(R、R’、R”代表烃基)
RCOOR”+R’OH(R、R’、R”代表烃基)
请回答:
(1)A中的官能团是____________________。
(2)C的结构简式是____________________。
(3)D→E的反应类型是____________________。
(4)E→G的化学方程式是______________________________________。
(5)已知:H是芳香族化合物。在一定条件下2B → K + H2O,K的核磁共振氢谱只有一组峰。J→L的化学方程式是____________________。
(6)L在体内可较快转化为具有药效的J,而化合物P与L相比,在体内能缓慢持续释放J。
① 血液中J浓度过高能使人中毒,可静脉滴注NaHCO3溶液解毒。请用化学方程式解释NaHCO3的作用:______________________________________________________________。
② 下列说法正确的是______(填字母)。
a.P中的酯基在体内可缓慢水解,逐渐释放出J
b.P在体内的水解产物中没有高分子化合物
c.将小分子药物引入到高分子中可以实现药物的缓释功能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为2 L的密闭容器中发生反应xA(g)+yB(g)![]() zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是( )
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是( )
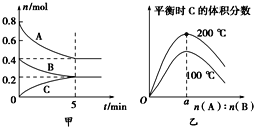
A. 200℃时,反应从开始到平衡的平均速率v(B)=0.04 mol·L-1·min-1
B. 200℃时,该反应的平衡常数为25
C. 当外界条件由200℃降温到100℃,原平衡一定被破坏,且正逆反应速率均增大
D. 由图乙可知,反应xA(g)+yB(g)![]() zC(g)的△H<0,且a=2
zC(g)的△H<0,且a=2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com