
【题目】甲醇是重要的化工原料,也可作燃料。工业上可用CO2和H2在一定条件下合成甲醇。回答下列问题。
(1)已知:CO 和 H2 的燃烧热分别为 283.0 kJ·mol-1、285.8kJ·mol-1 ,水的汽化热为 44.0kJ·mol-1, 反应① CO+H2O=CO2+H2 是生成合成甲醇的原料气(CO2、H2)的重要反应,其热化学方程式为: CO(g)+H2O(g)=CO2(g)+H2(g) ΔH =_____ kJ·mol-1。
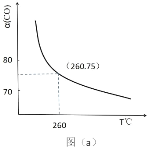
(2)某同学设计实验对反应①进行研究。将 1mol H2O(g)和 1mol CO 充入一个恒容密闭容器中,在催化剂和一定温度下达到化学平衡。如图是 CO 的平衡转化率(%)随温度变化的曲线,260℃时反应①的平衡常数 K=_______。
(3)CO2和 H2在催化剂、一定温度下合成甲醇。图为在容积为 1L 的恒容密闭容器中,加入 3 molH2和 1molCO2时经过相同时间甲醇产率与反应温度的关系曲线:
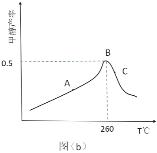
曲线上 A 点_____(填“是”或“不是”)对应温度下的平衡产率,理由是_____,C 点甲醇的产率低于 B 点的原因可能是_____(填标号)。
A.反应活化能增大 B.催化剂活性低 C.副反应多 D.平衡常数变大 E.平衡逆向移动
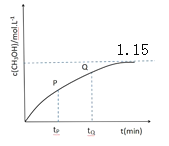
(4)CO和 H2在一定条件下也可以合成甲醇。在容积为1L的恒容密闭容器中,加入 a molH2和2.0molCO,在催化剂和 260℃温度条件下发生反应:CO+2H2=CH3OH。图为甲醇的浓度与反应时间的关系曲线,tP 时的 v 逆_____tQ 时的 v 逆(填大于、小于或等于),判断的依据是_____,达平衡时氢气的浓度为 1.0mol/L,则起始时加入的氢气的物质的量为_____mol。
【答案】-41.2 9 不是 该反应为放热反应,平衡产率随温度的升高而降低 BCE 小于 tP 时的甲醇浓度小于tQ 时浓度,反应速率更慢 3.3
【解析】
(1)H2的燃烧热为-285.8kJ·mol-1,故热化学方程式为H2(g)+![]() O2(g)=H2O(l)△H=-285.8KJ·mol-1;CO的燃烧热为-283.0kJ·mol-1,故热化学方程式为①CO(g)+
O2(g)=H2O(l)△H=-285.8KJ·mol-1;CO的燃烧热为-283.0kJ·mol-1,故热化学方程式为①CO(g)+![]() O2(g)=CO2(g)△H=-283.0KJ·mol-1,②H2(g)+O2(g)=H2O(l)△H=-285.8KJ·mol-1,③H2O(l)=H2O(g)△H=+44.0KJ·mol-1,1×①-②-③得, CO(g)+H2O(g)=CO2(g)+H2(g) ΔH =-41.2kJ·mol-1。故答案为:-41.2;
O2(g)=CO2(g)△H=-283.0KJ·mol-1,②H2(g)+O2(g)=H2O(l)△H=-285.8KJ·mol-1,③H2O(l)=H2O(g)△H=+44.0KJ·mol-1,1×①-②-③得, CO(g)+H2O(g)=CO2(g)+H2(g) ΔH =-41.2kJ·mol-1。故答案为:-41.2;
(2)对反应①CO(g)+H2O(g)=CO2(g)+H2(g) 进行研究。
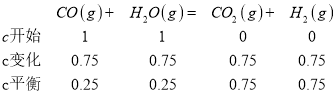
260℃时反应①的平衡常数 K=![]() =9。故答案为:9;
=9。故答案为:9;
(3)曲线上 A 点不是对应温度下的平衡产率,理由是该反应为放热反应,平衡产率随温度的升高而降低,C 点甲醇的产率低于 B 点的原因可能是:A.反应活化能增大,不影响产率,故错误; B.催化剂活性低,产率降低,故正确; C.副反应多,消耗大量原料,故正确; D.平衡常数变大,平衡正向移动,产率升高,故错误;E.平衡逆向移动,产率降低,故正确;故选BCE;故答案为:不是;该反应为放热反应,平衡产率随温度的升高而降低;BCE;
(4)甲醇的浓度与反应时间的关系曲线可知,tP 时的 v 逆小于tQ 时的 v 逆,tP 时的甲醇浓度小于tQ 时浓度,反应速率更慢;由图平衡时c(CH3OH)= 1.15mol·L-1,由方程式CO+2H2=CH3OH得氢气的浓度变化量为2.3mol·L-1,起始时加入的氢气的浓度为(2.3+1)mol·L-1=3.3mol·L-1,则起始时加入的氢气的物质的量为3.3mol;故答案为:小于:tP 时的甲醇浓度小于tQ 时浓度,反应速率更慢;3.3。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细磷化工产品,有强还原性。已知:①2P4+3Ba(OH)2+6H2O=3Ba(H2PO2)2+2PH3↑,②H3PO2+NaOH(足量)=NaH2PO2+H2O。下列推断不正确的是
A. H3PO2的结构式为
B. H3PO2具有强还原性,在空气中可能被氧化成磷酸
C. NaH2PO2是酸式盐
D. 每消耗1mol P4,反应①中转移6mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NiCl2是化工合成中最重要的镍源,在实验室中模拟工业上以金属镍废料(含Fe、Al等杂质)为原料生产NiCl2的工艺流程如下:
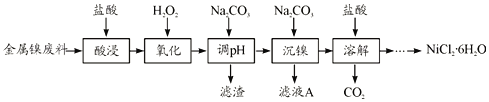
下表列出了相关金属离子生成氢氧化物沉淀的pH
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Ni(OH)2 |
开始沉淀的pH | 2.1 | 6.5 | 3.7 | 7.1 |
沉淀完全的pH | 3.3 | 9.7 | 4.7 | 9.2 |
(1)为了提高镍元素的浸出率,在“酸浸”时可采取的措施有__________(写一条即可)。
(2)加入H2O2时发生主要反应的离子方程式为__________。
(3)“调pH”时,控制溶液pH的范围为__________。
(4)“沉镍”过程中,若滤液A中c(Ni2+)=1.0mol/L,欲使100mL该滤液中的Ni2+沉淀完全[即溶液中c(Ni2+)≤1.0×10-5],则需用托盘天平称取Na2CO3固体的质量至少为_____g。(已知Ksp(NiCO3)=6.5×10-6,忽略溶液体积的变化)
(5)流程中由溶液得到NiCl2·6H2O的实验操作步骤依次为______、过滤、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为Lil晶体锂电池的工作示意图,该电池具有使用寿命长、电压稳定等优点,常用于心脏起搏器的电源。下列说法错误的是( )
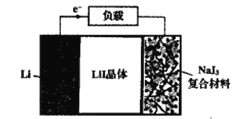
A.NaI3为电池的正极材料
B.电池工作时,Li+由NaI3移动到Li电极
C.正极电极反应为:2Li++NaI3+2e-=2LiI+NaI
D.该电池的总反应为:2Li+NaI3=2LiI+NaI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】HCHO与O2在羟基磷灰石(HAP)表面反应通过两步反应生成CO2、H2O的机理如图所示(图中只给出了HAP的部分结构)。下列说法错误的是( )
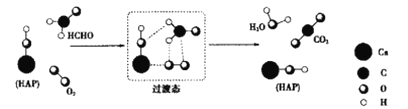
A.HCHO在反应过程中,所有C-H键都发生断裂
B.反应第一步是吸热过程
C.产物H2O中的O全部来自于O2
D.HAP是该反应的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物 A 是一种重要的化工原料,以 A为起始原料可合成药物 I(结构简式如下),其合成路线如下:

已知:①有机物 D 为芳香烃
②RNH2+
![]()
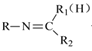 +H2O
+H2O
回答下列问题:
(1)F 的名称是_____,B 中官能团的名称是_____。
(2)由 B→C、E+H→I 的反应类型分别是_____、_____。
(3)G 的结构简式为_____。
(4)D→F 所需的试剂和反应条件是_____。
(5)G 和 CH3CHO 反应生成 H 的化学方程式为_____。
(6)芳香化合物J是 E的同分异构体。若J 能发生银镜反应,则J 可能结构有______种(不含立体异构), 其中核磁共振氢谱有四组峰,且峰面积之比为 1:1:2:6 的结构简式为_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2017·天津卷)常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A. 增加c(CO),平衡向正向移动,反应的平衡常数增大
B. 第二阶段,Ni(CO)4分解率较低
C. 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
D. 该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第四周期包含18种元素,其中多种元素具有重要的用途,在现代工业中备受青睐。
(l)铁位于元素周期表____区,Fe3+的价电子排布式为 ____。
(2)乙二胺(H2NCH2CH2NH2)是一种有机化合物,可用en代表,其能够与Cu2+形成稳定环状配离子,可表示为[Cu(en)2]2+,其中Cu2+的配位数为____。1 mol[Cu(en)2]C12中含有σ键的数目为____。
(3)气态SeO3为单分子,该分子中Se原子的杂化轨道类型为 ___。用物质结构理论解释H2SeO4比H2SeO3酸性强的原因:______________。
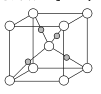
(4)如图为Cu2O的晶胞结构,其中黑球表示____原子(填元素符号);Cu2O的密度为pg·cm-3则晶胞的边长为 ___cm。(用NA表示阿伏加德罗常数的值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】淀粉在一定条件下发生下列转化关系:

已知:化合物H中含有一个甲基。请回答:
(1)写出B的电子式___;化合物D中的官能团名称___。
(2)E+H→G的化学方程式:___。
(3)下列说法不正确的是___。
A.化合物A和D能与银氨溶液反应生成光亮的银镜
B.用新制的氢氧化铜不能区分化合物C、D、E
C.相同质量的A、E和H充分燃烧时消耗等量的氧气
D.化合物F与G互为同分异构体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com