
【题目】PbCrO4是一种黄色颜料,制备PbCrO4的一种实验步骤如下:
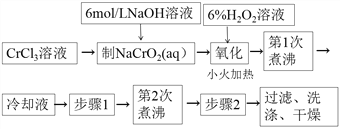
除图中标注的试剂外,实验中还用到6mol·L-1 醋酸,0.5 mol·L-1 Pb(NO3)2溶液,pH 试纸。
已知:①部分物质性质如下
物质 | 性质 | 颜色 | 溶解性 |
Cr(OH)3 | 两性氢氧化物 | 绿色 | 难溶于水 |
Pb(NO3)2 | - | 无色 | 易溶于水 |
Pb(CH3COO)2 | - | 无色 | 易溶于水 |
PbCrO4 | - | 黄色 | 难溶于水 |
Pb(OH)2 | 弱碱性 | 白色 | PH=7.2开始沉淀 ;PH=8.7完全沉淀 |
②PbCrO4可由沸腾的铬酸盐溶液与铅盐溶液作用制得,含PbCrO4晶种时更易生成
③六价铬在溶液中物种分布分数与pH关系如下图所示。
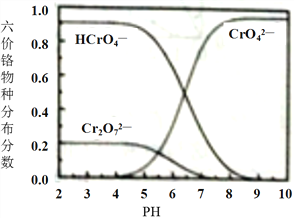
(1)“制NaCrO2(aq)”时,控制NaOH溶液加入量的操作方法是______。
(2)“氧化”时发生反应的离子方程式为______。
(3)下列说法正确的是(______)
A.两次煮沸的目的不相同
B.步骤2可以先加入一滴0.5mol·LPb(NO3)2溶液搅拌片刻,待产生少量沉淀后,继续滴加至有大量沉淀产生。
C.静置后,向上层清液中继续滴入Pb(NO3)2溶液,若无沉淀生成,则说明滴加完全。
D.小火加热的目的是为了避免反应过快。
(4)步骤1为__________________________________________________________。
(5)为测定产品的纯度,可用先用硝酸溶解PbCrO4,然后用EDTA(简写为Y4-)标准溶液滴定,反应的离子方程式:Pb2+ + Y4- =PbY2-。测定时,先称取0.5000g无水PbCrO4产品,溶解后,用0.05000 mol·L-1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液26.50 mL,则测得无水PbCrO4产品的纯度是_________(以质量分数表示)。
【答案】 不断搅拌下逐滴加入NaOH溶液,至产生的绿色沉淀恰好溶解 CrO2-+3H2O2+2OH-=2CrO42-+4H2O ABC 在不断搅拌下,向“冷却液”中加入6mol·L-1的醋酸至弱酸性(pH略小于7) 85.60%
【解析】(1)根据题给信息可知,Cr(OH)3为两性氢氧化物,溶于过量的强碱溶液,所以,制NaCrO2(aq)时,控制NaOH溶液加入量的操作方法是:不断搅拌下逐滴加入NaOH溶液,至产生的绿色沉淀恰好溶解为止;正确答案:不断搅拌下逐滴加入NaOH溶液,至产生的绿色沉淀恰好溶解。
(2)双氧水能够在碱性环境下,把+3价铬氧化为+6价铬,“氧化”时发生反应的离子方程式为CrO2-+3H2O2+2OH-=2CrO42-+4H2O;正确答案: CrO2-+3H2O2+2OH-=2CrO42-+4H2O。
(3)第一次煮沸是为了除去双氧水,第二次是把溶液浓缩,两次煮沸的目的不相同,A正确;将溶液加热至沸,先加入一滴0.5mol/LPb(NO3)2溶液搅拌片刻产生少量沉淀,然后继续滴加至有大量沉淀,步骤2可以先加入一滴0.5mol/LPb(NO3)2溶液搅拌片刻,待产生少量沉淀后,继续滴加至有大量沉淀PbCrO4产生,B正确;静置,向上层清液中滴入Pb(NO3)2溶液,若无沉淀生成,证明CrO42-沉淀完全,停止滴加,C正确;温度过高,双氧水易分解,D错误;正确选项ABC。
(4)由题意可知Pb2+在弱碱性环境下,生成Pb(OH)2沉淀,因此步骤1为目的就是提供弱酸性环境,具体操作为在不断搅拌下,向“冷却液”中加入6mol·L-1的醋酸至弱酸性(pH略小于7) ;正确答案: 在不断搅拌下,向“冷却液”中加入6mol·L-1的醋酸至弱酸性(pH略小于7) 。
(5)依据方程式Pb2+ + Y4- =PbY2-分析,PbCrO4的物质的量=0.0500mol/L×0.02650L=0.001325mol,PbCrO4的质量为0.001325mol×323=0.4280g,则则测得无水PbCrO4产品的纯度是0.4280/0.5000×100%=85.60%;正确答案:85.60%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】一定条件下硝酸铵受热分解的化学方程式为:5NH4NO3![]() 2HNO3+4N2+9H2O,在反应中被氧化与被还原的氮原子数之比为( )
2HNO3+4N2+9H2O,在反应中被氧化与被还原的氮原子数之比为( )
A. 5∶3 B. 5∶4 C. 1∶1 D. 3∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类中,所属关系不符合“X包含Y、Y包含Z”的有
选项 | X | Y | Z |
A | 芳香族化合物 | 芳香烃的衍生物 |
|
B | 脂肪族化合物 | 链状烃的衍生物 | CH3COOH(乙酸) |
C | 环状化合物 | 芳香族化合物 | 苯的同系物 |
D | 不饱和烃 | 芳香烃 |
|
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(g)+5B(g)![]() 4C(g)+6D(g),在5 L的密闭容器中进行,半分钟后,C的物质的量增加了0.30 mol。下列叙述正确的是( )
4C(g)+6D(g),在5 L的密闭容器中进行,半分钟后,C的物质的量增加了0.30 mol。下列叙述正确的是( )
A. A的平均反应速率是0.010 molL﹣1s﹣1
B. 容器中含D物质的量至少为0.45 mol
C. 容器中A、B、C、D的物质的量的比一定是4∶5∶4∶6
D. 容器中A的物质的量一定增加了0.30 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室要用CuSO4·5H2O晶体配制480mL 0.1mol/L CuSO4溶液,回答下列问题:
(1)应该用托盘天平称取CuSO4·5H2O________g。
(2)所需仪器除了烧杯、玻璃棒、胶头滴管,量筒、托盘天平外,还缺少_____________、_________。
(3)实验中两次用到玻璃棒,起作用分别是________________、______________。
(4)配制溶液时有以下几个操作:
①溶解 ②摇匀 ③洗涤 ④冷却 ⑤称量 ⑥转移溶液 ⑦定容
正确的操作顺序是__________________(填序号)。
(5)若实验中有下列情况,对配制溶液的浓度有何影响?(填“偏高”、“偏低”或“无影响”)
A.胆矾失去了部分结晶水_________________________;
B.定容时加水超过刻度线___________________________;
C.最终定容时仰视观察液面_________________________。
(6)如图是温度计、量筒的一部分,下述读数(虚线对应刻度)及说法正确的是________。

A.①是量筒,读数为2.5 mL B.②是量筒,读数为2.5 mL
C.①是温度计,读数为3.5℃ D.②是温度计,读数为2.5 ℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某化学实验的结果如下表:
实验序号 | 反应物 | 在相同温度下测得的反 | |
大小相同的金属片 | 酸溶液 | ||
1 | 镁条 | 1 mol·L-1盐酸 | v1 |
2 | 铁片 | 1 mol·L-1盐酸 | v2 |
3 | 铁片 | 0.1 mol·L-1盐酸 | v3 |
下列结论正确的是
A.v1>v2>v3B.v3>v2>v1C.v1>v3>v2D.v2>v3>v1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是某化学研究小组探究外界条件对化学反应速率和化学平衡影响的图像,其中图像和实验结论表达均正确的是( )


A. ①是其他条件一定时,反应速率随温度变化的图像,正反应ΔH<0
B. ②是在平衡体系的溶液中溶入少量KCl晶体后化学反应速率随时间变化的图像
C. ③是在有无催化剂存在下建立的平衡过程图像,a是使用催化剂时的曲线
D. ④是一定条件下,向含有一定量A的容器中逐渐加入B时的图像,压强p1>p2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应mA+nB===pC+qD中,若v(A)=4 mol·L-1·min-1, 而v(B)=1 mol·L-1·min-1,A表示的反应速率比B表示的反应速率快,而m、n符合的关系
A. m∶n=4∶1 B. m∶n<4∶1 C. m∶n>4∶1 D. 无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学反应中,反应前与反应后相比较,肯定不变的是
①元素的种类 ②原子的种类 ③分子数目 ④原子数目
⑤反应前物质的质量总和与反应后物质的质量总和
⑥如果在水溶液中反应,则反应前与反应后阳离子所带的正电荷总数
⑦反应前反应物的总能量与反应后生成物的总能量
A. ①②③④⑦ B. ①②④⑤ C. ①②⑤⑥⑦ D. ②③⑤⑥⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com