
【题目】用规范的化学用语回答下列问题
(1)下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

①从氯化钾溶液中得到氯化钾固体,选择装置__________ (填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置_________,为检测Cl-杂质是否除干净,应进行的操作_________________________________
②从碘水中分离出I2的方法,名称为________________________。
③装置A中①的名称是________,进水的方向是从______(填“上”“下”)口进水,装置B在分液时为使液体顺利下滴,应进行的具体操作是_______________________。
(2)实验室配制Fe(OH)3胶体时,将饱和的FeCl3溶液滴入沸水中,并继续加热至溶液呈红褐色,停止加热。向所得胶体中逐滴加入稀硫酸,开始观察到的现象是__________,这种现象称为胶体的________;最后观察到的现象是_________。
【答案】D A 取少量液体于试管中,加硝酸酸化的硝酸银溶液,若有白色沉淀生成,则有Cl- 萃取 冷凝管 下 打开分液漏斗上端玻璃塞或使玻璃塞上的凹槽对准漏斗上的小孔 有红褐色沉淀生成 聚沉 沉淀溶解
【解析】
(1)①蒸发可以实现易溶于水的固体和水的分离;分离沸点不同的混合物可以用蒸馏的方法;Cl-与Ag+反应生成氯化银白色沉淀,因此检测Cl-杂质是否除干净,应用硝酸酸化的硝酸银溶液,观察是否有白色沉淀生成;
②碘微溶于水,碘易溶于苯、四氯化碳等有机溶剂,且苯、四氯化碳与水互不相溶,可用萃取法分离;
③装置A为蒸馏装置,①为冷凝管,使用时下口进水上口出水可充分冷凝,装置B中在使用分液漏斗时,要打开分液漏斗上端玻璃塞或使玻璃塞上的凹槽对准漏斗上的小孔,以保证内部液体顺利流下;
(2)向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体,氢氧化铁胶体滴入硫酸先聚沉生成沉淀氢氧化铁,继续滴入硫酸,氢氧化铁沉淀溶解。
(1)①蒸发可以实现易溶于水的固体和水的分离,从氯化钾溶液中得到氯化钾固体可用蒸发的方法;因蒸馏可以实现水中难挥发性杂质和水的分离,则除去自来水中的Cl-等杂质,可用蒸馏的方法;检测Cl-杂质是否除干净,应进行的操作为取少量液体于试管中,加硝酸酸化的硝酸银溶液,若有白色沉淀生成,则有Cl-;
故答案为:取少量液体于试管中,加硝酸酸化的硝酸银溶液,若有白色沉淀生成,则有Cl-;
②碘微溶于水,碘易溶于苯、四氯化碳等有机溶剂,且苯、四氯化碳与水互不相溶,可用萃取法分离;
故答案为:萃取;
③装置A中①的名称是冷凝管,使用时下口进水上口出水,装置B中在使用分液漏斗时,要打开分液漏斗上端玻璃塞或使玻璃塞上的凹槽对准漏斗上的小孔,以保证内部液体顺利流下;
故答案为:冷凝管;下;打开分液漏斗上端玻璃塞或使玻璃塞上的凹槽对准漏斗上的小孔;
(2)向Fe(OH)3胶体中逐滴加入过量的稀硫酸,胶体在电解质溶液中阴阳离子作用下产生聚沉现象,有红褐色沉淀生成,继续滴入硫酸后氢氧化铁又和硫酸反应生成水和可溶性的硫酸铁,所以现象为:开始滴加时有红褐色沉淀出现,继续滴加沉淀溶解,
故答案为:有红褐色沉淀生成;聚沉;沉淀溶解。


科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数的数值为NA,则下列说法正确的是( )
A. 常温常压下,11.2 L甲烷中含有的氢原子数为2NA
B. 标准状况下,0.3 mol二氧化硫中含有的氧原子数为0.3×6.02×1023
C. 标准状况下,2.7 g Al与足量的盐酸反应,生成H2的体积是22.4L
D. 常温下,1 L 0.1 mol·L-1MgCl2溶液中含Cl-数为0.2moL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组的同学在网上查询资料时得知,干燥的CO2与Na2O2不能反应,只有在水蒸气存在下二者才能发生反应。他们设计了如图所示实验装置,用于验证上述结论。
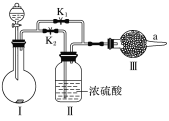
(1)装置Ⅰ中的试剂的最佳组合是________(填字母)。
a.稀盐酸 b.稀硫酸
c.小苏打 d.石灰石
(2)实验时,甲同学认为关闭K1、打开K2,通过观察________判断此时Ⅲ中是否发生了化学反应。
(3)乙同学认为可以分别按“先关闭K1、打开K2,再关闭K2、打开K1”的方式进行操作,并在a处收集所得气体,然后用带火星的木条检验收集到的气体,但他发现两种情况下木条均没有复燃。
①丙同学经过观察分析,建议在Ⅲ后安装一个盛有碱石灰的干燥管,目的是________________
②丁同学认为即使采纳丙同学的建议且最终观察到木条复燃,也不能证明CO2参与了反应,原因是________________________
(4)为进一步达到实验目的,应补充的实验操作是:取最终反应后Ⅲ中所得固体,____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图所示,Na、NaOH、NaHCO3分别与等物质的量的该物质恰好反应时,Na、NaOH、NaHCO3的物质的量之比为( )
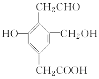
A. 3∶3∶2B. 3∶2∶1
C. 1∶1∶1D. 3∶2∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三种气体X、Y、Z的相对分子质量关系为Mr(X) < Mr(Y)= 0.5Mr(Z),下列说法正确的是()
A.原子数目相等的三种气体,质量最大的是Z
B.相同条件下,同质量的三种气体,气体密度最小的是X
C.若一定条件下,三种气体体积均为2.24 L,则它们的物质的量一定均为0.1 mol
D.同温下,体积相同的两容器分别充2gY气体和1gZ气体,则其压强比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】托盘天平、容量瓶、量筒是常见的中学化学计量仪器,熟知这些仪器的使用是定量研究化学的基础。
(1)其中标示出使用温度的仪器是________________。
(2)下列操作中,容量瓶所不具备的功能有________________ (填序号)。
A.配制一定体积准确浓度的标准溶液 B.贮存溶液
C.测量容量瓶规格以下的任意体积的溶液 D.准确稀释某一浓度的溶液
E.量取一定体积的液体 F.用来加热溶解固体溶质
(3)如图是某些仪器的刻度部分示意图,图中各仪器虚线为所示读数。其中为量筒的是________________ (填编号,),读数为_____mL。

(4)实验室用98%的浓硫酸配制(浓硫酸的密1.84g/mL)450mL 0.1 mol·L-1的硫酸。回答下列问题
① 配制中应选用的玻璃仪器有_________________,应量取________mL 98%的浓硫酸。
② 量筒在使用前已洗干净但不干燥,对结果是否造成影响________(填“是”或“否”),某同学认为将量筒内的浓硫酸倒出之后,应将量筒洗涤—下并将洗涤液倒入烧杯中,最后转移到容量瓶中,你认为他的做法______(填“对”或“错”)。
③对浓硫酸稀释过程中遇到下列情况,使所配制的硫酸浓度大于 0.1mol/L有 ______(填序号)
A.未经冷却趁热将溶液注入容量瓶中
B.摇匀后发现液面低于刻度线,再加水至刻度线
C.容量瓶中原有少量蒸馏水
D.定容时俯视观察液面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列叙述中正确的是
①106 g Na2CO3晶体中的离子总数大于3NA
②25 ℃、1.01×105 Pa下,14 g氮气所含的氮原子数为NA
③标准状况下,22.4LCCl4中所含的分子数约为6.02×1023
④标准状况下,aL的氧气和氮气的混合物含有的分子数约为![]() ×6.02×1023
×6.02×1023
⑤常温常压下,92 g的NO2和N2O4混合气体含有的原子数为6NA
A.①②④B.②④⑤C.③④⑤D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) 如图所示是分离混合物时常用的仪器,回答下列问题:
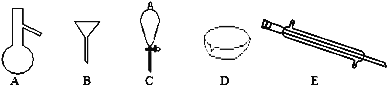
①写出仪器C、E的名称________________、________________。
②分离以下混合物应该主要选用上述什么仪器(填字母符号)
a.粗盐和泥沙:________ b.花生油和水___________。
(2)按照物质的树状分类和交叉分类,硫酸应属于___________。
①酸 ②能导电的纯净物 ③含氧酸 ④混合物 ⑤化合物 ⑥二元酸 ⑦电解质
A.①②③④⑦ B.①③⑤⑥⑦ C.①②③⑤⑥⑦ D.②③⑤⑥⑦
(3)往Fe(OH)3胶体中逐滴加入过量的3mol/L硫酸产生的现象是_______________________。
(4)现在有下列10种物质:① H2O ②空气 ③Mg ④ NH3 ⑤ 稀H2SO4⑥ Ca(OH)2 ⑦CuSO4 .5 H2O ⑧碘酒⑨无水乙醇⑩NaHCO3其中,⑤在水溶液中的电离方程式为______,属于电解质的是__________ (填序号,下同);属于非电解质的是__________ ;属于既不是电解质也不是非电解质的是__________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量是七大基本物理量之一,计算并回答下列问题:
(1)标准状况下,33.6LH2S的物质的量为___mol,质量为___g,所含H原子的数目为____;
(2)16g的O2和O3混合气体中含有O原子数目为____;
(3)1mol/L的BaCl2溶液0.5L中含有Ba2+的物质的量浓度为__mol/L,含有Cl—的物质的量为___mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com