
【题目】为探究碳酸氢钠的热稳定性,并利用其产物验证过氧化钠与二氧化碳的反应,按以下装置图进行实验,按要求填空。
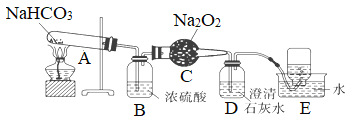
(1)A中反应的化学方程式为________________________________。
(2)B中浓硫酸的作用是__________________。
(3)C中发生反应的化学方程式为_________________________________。
(4)D中反应的离子方程式是_______________________________。
(5)E中收集的气体主要是________。
【答案】2NaHCO3![]() Na2CO3+CO2↑+H2O 干燥二氧化碳 2Na2O2+2CO2=2Na2CO3+O2 Ca2++2OH+CO2=CaCO3↓+H2O O2
Na2CO3+CO2↑+H2O 干燥二氧化碳 2Na2O2+2CO2=2Na2CO3+O2 Ca2++2OH+CO2=CaCO3↓+H2O O2
【解析】
探究碳酸氢钠的热稳定性,并利用其产物验证过氧化钠与二氧化碳的反应,由实验装置可知,A中碳酸氢钠分解生成二氧化碳,B中浓硫酸干燥气体,C中发生2Na2O2+2CO2=2Na2CO3+O2,D中吸收二氧化碳,E为排水法收集氧气,以此来解答。
(1)A中反应为碳酸氢钠受热分解的反应,化学方程式为2NaHCO3![]() Na2CO3+CO2↑+H2O,
Na2CO3+CO2↑+H2O,
故答案为:2NaHCO3![]() Na2CO3+CO2↑+H2O ;
Na2CO3+CO2↑+H2O ;
(2)B中浓硫酸的作用是干燥二氧化碳,故答案为:干燥二氧化碳;
(3)C中发生反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2,
故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(4)D中吸收二氧化碳,离子方程式为Ca2++2OH-+CO2=CaCO3↓+H2O,故答案为: Ca2++2OH-+CO2=CaCO3↓+H2O;
(5)E中收集的气体主要是O2,故答案为:O2。


科目:高中化学 来源: 题型:
【题目】关于氢键,下列说法正确的是
A.分子中有N、O、F原子,分子间就存在氢键
B.因为氢键的缘故,![]() 熔沸点高
熔沸点高
C.NH3的稳定性很强,是因为其分子间能形成氢键
D.“可燃冰” 甲烷水合物(8CH4·46H2O)中CH4与H2O之间存在氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.KClO3和浓盐酸在一定温度下反应,会生成橙黄色的易爆物二氧化氯(ClO2)气体,该反应的化学方程式为2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O。
(1)该反应的还原产物是_____________ (填化学式)。
(2)在反应中浓盐酸表现出来的性质是________(填字母)。
A 只有还原性 B 只有氧化性 C 还原性和酸性 D 氧化性和酸性
(3)若该反应产生2.24L(标准状况)ClO2,则转移电子的物质的量为_____________。
(4)某地生产的氧化钠井盐中含有少量的剧毒物质氰化钠(NaCN),用ClO2可除去其中的氰化钠,从而得到纯净的食盐,同时产生两种无毒气体。写出该反应的化学方程式: __________。
Ⅱ.(5)一定条件下,PbO2与Cr3+反应,产物是Cr2O72-和Pb2+,则与1molCr3+反应所需PbO2的物质的量为_______mol;
(6)在一定条件下,实验室分别以过氧化氢、高锰酸钾、氯酸钾为原料制取氧气,当制得同温同压下相同体积的氧气时,三个反应中转移的电子数之比为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是与生命活动密切相关的三种常见化合物,每种物质所含元素种类均不超过三种,甲是单质。它们之间有如下转化关系:
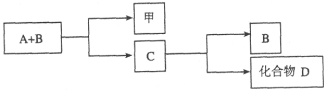
化合物D也是生活中常见的化合物,在一定条件下可发生如下反应:D+3甲![]() 3A+2B
3A+2B
请回答下列问题:
(1)在化合物A、B、C、D中所含元素完全相同的是__________和__________(填字母)。
(2)在常温下,A和B通过__________转化为C。该过程的能量转化关系如何?
____________________。
(3)写出由C生成D的反应的化学方程式____________________。
(4)化合物C是人类生命活动不可缺少的物质之一,它在血液中的正常含量是__________。
(5)目前化合物B在大气中含量呈上升趋势,对环境造成的影响是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4NH3 (g) +5O2(g)![]() 4NO(g) +6H2O(g), △H=-a kJmol-1,在5L密闭容器投入1molNH3和1mol的O2,2分钟后NO的物质的量增加了0.4mol,下列说法正确的是
4NO(g) +6H2O(g), △H=-a kJmol-1,在5L密闭容器投入1molNH3和1mol的O2,2分钟后NO的物质的量增加了0.4mol,下列说法正确的是
A. 2分钟反应放出的热.量值小于0.1akJ
B. 用氧气表示2分钟的反应速率:v(O2)=0.05mol ·L-1 ·min-1
C. 2分钟内NH3的转化率是50%
D. 2分钟末 c(H2O)=0.6mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向盛有氯气的三个集气瓶中,分别注入约五分之一的液体并振荡,观察下图所记录的现象,其中判断各瓶所注入的液体正确的是( )

A. ①中为硝酸银溶液B. ②中为氢氧化钠溶液
C. ③中为蒸馏水D. ③中为澄清石灰水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列化学方程式或离子方程式。
(1)钠与水反应的离子方程式:___;
(2)钠与硫酸铜溶液反应的离子方程式:___;
(3)过氧化钠与二氧化碳反应的化学方程式:___;
(4)过氧化钠与二氧化硫反应的化学方程式:___;
(5)镁在氮气中点燃镁条的化学方程式:___;
(6)镁在二氧化碳中点燃镁条的化学方程式:___;
(7)铝与氢氧化钠溶液的反应的离子方程式:___;
(8)氧化铝与氢氧化钠溶液反应的离子方程式:___;
(9)氢氧化铝与氢氧化钠溶液反应的离子方程式:___;
(10)铝与四氧化三铁反应的化学方程式:___;
(11)铜与氯化铁溶液反应的离子方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M是一种治疗济疮的新型药物,合成路线如下:
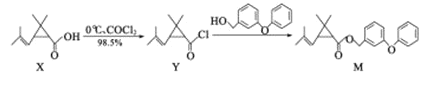
下列说法不正确的是
A.X的分子式为C11H16O2
B.Y分子中所有碳原子不可能在同一平面上
C.Y生成M的反应类型为取代反应
D.可用NaHCO3溶液或溴水鉴别X和M
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.常温常压下,3.4 g NH3中含有的电子数为0.2NA
B.1 mol·L-1的Fe2(SO4)3溶液中,含有的SO42-数目为3NA
C.标准状况下,22.4 L CO2和O2的混合气体中含氧原子数为2NA
D.1 mol Fe在纯氧中完全燃烧,生成Fe3O4,Fe失去8NA个电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com