
【题目】某化学活动小组设计以下装置进行不同实验。其中a为用于鼓入空气的气囊,b为螺旋状铜丝,c烧杯中盛有冰水。

(1)若用A装置做乙醇与乙酸的酯化反应实验,则还需连接的装置是_________(填序号),该装置中应加入试剂___________。从实验安全角度考虑,A装置试管中除加入反应液外,还需加入的固体物质是_________,该物质的作用是______________________。
(2)该小组同学欲做乙醇氧化成乙醛的实验,则应选用的装置是__________(填序号),写出该反应的化学方程式_______________。用制得的乙醛溶液进行银镜反应,正确的操作顺序是_________(填序号)。
①向试管中滴入3滴乙醛溶液。
②一边振荡一边滴入2%的稀氨水,直至最初产生的沉淀恰好溶解为止。
③振荡后放入热水中水浴加热。
④在洁净的试管中加入1mL 2%的AgNO3溶液。
【答案】D 饱和Na2CO3溶液 碎瓷片或沸石 防暴沸 A、B、C ![]() ④②①③
④②①③
【解析】
(1)若用A装置做乙醇与乙酸的酯化反应实验,需要连接D装置(导管口为插入溶液中,目的是防止倒吸)吸收乙醇,中和乙酸,降低乙酸乙酯溶解度;A装置液体加热沸腾需要加入碎瓷片或沸石防止暴沸;
(2)做乙醇氧化成乙醛的实验,需要提供乙醇蒸气和氧气在催化剂作用下氧化反应生成乙醛,冷却得到液体乙醛;乙醛溶液进行银镜反应,先制取银氨溶液,向硝酸银溶液中滴入氨水至变色沉淀全部溶解得到银氨溶液,滴入乙醛溶液在水浴中加热反应观察银镜现象;
(3)乙醛分子间易形成加合物(C2H4O)n而不能发生银镜反应,说明分子中无醛基;醛基中羰基相互加成形成环状结构。
(1)若用A装置做乙醇与乙酸的酯化反应实验,需要连接D装置(导管口为插入溶液中,目的是防止倒吸),加入饱和碳酸钠溶液,吸收乙醇,中和乙酸,降低乙酸乙酯溶解度;A装置液体加热沸腾需要加入碎瓷片或沸石,防止暴沸;
(2)做乙醇氧化成乙醛的实验,需要提供乙醇蒸气和氧气在催化剂作用下氧化反应生成乙醛,反应的化学方程式为:![]() ,冷却得到液体乙醛装置连接为A、B、C;乙醛溶液进行银镜反应,先制取银氨溶液,向硝酸银溶液中滴入氨水至变色沉淀全部溶解得到银氨溶液,滴入乙醛溶液在水浴中加热反应观察银镜现象,实验顺序是④②①③。
,冷却得到液体乙醛装置连接为A、B、C;乙醛溶液进行银镜反应,先制取银氨溶液,向硝酸银溶液中滴入氨水至变色沉淀全部溶解得到银氨溶液,滴入乙醛溶液在水浴中加热反应观察银镜现象,实验顺序是④②①③。


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】如图是某种有机物分子的球棍模型。图中的“棍”代表单键或双键,不同大小的“球”代表三种不同的短周期元素的原子。对该有机物的叙述错误的是( )
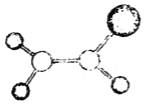
A.该有机物的分子式可能为C2HCl3
B.该有机物分子中的所有原子在同一平面上
C.该有机物无相同官能团同分异构体
D.该有机物可以和氢气发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaCO3广泛存在于自然界,是一种重要的化工原料。大理石主要成分为CaCO3,另外有少量的含硫化合物。实验室用大理石和稀盐酸反应制备CO2气体。下列装置可用于CO2气体的提纯和干燥。完成下列填空:
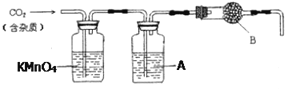
(1)用浓盐酸配制1:1(体积比)的稀盐酸(约6 mol·L-1),需要的玻璃仪器有___________
(2)上述装置中,A是___________溶液,其作用是___________ 。
(3)上述装置中,B物质是___________。
(4)一次性饭盒中石蜡和CaCO3在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下:剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重
①从物质分类的角度分析,石蜡属于有机物中的____________类,为了将石蜡从饭盒中溶出,应选用下列试剂中的__________。
a.氯化钠溶液 b.稀醋酸 c.稀硫酸 d 正已烷
②饭盒中的碳酸钙常用稀醋酸将其溶出,试写出其反应的离子方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2008奥运吉祥物福娃,其外材为纯羊毛线,内充物为无毒的聚酯纤维(如图)。下列说法正确的是( )

A.羊毛与聚酯纤维的化学成分相同
B.聚酯纤维和羊毛一定条件下均能水解
C.该聚酯纤维的单体为对苯二甲酸和乙醇
D.聚酯纤维属于纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A.14g乙烯和丁烯的混合物中含有的原子总数为3 NA
B.标准状况下,22.4L己烷中共价键数目为19 NA
C.7g C2H4中含有的氢原子数目为2 NA
D.1mol苯乙烯( ![]() )中含有的C=C数为4 NA
)中含有的C=C数为4 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化亚铜(Cu2O)可用于陶瓷、固体整流器,可用下列反应制备:2(CuSO4H2O)![]() Cu2O+SO2↑+SO3↑+O2↑+10H2O。回答下列问题:
Cu2O+SO2↑+SO3↑+O2↑+10H2O。回答下列问题:
(1)Cu2O中基态铜的离子的价层电子排布图为________________。上述反应中,电负性最大的元素是________________(填元素符号)
(2)元素Cu和Ni相邻,其第一、二电离能数据如表所示:
I1/(kJ/mol) | I2/(kJ/mol) | |
Ni | 737.1 | 1753.0 |
Cu | 745.5 | 1957.9 |
铜的第一、二电离能都比镍对应的高,其原因除了铜的核电荷数比多,对外电子的吸外力大外,还有一个原因是________。
(3)已知H2SO4的结构式如图所示,上述反应中:

①在上述产物中,VSEPR模型与SO42-相同的是________(填化学式)
②SO3分子的立体构型是________________,写出一种与SO3互为等电子体的离子:________(填离子符号)
(4)Cu2+、Cu+与CN-、OH-、NH3、H2O等组成多种配离子。[Cu(NH3)4]2+中的Cu2+配位数为________。
(5)铜元素和氧元组成一种晶体M,M的晶胞如图所示。

已知:NA是阿伏加德罗常数的值,M晶体密度为dgcm-3。M的晶胞中Cu+、Cl-个数比为________,晶胞参数为________pm(用含d和NA的代数式表示)。(用含d和NA的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A.氯气溶于水:Cl2+H2OH++Cl-+HClO
B.金属铝溶于氢氧化钠溶液:Al+2OH-=AlO2-+H2↑
C.苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2=2C6H5OH+CO32-
D.实验室制备氢氧化铁胶体:Fe3++3H2O=Fe(OH)3(胶体)+3H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式书写不正确的是( )
A. 乙烯使溴的四氯化碳溶液褪色: Br2+ CH2=CH2→ CH2BrCH2Br
B. 用惰性电极电解氯化钠溶液: 2Cl -+ 2H2O![]() H2+Cl2↑+ 2OH-
H2+Cl2↑+ 2OH-
C. 实验室制乙炔: CaC2 + 2H2O → C2H2↑ + Ca(OH)2
D. 溴乙酸与氢氧化钠溶液共热: BrCH2COOH+OH-![]() BrCH2COO-+H2O
BrCH2COO-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验过程如图所示,则图③试管中的现象是( )
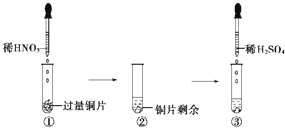
A.铜片溶解,产生无色气体,该气体遇空气变为红棕色
B.铜片溶解,产生无色气体,该气体遇到空气不变色
C.铜片溶解,放出红棕色有刺激性气味的气体
D.无明显现象,因稀硫酸不与铜反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com