
【题目】t ℃时,某平衡体系中含有X、Y、Z、W四种物质,此温度下发生反应的平衡常数表达式为K=![]() 。有关该平衡体系的说法正确的是
。有关该平衡体系的说法正确的是
A. 当混合气体的平均相对分子质量保持不变时,反应达平衡
B. 增大压强,各物质的浓度不变
C. 升高温度,平衡常数K增大
D. 增加X的量,平衡既可能正向移动,也可能逆向移动
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.![]() 的名称为2-乙基丁烷
的名称为2-乙基丁烷
B.35Cl和37Cl 互为同素异形体
C.![]() 经催化加氢后能生成2-甲基戊烷
经催化加氢后能生成2-甲基戊烷
D.CH3CH2COOH和HCOOCH3互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】推理是化学学习中常用的思维方法,下列推理合理的是
A. NaOH和CaCl2都是离子化合物,所以二者化学键类型相同
B. 可逆反应达平衡时,体系中各组分的浓度不再变化,可推知正、逆反应停止了
C. 原电池加快某些反应的速率,所以用锌与稀硫酸反应制取氢气常加入少量硫酸铜
D. 同条件下反应物浓度越大反应越快,所以铁在浓硝酸中比在稀硝酸中溶解得快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源。
(1)在25℃、101kPa下,16g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式___。
(2)化学反应中放出的热能(焓变,△H)与反应物和生成物的键能(E)有关。
已知:H2(g)+Cl2(g)=2HCl(g) △H=﹣185kJ/mol,
E(H﹣H)=436kJ/mol, E(Cl﹣Cl)=243kJ/mol则E(H﹣Cl)=___。
(3)①如图是N2和H2反应生成2molNH3过程中能量变化示意图,请计算每生成1molNH3放出热量为:___;
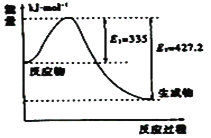
②若起始时向容器内放入1molN2和3molH2,达平衡后N2的转化率为20%,则反应放出的热量为Q1kJ,则Q1的数值为___;
(4)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH=akJ·mol-1;
CO(g)+![]() O2(g)=CO2(g) ΔH=bkJ·mol-1;
O2(g)=CO2(g) ΔH=bkJ·mol-1;
C(石墨)+O2(g)=CO2(g) ΔH=ckJ·mol-1
则反应:4Fe(s)+3O2(g)=2Fe2O3(s)的焓变ΔH=___kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列原子或离子的电子排布的表示方法中,正确的是___,违反了能量最低原理的是___,违反洪特规则的是__。
①Ca2+:1s22s22p63s23p6
②F-:1s22s23p6
③P:![]()
④Cr:1s22s22p63s23p63d44s2
⑤Fe:1s22s22p63s23p63d64s2
⑥Mg2+:1s22s22p6
⑦C:![]()
绿柱石被国际珠宝界公认为四大名贵宝石之一。主要成分为Be3Al2[Si6O18],因含适量的Cr2O3(0.15~0.6%),而形成祖母绿。试回答下列问题:
(2)基态Al原子中,电子填充的最高能级是___,基态Cr原子的价电子排布式是___。
(3)用“>”或“<”填空:
第一电离能 | 沸点 | 离子半径 |
Be___B | H2S___H2O | Al3+___O2- |
(4)卟啉与Fe2+合即可形成血红素,Fe2+的电子排布式为___,铁在周期表中的位置为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式的叙述中,正确的是( )
A.对于反应CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH<0,升温ΔH不变
CO2(g)+H2(g) ΔH<0,升温ΔH不变
B.已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定
C.已知2H2(g)十O2(g)=2H2O(g) △H = -483.6 kJ/mol,则H2的燃烧热为 241.8 kJ/mol
D.已知2C(s)+2O2(g)=2CO2(g) △H1,2C(s)+O2(g)=2CO(g) △H2 ,则△H1>△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,相同pH的两种一元弱酸HA与HB溶液分别加水稀释,溶液pH随加水体积变化的曲线如图所示。下列说法正确的是

A. HB的酸性强于HA
B. a点溶液的导电性大于b点溶液
C. 同浓度的NaA与NaB溶液中,c(A-)=c(B-)
D. 加水稀释到pH相同时,酸HA、HB用到的水V(A)小于V(B)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在T农业生产中有重要的作用
(1)![]() 在空气屮灼烧可制得铁系氧化物材料。已知
在空气屮灼烧可制得铁系氧化物材料。已知![]() ,101kPa时:
,101kPa时:
![]()
![]()
![]()
![]()
写出![]() 在空气中灼烧生成
在空气中灼烧生成![]() 的热化学方程式______
的热化学方程式______
(2)生产中常用CO还原铁的氧化物冶炼铁。T业上可利用甲烷与水蒸气反应制备CO原料气:![]() 。如图是
。如图是![]() 与
与![]() 初始体积比为1:3时乎衡体系中甲烷的体积分数受温度、压强影响的关系图:
初始体积比为1:3时乎衡体系中甲烷的体积分数受温度、压强影响的关系图:
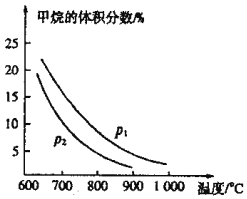
①甲烷与水蒸气反应制备CO的反应为______![]() 填“放热”或“吸热”
填“放热”或“吸热”![]() 反应,压强
反应,压强![]() ______
______![]() 填“
填“![]() ”或“
”或“![]() ”
”![]()
②在恒温恒压的条件下,上述反应达到平衡状态。当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是______
A.逆反应速率先增大后减小
B.混合气体的密度减小
C.化学平衡常数K值减小
D.水蒸气的转化率减小
③在恒温、恒容的条件下,向上述平衡体系中充人体积比为:3的甲烷与水蒸气混合气体,再次达到平衡时CO的体积分数______![]() 填“增大”、减小”或“不变”
填“增大”、减小”或“不变”![]() ,
,
(3)已知![]() 时,
时,![]() ,该温度下反应
,该温度下反应![]() 的平衡常数
的平衡常数![]() ______
______
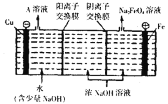
(4)工业上通过电解浓NaOH溶液可制备![]() ,然后转化为
,然后转化为![]() ,电解原理如图所示,则A溶液中溶质的成分为______
,电解原理如图所示,则A溶液中溶质的成分为______![]() 填化学式
填化学式![]() :阳极的电极反应式为______
:阳极的电极反应式为______
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象能得出相应结论的是( )
选项 | 实验操作 | 现象 | 结论 |
A | SO2缓慢通入滴有酚酞的NaOH溶液中 | 溶液红色褪去 | SO2具有漂白性 |
B | 将充满NO2的密闭玻璃球浸泡在热水中 | 气体红棕色加深 | 2NO2(g) |
C | 某黄色溶液X中加入淀粉-KI溶液 | 溶液变成蓝色 | 溶液X中含有Br2 |
D | 无水乙醇中加入浓硫酸,加热,产生的气体Y通入酸性KMnO4溶液 | 溶液紫色褪去 | 气体Y中含有乙烯 |
A. AB. BC. CD. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com