
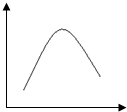
 对如图的解读不正确的是( )
对如图的解读不正确的是( )| 选项 | 研究对象 | 横坐标 | 纵坐标 |
| A | 浓醋酸溶于水 | 加入水的量 | 导电能力 |
| B | A(g)?2B(g) | 压强 | 正反应速率 |
| C | 镁和稀盐酸反应 | 时间 | 反应速率 |
| D | 往密闭容器中通入 N2和H2发生反应: N2(g)+3H2(g)?2NH3(g)△H<0 | 温度 | NH3的体积分数 |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:
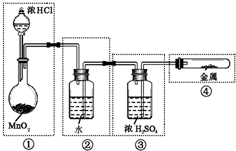 实验室用MnO2与浓HCl反应制Cl2,若用如图所示的实验装置来制备纯净、干燥的氯气,并试验它与金属镁粉的反应.每个虚线框表示一个单元装置,其中错误的是( )
实验室用MnO2与浓HCl反应制Cl2,若用如图所示的实验装置来制备纯净、干燥的氯气,并试验它与金属镁粉的反应.每个虚线框表示一个单元装置,其中错误的是( )| A、只有①和②处 |
| B、只有②处 |
| C、只有①、②和③处 |
| D、①、②、③、④处 |
查看答案和解析>>
科目:高中化学 来源: 题型:
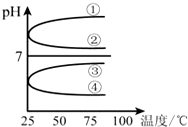 (1)稀释0.1mol?L-1氨水时,随着水量的增加而减小的是
(1)稀释0.1mol?L-1氨水时,随着水量的增加而减小的是| c(NH3?H2O) |
| c(OH-) |
| c(OH-) |
| c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、各平衡常数的大小与温度有关 |
| B、若温度升高则各平衡常数一定增大 |
| C、平衡常数的大小能说明反应(或电离、溶解)进行的程度 |
| D、平衡常数越大反应(或电离)程度越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(O2)=0.01 mol?L-1?s-1 |
| B、v(NH3)=0.02 mol?L-1?s-1 |
| C、v(H2O)=0.04 mol?L-1?s-1 |
| D、v(NO)=0.03 mol?L-1?s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、C(s)+O2(g)═CO2(g)△H1 C(s)+
| ||
| B、S(g)+O2(g)═SO2(g)△H1 S(s)+O2(g)═SO2(g)△H2 | ||
C、2H2(g)+O2(g)═2H2O(l)△H1 H2(g)+
| ||
| D、CaCO3(s)═CaO(s)+CO2(g)△H1 CaO(s)+H2O(l)═Ca(OH)2(s)△H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com