
| A、0.045mol?L-1 |
| B、0.036mol?L-1 |
| C、0.026mol?L-1 |
| D、0.030mol?L-1 |
| V |
| Vm |
| n |
| V |
| 4 |
| 5 |
| ||
| 22.4L/mol |
| 1 |
| 28 |
| 1 |
| 28 |
| ||
| 1L |


科目:高中化学 来源: 题型:
| 阳离子 | K+、Ag+、Mg2+ |
| 阴离子 | NO3-、CO32-、SiO32-、SO42- |
| 序号 | 实验内容 | 实验结果 |
| Ⅰ | 向该溶液中加入足量稀HCl | 产生白色沉淀并放出0.56L气体 |
| Ⅱ | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为2.4g |
| Ⅲ | 在Ⅱ的滤液中滴加BaCl2溶液 | 无明显现象 |
| 阴离子 | NO3- | CO32- | SiO32- | SO42- |
| c/mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳与二氧化碳在高温条件下反应 |
| B、Ba(OH)2?8H2O与NH4Cl的反应 |
| C、乙炔在O2中的燃烧 |
| D、氢氧化钠与稀盐酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3CH(OCH3)CHO |
| B、OHCCH2COOCH2CH3 |
| C、CH3COOCH(CH3)CHO |
| D、CH3COOCH2CH2COCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①④⑨ | B、①③⑤⑧ |
| C、①④⑥⑦ | D、③⑦⑧⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、已知有2mol Na218O2与足量的CO2充分反应,生成的碳酸钠中含18O的原子为NA个 |
| B、电解精炼镍时,当电源提供NA个电子时,阳极溶解的Ni2+应为0.5mol |
| C、标准状况下,22.4L SO2和O2的混合气体中含有的氧原子数为2NA |
| D、向足量MnO2中加入溶有4mol HCl的浓盐酸,加热,反应后的溶液中的Cl-数是2NA个(不考虑盐酸的挥发) |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、H2O2的电子式为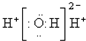 |
| B、4℃时,纯水的pH<7,溶液呈中性 |
| C、H2O2中,质量数之和是质子数之和的两倍 |
| D、273K、101kPa,水分子间的平均距离d(气态)>d(固态)>d(液态) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com