
【题目】铜锌原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )
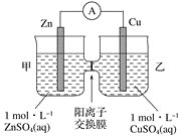
A. 铜电极上发生氧化反应
B. 电池工作一段时间后,甲池中硫酸根的浓度减小
C. 电池工作一段时间后,乙池溶液的总质量增加
D. 阴、阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
科目:高中化学 来源: 题型:
【题目】如图是实验室研究潜水艇中供氧体系反应机理的装置图(夹持仪器略)。
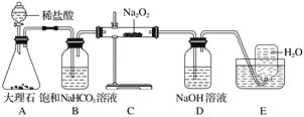
(1)A装置为CO2的发生装置,反应的离子方程式为____________________。
(2)B装置可除去A装置中可能挥发出的___________,反应的离子方程式为_______________。
(3)C装置为O2的发生装置,反应的化学方程式为__________________、________________。
(4)D装置可除去C装置中未反应的__________,反应的离子方程式为____________________。
(5)E装置为排水法收集O2的装置,检验所收集的气体为O2的方法为_____________________。
(6)C装置中固体由淡黄色完全变为白色,检验固体成分的实验方案为取少量C装置中反应后的固体溶于水,向溶液中滴入过量___溶液,若有白色沉淀生成,则证明固体中含有___;过滤,向滤液中滴入几滴酚酞溶液,若__且不褪色,则证明固体中含有__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作对应的现象不符合事实的是
|
|
|
|
A.将二氧化碳气体通入CaCl2溶液,不会产生白色沉淀 | B.用激光笔照射Fe(OH)3胶体,产生“丁达尔效应” | C.将湿润的有色布条放入盛有干燥氯气的瓶中,布条不褪色 | D.将滴管中的浓盐酸加入碳酸氢钠溶液,气球体积由小变大 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组为了证明二氧化硫和氯气的漂白性,设计了如下图所示的实验装置:
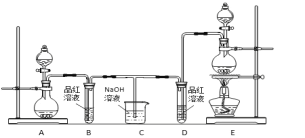
他们制备二氧化硫和氯气所依据的原理分别是:
Na2SO3+H2SO4 = Na2SO4+H2O+SO2↑
MnO2+4HCl(浓) ![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
(1)用来制取氯气的装置是______(填字母),反应中浓盐酸所表现出________________性质。
(2)反应开始一段时间后,B、D试管中的品红溶液均退色。停止通气后,再给B、D两个试管分别加热____ (填" B”或“D")试管中无明显现象。
(3)装置C的作用是________________________;
(4)若装置D中的品红溶液换成紫色的石蕊溶液,则出现的现象是____________________________;
(5)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不退色。查阅资料得知:两种气体按体积比1:1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,该反应的化学方程式是:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为800℃时A、B、C三种气体在密闭容器中反应时浓度的变化,只从图上分析不能得出的结论是( )
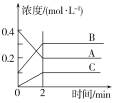
A.发生的反应可表示为2A(g)![]() 2B(g)+C(g)
2B(g)+C(g)
B.前2 min A的分解速率为0.1 mol·L-1·min-1
C.达平衡后,若升高温度,平衡向正反应方向移动
D.达平衡后,若增大压强,平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用右图所示的装置及药品进行酸性强弱比较的实验,下列说法不正确的是
A.①和②中发生的反应均为复分解反应
B.向Na2SiO3饱和溶液中滴酚酞溶液无明显现象
C.一段时间后②中有胶冻状物质生成
D.该实验能证明酸性强弱的顺序是:硫酸>碳酸>硅酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“84”消毒液(有效成分为![]() )可用于消毒和漂白,下列实验现象的分析不正确的是
)可用于消毒和漂白,下列实验现象的分析不正确的是
实验操作 | ①
| ② | ③
|
实验现象 | 混合后溶液的 | 混合后溶液 | 混合后溶液 |
A. 对比实验①和②,②中蓝色迅速褪去的原因是发生了反应![]()
B. 实验③中产生的气体是![]() ,由
,由![]() 分解得到:
分解得到:![]()
C. 对比实验②和③,溶液的![]() 可能会影响
可能会影响![]() 的氧化性或
的氧化性或![]() 的还原性
的还原性
D. 加酸可以提高“84”消毒液的漂白效果,但需要调控到合适的![]() 才能安全使用
才能安全使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应过程如图所示,关于该反应的下列说法中不正确的是( )
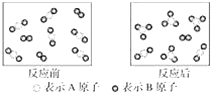
A. 该反应为可逆反应
B. 该反应可表示为2AB2+B2![]() 2AB3
2AB3
C. 若反应开始加入1 mol B2,则会生成2 mol AB3
D. 该过程中,已反应的AB2占AB2总数的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:①25℃、101kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221kJ·mol1;②稀溶液中,H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3kJ·mol1。下列结论中正确的是( )
A. 碳的燃烧热ΔH<-110.5kJ·mol1
B. ①的反应热为221kJ·mol1
C. 稀醋酸与稀氢氧化钠溶液反应生成1mol水,放出57.3kJ热量
D. 由②可知稀溶液中![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com