
ΓΨΧβΡΩΓΩœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©
A.“ρΈΣ SO2 ΨΏ”–Τ·ΑΉ–‘Θ§Υυ“‘ΥϋΡή ΙΤΖΚλ»ή“ΚΓΔδεΥ°ΓΔKMnO4(HΘΪ)ΓΔ ·»ο»ή“ΚΆ …Ϊ
B.œρ 50 mL 18.4 mol/L H2SO4 »ή“Κ÷–Φ”»κΉψΝΩΒΡΆ≠Τ§≤ΔΦ”»»Θ§≥δΖ÷Ζ¥”ΠΚσΘ§±ΜΜΙ‘≠ΒΡ H2SO4ΒΡΈο÷ ΒΡΝΩ–Γ”Ύ 0.46 mol
C.SO2ΓΔNO2 ΚΆ CO2 ΕΦ «“ΐΤπΥα”ξΒΡ÷ς“Σ‘≠“ρΘ§ΒΦ÷¬”ξΥ°ΒΡ pH –Γ”Ύ 5.6
D.≈® HNO3 ”κ≈®―ΈΥαΑ¥ 3ΓΟ1 ΒΡΧεΜΐ±»ΜλΚœΥυΒΟΒΡΜλΚœΈοΫ–ΆθΥ°Θ§Ρή»ήΫβΫπΚΆ≤§
ΓΨ¥πΑΗΓΩB
ΓΨΫβΈωΓΩ
A. SO2 ΙδεΥ°ΓΔKMnO4(HΘΪ)±μœ÷ΒΡ «ΜΙ‘≠–‘Θ§SO2≤ΜΡήΤ·ΑΉ ·»ο»ή“ΚΘ§A―Γœν¥μΈσΘΜ
B. 50 mL 18.4 mol/L H2SO4Κ§H2SO4ΘΚ50ΓΝ10-3LΓΝ18.4 mol/L=0.92molΘ§Φ”»κΉψΝΩΒΡΆ≠Τ§≤ΔΦ”»»ΘΚ2H2SO4(≈®) + Cu ![]() CuSO4 + 2H2O + SO2ΓϋΘ§±ΜΜΙ‘≠ΒΡ H2SO4’ΦΖ¥”ΠΒΡH2SO4ΉήΝΩΒΡ“ΜΑκΘ§ΒΪΥφΖ¥”ΠΫχ––Θ§ΝρΥα±δœΓΘ§Ζ¥”ΠΆΘ÷ΙΓΘΥυ“‘Θ§≥δΖ÷Ζ¥”ΠΚσΘ§±ΜΜΙ‘≠ΒΡ H2SO4ΒΡΈο÷ ΒΡΝΩ–Γ”Ύ0.92molΓ¬2= 0.46 molΘ§B―Γœν’ΐ»ΖΘΜ
CuSO4 + 2H2O + SO2ΓϋΘ§±ΜΜΙ‘≠ΒΡ H2SO4’ΦΖ¥”ΠΒΡH2SO4ΉήΝΩΒΡ“ΜΑκΘ§ΒΪΥφΖ¥”ΠΫχ––Θ§ΝρΥα±δœΓΘ§Ζ¥”ΠΆΘ÷ΙΓΘΥυ“‘Θ§≥δΖ÷Ζ¥”ΠΚσΘ§±ΜΜΙ‘≠ΒΡ H2SO4ΒΡΈο÷ ΒΡΝΩ–Γ”Ύ0.92molΓ¬2= 0.46 molΘ§B―Γœν’ΐ»ΖΘΜ
C. CO2 ≤Μ «“ΐΤπΥα”ξΒΡ‘≠“ρΘ§C―Γœν¥μΈσΘΜ
D. ΆθΥ° «≈® HNO3 ”κ≈®―ΈΥαΑ¥ 1ΓΟ3 ΒΡΧεΜΐ±»ΜλΚœΥυΒΟΒΡΜλΚœΈοΘ§D―Γœν¥μΈσΘΜ
¥πΑΗ―ΓBΓΘ



| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΜ·―ß”Ο”ο «―ßœΑΜ·―ßΒΡ÷Ί“ΣΙΛΨΏΘ§œ¬Ν–Μ·―ß”Ο”ο÷–Θ§’ΐ»ΖΒΡ «![]()
A.![]() ΒΡΒγάκΖΫ≥Χ ΫΈΣ
ΒΡΒγάκΖΫ≥Χ ΫΈΣ![]()
B.œρAgClΒΡ±ΞΚΆ»ή“Κ÷–Φ”»κΉψΝΩ≈®![]() »ή“ΚΘ§»ή“Κ÷–ΗςάκΉ”≈®Ε»≤Μ±δ
»ή“ΚΘ§»ή“Κ÷–ΗςάκΉ”≈®Ε»≤Μ±δ
C.≥ΘΈ¬œ¬Θ§![]() ΒΡ
ΒΡ![]() ”κΑ±Υ°ΒΡΜλΚœ»ή“Κ÷–άκΉ”≈®Ε»¥σ–ΓΥ≥–ρΘΚ
”κΑ±Υ°ΒΡΜλΚœ»ή“Κ÷–άκΉ”≈®Ε»¥σ–ΓΥ≥–ρΘΚ![]()
D.![]() ΒΡΥ°ΫβΖ¥”ΠάκΉ”ΖΫ≥Χ ΫΘΚ
ΒΡΥ°ΫβΖ¥”ΠάκΉ”ΖΫ≥Χ ΫΘΚ![]()
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΫϋΤΎΖΔœ÷Θ§H2S «ΦΧNOΓΔCO÷°ΚσΒΡΒΎ»ΐΗω…ζΟϋΧεœΒΤχΧε–≈Κ≈Ζ÷Ή”Θ§ΥϋΨΏ”–≤Έ”κΒςΫΎ…ώΨ≠–≈Κ≈¥ΪΒίΓΔ φ’≈―ΣΙήΦθ«αΗΏ―Σ―ΙΒΡΙΠΡήΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©œ¬ΆΦ «Ά®Ιΐ»»Μ·―ß―≠ΜΖ‘ΎΫœΒΆΈ¬Ε»œ¬”…Υ°ΜρΝρΜ·«βΖ÷Ϋβ÷Τ±Η«βΤχΒΡΖ¥”ΠœΒΆ≥‘≠άμΓΘ

Ά®ΙΐΦΤΥψΘ§Ω…÷ΣœΒΆ≥Θ®ΔώΘ©÷Τ«βΒΡ»»Μ·―ßΖΫ≥Χ ΫΈΣ_____________ΓΘ
Θ®2Θ©H2S”κCO2‘ΎΗΏΈ¬œ¬ΖΔ…ζΖ¥”ΠΘΚH2S(g)+CO2(g) ![]() COS(g) +H2O(g)ΓΘ‘Ύ610 K ±Θ§ΫΪ0.10 mol CO2”κ0.40 mol H2S≥δ»κ2.5 LΒΡΩ’Η÷ΤΩ÷–Θ§Ζ¥”ΠΤΫΚβΚσΥ°ΒΡΈο÷ ΒΡΝΩΖ÷ ΐΈΣ0.02ΓΘΔΌH2SΒΡΤΫΚβΉΣΜ·¬
COS(g) +H2O(g)ΓΘ‘Ύ610 K ±Θ§ΫΪ0.10 mol CO2”κ0.40 mol H2S≥δ»κ2.5 LΒΡΩ’Η÷ΤΩ÷–Θ§Ζ¥”ΠΤΫΚβΚσΥ°ΒΡΈο÷ ΒΡΝΩΖ÷ ΐΈΣ0.02ΓΘΔΌH2SΒΡΤΫΚβΉΣΜ·¬ ![]() =____%Θ§Ζ¥”ΠΤΫΚβ≥Θ ΐK=_____ΓΘ
=____%Θ§Ζ¥”ΠΤΫΚβ≥Θ ΐK=_____ΓΘ
Θ®3Θ©H2SΚΆSO2ΜαΕ‘ΜΖΨ≥ΚΆ»ΥΧεΫΓΩΒ¥χά¥ΦΪ¥σΒΡΈΘΚΠΘ§ΙΛ“Β…œ≤…»ΓΕύ÷÷ΖΫΖ®Φθ…Ό’β–©”–ΚΠΤχΧεΒΡ≈≈Ζ≈Θ§“―÷Σ25ΓφΘ§NH3ΓΛH2OΒΡKb=1.8ΓΝ105Θ§H2SO3ΒΡKa1=1.3ΓΝ102Θ§Ka2=6.2ΓΝ108ΓΘ»τΑ±Υ°ΒΡ≈®Ε»ΈΣ2.0 molΓΛL1Θ§»ή“Κ÷–ΒΡc(OH)=________ molΓΛL1ΓΘΫΪSO2Ά®»κΗΟΑ±Υ°÷–Θ§Β±c(OH)ΫΒ÷Ν1.0ΓΝ107 molΓΛL1 ±Θ§»ή“Κ÷–ΒΡc(![]() )/c(
)/c(![]() )=___________________ΓΘ
)=___________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΑ±Τχ «“Μ÷÷÷Ί“ΣΜ·ΙΛ‘≠ΝœΓΘ
(1)Β¬ΙζΜ·―ßΦ“Ιΰ≤°¥”1902ΡξΩΣ Φ―–ΨΩ”…ΒΣΤχΚΆ«βΤχ÷±Ϋ”Κœ≥…Α±ΓΘ
“―÷ΣΘΚΔΌ![]() ΓςH=a kJ/mol
ΓςH=a kJ/mol
ΔΎΟΩΤΤΜΒlmol”–ΙΊΜ·―ßΦϋ–η“ΣΒΡΡήΝΩ»γœ¬±μΘΚ
H-H | N-H | NΓ‘N |
436kJ | 391kJ | 946k |
‘ρa=_________________ΓΘ
(2)œ¬ΆΦΈΣ≤ΜΆ§Έ¬Ε»(T)ΓΔ≤ΜΆ§ΆΕΝœ±»[n(![]() )/n(
)/n(![]() )] ±Ζ¥”Π¥οΒΫΤΫΚβ ±
)] ±Ζ¥”Π¥οΒΫΤΫΚβ ±![]() ΒΡΉΣΜ·¬ ±δΜ·«ζœΏΓΘ
ΒΡΉΣΜ·¬ ±δΜ·«ζœΏΓΘ

ΔΌ![]() ΓΔ
ΓΔ![]() ΓΔ
ΓΔ![]() ΓΔ
ΓΔ![]() ΒΡ¥σ–ΓΙΊœΒΈΣ__________________ΓΘ
ΒΡ¥σ–ΓΙΊœΒΈΣ__________________ΓΘ
ΔΎ±Θ≥÷Έ¬Ε»ΚΆΧεΜΐ≤Μ±δΘ§ΧαΗΏΆΕΝœ±»[n(![]() )/n(
)/n(![]() )]Θ§‘ρ÷Ί–¬¥οΒΫΤΫΚβ ±Θ§œ¬Ν–ΥΒΖ®“ΜΕ®’ΐ»ΖΒΡ «_______(ΧνΉ÷ΡΗ–ρΚ≈)ΓΘ
)]Θ§‘ρ÷Ί–¬¥οΒΫΤΫΚβ ±Θ§œ¬Ν–ΥΒΖ®“ΜΕ®’ΐ»ΖΒΡ «_______(ΧνΉ÷ΡΗ–ρΚ≈)ΓΘ
A.![]() ΒΡ≈®Ε»‘ω¥σ
ΒΡ≈®Ε»‘ω¥σ
B.![]() ΒΡΉΣΜ·¬ ‘ω¥σ
ΒΡΉΣΜ·¬ ‘ω¥σ
C.![]() ΒΡΧεΜΐΖ÷ ΐ‘ω¥σ
ΒΡΧεΜΐΖ÷ ΐ‘ω¥σ
D.![]() ΒΡ≈®Ε»Φθ–Γ
ΒΡ≈®Ε»Φθ–Γ
ΔέΈ¬Ε»ΈΣ![]() ±Θ§œρ2LΟή±’»ίΤς÷–Φ”»κ1.0mol
±Θ§œρ2LΟή±’»ίΤς÷–Φ”»κ1.0mol![]() ΚΆ1.0mol
ΚΆ1.0mol![]() Θ§»τ5minΚσΖ¥”Π¥οΒΫΤΫΚβΘ§‘ρ”Οv(
Θ§»τ5minΚσΖ¥”Π¥οΒΫΤΫΚβΘ§‘ρ”Οv(![]() )±μ ΨΗΟΖ¥”ΠΒΡΤΫΨυΥΌ¬ ΈΣ____________________ΘΜΖ¥”Π‘Ύ
)±μ ΨΗΟΖ¥”ΠΒΡΤΫΨυΥΌ¬ ΈΣ____________________ΘΜΖ¥”Π‘Ύ![]() ±ΒΡΤΫΚβ≥Θ ΐK=________________ΓΘ
±ΒΡΤΫΚβ≥Θ ΐK=________________ΓΘ
(3)“Μ÷÷–¬–Ά≥ΐ―ΧΤχ÷–ΒΣ―θΜ·ΈοΒΡΖΫΖ® «≤…”Ο![]() ΉςΜΙ‘≠ΦΝΜΙ‘≠―ΧΤχ÷–ΒΡΒΣ―θΜ·Έο«“≤ζΈοΈόΈέ»ΨΘ§–¥≥ω
ΉςΜΙ‘≠ΦΝΜΙ‘≠―ΧΤχ÷–ΒΡΒΣ―θΜ·Έο«“≤ζΈοΈόΈέ»ΨΘ§–¥≥ω![]() ΜΙ‘≠
ΜΙ‘≠![]() ΒΡΜ·―ßΖ¥”ΠΖΫ≥Χ Ϋ_____________________________________ΓΘ
ΒΡΜ·―ßΖ¥”ΠΖΫ≥Χ Ϋ_____________________________________ΓΘ
(4)»τ”Ο±ξΉΦ―ΈΥα≤βΕ®Ρ≥œΓΑ±Υ°ΒΡ≈®Ε»Θ§”Π―Γ‘ώ__________Ής÷Η ΨΦΝΘΜΒΈΕ®Ιΐ≥Χ÷–―έΨΠΉΔ ”_____________ΓΘ“―÷ΣœΓΑ±Υ°ΧεΜΐΈΣ25.0mLΘ§ΒΈΕ®Ϋα χ≤βΒΟœϊΚΡ0.0100mol/L―ΈΥαΒΡΤΫΨυΧεΜΐΈΣ20.0mLΘ§‘ρΗΟΑ±Υ°ΒΡ≈®Ε»ΈΣ________________(±ΘΝτ2ΈΜ”––ß ΐΉ÷)ΘΜ»τΒΈΕ®«ΑΒΈΕ®ΙήΦβΉλ”–Τχ≈ίΘ§ΒΈΕ®ΚσΦβΉλΈόΤχ≈ίΘ§‘ρ≤βΕ®ΫαΙϊ________(ΧνΓΑΤΪ¥σΓ±ΓΔΓΑΤΪ–ΓΓ±ΓΔΓΑ≤Μ±δΓ±)ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΚΘ≤®![]() «Έό…ΪΆΗΟςΒΡΨßΧεΘ§“Ή»ή”ΎΥ°Θ§”ωΥαΝΔΦ¥Ζ÷
«Έό…ΪΆΗΟςΒΡΨßΧεΘ§“Ή»ή”ΎΥ°Θ§”ωΥαΝΔΦ¥Ζ÷![]() Θ§ΝρΜ·ΦνΖ® «ΙΛ“Β…œ÷Τ±ΗΚΘ≤®ΒΡΖΫΖ®÷°“ΜΘ§Ζ¥”Π‘≠άμΈΣΘΚ
Θ§ΝρΜ·ΦνΖ® «ΙΛ“Β…œ÷Τ±ΗΚΘ≤®ΒΡΖΫΖ®÷°“ΜΘ§Ζ¥”Π‘≠άμΈΣΘΚ![]() Ρ≥―–ΨΩ–ΓΉι‘Ύ Β―ι “”ΟΝρΜ·ΦνΖ®÷Τ±Η
Ρ≥―–ΨΩ–ΓΉι‘Ύ Β―ι “”ΟΝρΜ·ΦνΖ®÷Τ±Η![]() Θ§ Β―ιΉΑ÷Ο»γΆΦΥυ ΨΘΚ
Θ§ Β―ιΉΑ÷Ο»γΆΦΥυ ΨΘΚ

![]() ΉΑ÷ΟA÷–ΒΈΦ”≈®ΝρΥαΒΡ“«ΤςΟϊ≥Τ « ______ Θ§ Β―ι “ΜΙΩ…“‘”ΟAΉΑ÷Ο÷Τ»ΓΒΡΤχΧεΒΞ÷ ΒΡάκΉ”ΖΫ≥Χ Ϋ « ______ Θ°
ΉΑ÷ΟA÷–ΒΈΦ”≈®ΝρΥαΒΡ“«ΤςΟϊ≥Τ « ______ Θ§ Β―ι “ΜΙΩ…“‘”ΟAΉΑ÷Ο÷Τ»ΓΒΡΤχΧεΒΞ÷ ΒΡάκΉ”ΖΫ≥Χ Ϋ « ______ Θ°
![]() ΉΑ÷ΟDΒΡΉς”Ο «Φλ―ιΉΑ÷ΟC÷–
ΉΑ÷ΟDΒΡΉς”Ο «Φλ―ιΉΑ÷ΟC÷–![]() ΒΡΈϋ ’–߬ Θ§D÷–ΒΡ ‘ΦΝΩ…“‘ « ______
ΒΡΈϋ ’–߬ Θ§D÷–ΒΡ ‘ΦΝΩ…“‘ « ______ ![]() ±μΟς
±μΟς![]() Έϋ ’–߬ ΒΆΒΡ Β―ιœ÷œσ « ______ Θ°
Έϋ ’–߬ ΒΆΒΡ Β―ιœ÷œσ « ______ Θ°
![]() Β―ι÷ΤΒΟΒΡ
Β―ι÷ΤΒΟΒΡ![]() ≤ζΤΖ÷–Ω…ΡήΚ§”–
≤ζΤΖ÷–Ω…ΡήΚ§”–![]() ΓΔ
ΓΔ![]() Β»‘”÷ Θ°«κ…ηΦΤ Β―ιΘ§Φλ≤β
Β»‘”÷ Θ°«κ…ηΦΤ Β―ιΘ§Φλ≤β![]() ≤ζΤΖ÷– «Ζώ¥φ‘Ύ
≤ζΤΖ÷– «Ζώ¥φ‘Ύ![]() ‘”÷ Θ§Φρ“ΣΥΒΟς Β―ι≤ΌΉςΓΔœ÷œσΚΆΫα¬έΘΚ ______ Θ°
‘”÷ Θ§Φρ“ΣΥΒΟς Β―ι≤ΌΉςΓΔœ÷œσΚΆΫα¬έΘΚ ______ Θ°
![]() »ή“Κ «Ε®ΝΩ Β―ι÷–ΒΡ≥Θ”Ο ‘ΦΝΘ§ΈΣΝΥ≤βΕ®Ρ≥
»ή“Κ «Ε®ΝΩ Β―ι÷–ΒΡ≥Θ”Ο ‘ΦΝΘ§ΈΣΝΥ≤βΕ®Ρ≥![]() »ή“ΚΒΡ≈®Ε»Θ§―–ΨΩ–ΓΉιΒΡΆ§―ßΉΦ»ΖΝΩ»Γ
»ή“ΚΒΡ≈®Ε»Θ§―–ΨΩ–ΓΉιΒΡΆ§―ßΉΦ»ΖΝΩ»Γ![]() »ή“Κ”ΎΉΕ–ΈΤΩ÷–Θ§Φ”»κΙΐΝΩKIΙΧΧεΚΆ ΝΩΒΡœΓ
»ή“Κ”ΎΉΕ–ΈΤΩ÷–Θ§Φ”»κΙΐΝΩKIΙΧΧεΚΆ ΝΩΒΡœΓ![]() Θ§ΒΈΦ”÷Η ΨΦΝΘ§”Ο
Θ§ΒΈΦ”÷Η ΨΦΝΘ§”Ο![]() ±ξΉΦ»ή“ΚΒΈΕ®÷Ν÷’ΒψΘ§3¥ΈΤΫ–– Β―ι≤βΒΟΤΫΨυœϊΚΡ
±ξΉΦ»ή“ΚΒΈΕ®÷Ν÷’ΒψΘ§3¥ΈΤΫ–– Β―ι≤βΒΟΤΫΨυœϊΚΡ![]() »ή“ΚΒΡΧεΜΐΈΣ
»ή“ΚΒΡΧεΜΐΈΣ![]() Θ§‘ρ
Θ§‘ρ![]() ______
______ ![]() “―÷ΣΘΚ
“―÷ΣΘΚ![]() Θ§
Θ§![]()
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘Ύ “Έ¬œ¬Θ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «![]()
![]()
A.‘ΎΒΈ”–Ζ”ΧΣ»ή“ΚΒΡΑ±Υ°άοΘ§Φ”»κ![]() ÷Ν»ή“Κ«ΓΚΟΈό…ΪΘ§‘ρ¥Υ ±»ή“ΚΒΡ
÷Ν»ή“Κ«ΓΚΟΈό…ΪΘ§‘ρ¥Υ ±»ή“ΚΒΡ![]()
B.Ά§![]() ΒΡ»ή“ΚΘΚ
ΒΡ»ή“ΚΘΚ![]() »ή“ΚΘ§Έο÷ ΒΡΝΩ≈®Ε»Ήν¥σΒΡ «
»ή“ΚΘ§Έο÷ ΒΡΝΩ≈®Ε»Ήν¥σΒΡ «![]()
C.”–ΝΫ÷÷ΥαHAΚΆHBΘ§“―÷ΣHAΒΡΥα–‘±»HB»θΘ§‘ΎΈο÷ ΒΡΝΩ≈®Ε»ΨυΈΣ![]() ΒΡNaAΚΆNaBΜλΚœ»ή“Κ÷–Θ§”–
ΒΡNaAΚΆNaBΜλΚœ»ή“Κ÷–Θ§”–![]()
D.pHœύΆ§ΒΡ![]() »ή“ΚΓΔ
»ή“ΚΓΔ![]() »ή“ΚΓΔ
»ή“ΚΓΔ![]() »ή“ΚΓΔNaOH»ή“ΚΘ§Τδ≈®Ε»¥σ–ΓΙΊœΒΈΣΘΚ
»ή“ΚΓΔNaOH»ή“ΚΘ§Τδ≈®Ε»¥σ–ΓΙΊœΒΈΣΘΚ![]()
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΙΊœΒΆΦ÷–Θ§A «“Μ÷÷’ΐ―ΈΘ§B «ΤχΧ§«βΜ·ΈοΘ§C «ΒΞ÷ Θ§F ««ΩΥαΓΘΒ± X Έό¬έ ««ΩΥαΜΙ ««ΩΦν ±ΕΦ”–»γœ¬ΉΣΜ·ΙΊœΒΘ®ΤδΥϊΖ¥”Π≤ζΈοΦΑΖ¥”ΠΥυ–ηΧθΦΰΨυ“―¬‘»ΞΘ©Θ§Β± X ««ΩΦν ±Θ§ΙΐΝΩΒΡ B Ηζ Cl2 Ζ¥”Π≥ΐ…ζ≥… C ΆβΘ§Νμ“Μ≤ζΈο «―ΈΥα―ΈΓΘ
œ¬Ν–ΥΒΖ®÷–≤Μ’ΐ»ΖΒΡ «Θ® Θ©
![]()
A.Β± X ««ΩΥα ±Θ§AΓΔBΓΔCΓΔDΓΔEΓΔF÷–ΨυΚ§Ά§“Μ÷÷‘ΣΥΊΘ§F Ω…Ρή « H2SO4
B.Β± X ««ΩΦν ±Θ§AΓΔBΓΔCΓΔDΓΔEΓΔF÷–ΨυΚ§Ά§“Μ÷÷‘ΣΥΊΘ§F « HNO3
C.”Ο O2 ¥ζΧφ Cl2, “≤Ρή”κ B Ζ¥”Π…ζ≥… C Έο÷
D.Β± X ««ΩΥα ±Θ§C ‘Ύ≥ΘΈ¬œ¬ «“Μ÷÷“Ή»ή”ΎΨΤΨΪΒΡΙΧΧε
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ298K ±Θ§œρ ![]() Εΰ‘Σ»θΥα
Εΰ‘Σ»θΥα ![]() »ή“Κ÷–ΒΈΦ”
»ή“Κ÷–ΒΈΦ” ![]() »ή“ΚΘ§»ή“Κ÷–ΒΡ
»ή“ΚΘ§»ή“Κ÷–ΒΡ ![]() Θ§
Θ§![]() Θ§
Θ§ ![]() ΒΡΈο÷ ΒΡΝΩΖ÷ ΐ
ΒΡΈο÷ ΒΡΝΩΖ÷ ΐ![]()
![]() Υφ pHΒΡ±δΜ·»γΆΦΥυ ΨΓΘœ¬Ν–ΥΒΖ®¥μΈσΒΡ «
Υφ pHΒΡ±δΜ·»γΆΦΥυ ΨΓΘœ¬Ν–ΥΒΖ®¥μΈσΒΡ «![]()
![]()
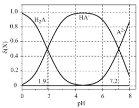
![]() “―÷Σ
“―÷Σ
A.Φ”»κ ![]() ±Θ§
±Θ§![]()
B.Β± ![]() Θ§
Θ§ ![]()
C.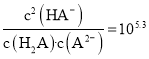
D.Β±ΜλΚœ»ή“Κ≥ ÷––‘ ±Θ§![]()
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΥ°νήΩσ÷–≥ΐSiO2ΆβΘ§ΜΙ”–9.24%CoOΓΔ2.78%Fe2O3ΓΔ0.96%MgOΓΔ0.084%CaOΓΘ¥”÷–Χα»ΓνήΒΡ÷ς“ΣΙΛ“’Νς≥Χ»γœ¬ΘΚ
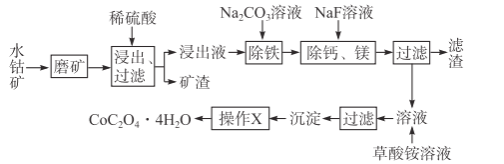
Θ®1Θ©Ϋΰ≥ωΙΐ≥Χ÷–Θ§CoO»ήΫβΒΡάκΉ”Ζ¥”ΠΖΫ≥Χ ΫΈΣ___Θ§Ωσ‘ϋΒΡ÷ς“Σ≥…Ζ÷ «___ΓΔ___ΓΘ
Θ®2Θ©«κ≈δΤΫœ¬Ν–≥ΐΧζΒΡΜ·―ßΖΫ≥Χ ΫΘΚ
_Fe2(SO4)3+_H2O+_Na2CO3=_Na2Fe6(SO4)4(OH)12Γΐ+_Na2SO4+_CO2Γϋ
Θ®3Θ©≥ΐΗΤΓΔΟΨΙΐ≥Χ÷–Θ§÷πΫΞΦ”»κNaF»ή“ΚΘ§Β±CaF2ΩΣ Φ≥ΝΒμ ±Θ§»ή“Κ÷–![]() =___ΓΘ[“―÷ΣKsp(CaF2)=1.0ΓΝ10-10ΓΔKsp(MgF2)=7.4ΓΝ10-11]ΓΘ
=___ΓΘ[“―÷ΣKsp(CaF2)=1.0ΓΝ10-10ΓΔKsp(MgF2)=7.4ΓΝ10-11]ΓΘ
Θ®4Θ©ΓΑ≤ΌΉςXΓ± «___ΓΘΫχ––ΗΟ≤ΌΉςΒΡ÷ς“ΣΡΩΒΡ «≥ΐ»Ξ≥ΝΒμ÷–ΒΡ‘”÷ άκΉ”Θ§Φλ―ι‘”÷ ÷–ΒΡ÷ς“Σ“θάκΉ” «Ζώ≥ΐΨΜΒΡ ‘ΦΝ «___ΓΘ
Θ®5Θ©100tΥ°νήΩσΉνΕύΩ…ΜώΒΟ___tCoC2O44H2O≤ζΤΖΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com