
【题目】如图所示是25℃时,N2与H2反应过程中能量变化的曲线图,下列叙述正确的是
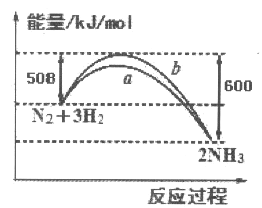
A. 该反应为放热反应
B. b曲线是表示加入了催化剂时的能量变化曲线
C. 加入催化剂,增加了反应的热效应
D. 反应开始通入1 mol N2和3 mol H2,反应后放出的热量一定为92kJ
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式是( )
A. 向水中通入氯气:Cl2+H2O2H++Cl﹣+ClO﹣
B. 二氧化锰与浓盐酸反应:MnO2+4HCl(浓)![]() Mn2++2Cl2↑+2H2O
Mn2++2Cl2↑+2H2O
C. 碳酸氢钠溶液加过量澄清石灰水:2HCO3﹣+Ca2++2OH﹣═CaCO3↓+2H2O+CO32﹣
D. 金属钠与硫酸铜溶液反应:2Na+2H2O+Cu2+═2Na++Cu(OH)2↓+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g) ![]() M(g)+N(g),所得实验数据如下表,下列说法不正确的是
M(g)+N(g),所得实验数据如下表,下列说法不正确的是
实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(X) | n(Y) | n(M) | ||
① | 700 | 0.10 | 0.10 | 0.09 |
② | 800 | 0.20 | 0.20 | 0.10 |
③ | 900 | 0.10 | 0.15 | a |
A. 正反应为放热反应
B. 实验①中,若5min时测得n(M)=0.05mol,则0~5min时间内,用N表示的平均反应速率v(N)= 0.01mol/(Lmin)
C. 实验②中,该反应的平衡常数K=1.0
D. 实验③中,达到平衡时,a大于0.06
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国际计量大会第26次会议新修订了阿伏加德罗常数(NA=6.02214076×1023mol-1),并于2019年5月20日正式生效。下列说法正确的是
A. 1L0.5mol·L-1Al2Fe(SO4)4溶液中阳离子数目小于1.5NA
B. 2 mol NH3和3molO2在催化剂和加热条件下充分反应生成NO的分子数为2NA
C. 56g聚乙烯分子中含碳碳双键的数目为2NA
D. 32.5g锌与一定量浓硫酸恰好完全反应,生成气体的分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ca3(PO4)2与SiO2、C高温共热可以反应得到CaSiO3、P4蒸气和CO。反应如下:Ca3(PO4)2+SiO2+C![]() CaSiO3+P4↑+CO↑。
CaSiO3+P4↑+CO↑。
(1)配平该反应方程式,并标出电子转移方向和数目_____。
(2)该反应中被还原的元素是___,氧化产物是______。
(3)每消耗24.0g碳时,有___个电子发生转移,生成P4__g。
(4)反应所得混合气体,折算成标况下,其气体密度为____g/L(保留两位小数)。
(5)与该反应中涉及到的磷元素相同主族的氮元素,是造成水体富营养化的主要原因。若某污水中NH4Cl含量为180 mg/L。
①写出NH4Cl的电子式____。
②为除去废水中的NH4+,向103L该污水中加入0.1 mol/LNaOH溶液,发生如下反应:NH4++OH-=NH3+H2O,则理论上需要NaOH溶液的体积为___L(计算结果保留两位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作、现象以及结论完全对应的是
实验操作 | 实验现象 | 结论 | |
A | 0.1 mol/L MgSO4溶液中滴加过量NaOH 溶液,再滴加 0.1 mol/L CuSO4溶液 | 先生成白色沉淀,后变为浅蓝色沉淀 | Cu(OH)2溶度积比Mg(OH)2小 |
B | 将水蒸气通过灼热的铁粉 | 铁粉变为红色 | 铁可以与水在高温下发生反应 |
C | 向酸性KMnO4溶液中滴加乙醇 | 溶液褪色 | 乙醇具有还原性 |
D | 向FeCl3和BaCl2混合溶液中通入足量SO2 | 溶液变为浅绿色且有白色沉淀生成 | Fe3+被还原为Fe2+,白色沉淀为BaSO3 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.1 molL1CH3COOH溶液中存在如下电离平衡:CH3COOH![]() CH3COO- + H+,对于该平衡,下列叙述正确的是
CH3COO- + H+,对于该平衡,下列叙述正确的是
A. 加热,平衡向逆反应方向移动
B. 加入少量0.05 molL﹣1 H2SO4溶液,溶液中c(H+)不变
C. 加入少量NaOH固体,平衡向正反应方向移动
D. 加入少量水,水的电离平衡不移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下12种物质为中学化学中常见的物质:
①Cu ②NaCl ③NaHSO4 ④SO3 ⑤H2SO4⑥C2H5OH ⑦CaCO3 ⑧BaSO4 ⑨Cu(OH)2⑩Fe(OH)3 ![]() NaOH
NaOH ![]() NH3·H2O
NH3·H2O
请回答下列问题(填序号)。
(1)属于电解质的是_____。
(2)属于非电解质的是_____。
(3)在水溶液中能导电的电解质是_____。
(4)属于弱电解质的是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知气态烃A在标准状况下的密度为1.25 g·L-1,C能够发生银镜反应, E与B、D均能发生酯化反应。有关物质的转化关系如下:

请回答:
(1) F的结构简式______。
(2) A→B的反应类型______。
(3) C→D的化学方程式______。
(4) 下列说法不正确的是______。
A.将金属钠投入B中,金属钠沉入底部,并缓慢的放出气泡
B.2 mol F可以反应产生1 mol环状化合物,其分子式为C4H6O5
C.G加入NaHCO3溶液中会产生气体
D.1 mol H可以与含2 mol NaOH的水溶液完全反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com