
【题目】向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,生成的沉淀质量与滴入NaOH溶液体积关系如右图,则原混合溶液中MgCl2与FeCl3的物质的量之比为( ) 
A.![]()
B.![]()
C.![]()
D.![]()
【答案】D
【解析】解:向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,首先发生反应NaOH+HCl=NaCl+H2O,即为图象中0﹣amL,沉淀的质量为0g;FeCl3只能在酸性较强的溶液中存在,当酸性减弱时,会转化为Fe(OH)3沉淀,从amL开始,bmL时沉淀完全.bmL时,溶液仍然呈酸性,到cmL时,才开始产生Mg(OH)2沉淀,
令氢氧化钠浓度为xmol/L,
Fe3+完全沉淀消耗氢氧化钠为(b﹣a)mL,结合Fe3++3OH﹣═Fe(OH)3↓可知,溶液中n(Fe3+)= ![]() ×(b﹣a)×10﹣3Lxmol/L,
×(b﹣a)×10﹣3Lxmol/L,
Mg2+完全沉淀消耗氢氧化钠为(d﹣c)mL,结合Mg2++2OH﹣═Mg(OH)2↓可知,溶液中n(Mg2+)= ![]() ×(d﹣c)×10﹣3Lxmol/L,
×(d﹣c)×10﹣3Lxmol/L,
故原混合溶液中n(MgCl2):n(FeCl3)= ![]() ×(d﹣c)×10﹣3Lxmol/L:
×(d﹣c)×10﹣3Lxmol/L: ![]() ×(b﹣a)×10﹣3Lxmol/L=
×(b﹣a)×10﹣3Lxmol/L= ![]() ,
,
故选D.
向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,首先发生反应NaOH+HCl=NaCl+H2O,即为图象中0﹣amL,沉淀的质量为0g;FeCl3只能在酸性较强的溶液中存在,当酸性减弱时,会转化为Fe(OH)3沉淀,从amL开始,bmL时沉淀完全.bmL时,溶液仍然呈酸性,到cmL时,才开始产生Mg(OH)2沉淀,结合Fe3++3OH﹣═Fe(OH)3↓、Mg2++2OH﹣═Mg(OH)2↓计算判断.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】Cu2O主要用于制造船底防污漆,它是一种鲜红色粉末,几乎不溶于水,在湿空气中逐渐氧化成黑色氧化铜。用含NaOH的Na2SO3溶液还原CuSO4制备Cu2O的工艺流程如下:

回答下列问题:
(1)流程中涉及的化学反应主要包括:
Ⅰ.Cu2++2OH-=Cu(OH)2↓;Ⅱ.生成CuOH;Ⅲ.2CuOH=Cu2O+H2O。
写出第Ⅱ步反应的离子方程式: ______________________________。
(2)其他反应条件相同时,测得反应时间和溶液的pH对Cu2O产率的影响如下图所示:
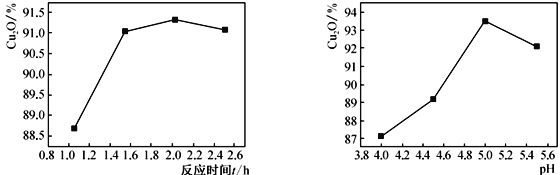
①反应时间超过2h时,Cu2O产率开始降低其原因是____________________________。
②pH<5时,Cu2O产率随pH减小而减小,产品中铜含量增加明显,其原因是______________________(用离子方程式说明)。
(3)为测定产品中Cu2O的含量,称取3.96 g产品于锥形瓶中,加入30mL硫酸酸化的Fe2(SO4)3溶液(足量),充分反应后用0.2000 mol·L-1标准KMnO4溶液滴定,至终点时消耗50mL标准液。
①滴定时应选用______(填“酸式”或“碱式”)滴定管,滴定终点的现象是______________________。
②产品与硫酸酸化的Fe2(SO4)3溶液反应的离子方程式为________________________________。
③假定杂质不参与反应,产品中Cu2O的质量分数为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人工肾脏可采用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如下图所示。下列说法不正确的是( )

A. B为电源的负极
B. 阳极室中发生的反应依次为:2Cl--2e-=Cl2↑,CO(NH2)2+3Cl2+H2O=N2+CO2+6HCl
C. 电解结束后,阴极室溶液的pH与电解前相比一定会减小
D. 若两极共收集到气体13.44 L(标准状况),则理论可去除尿素为7.2g(忽略气体的溶解)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同条件下,一定量的氢气在氧气中充分燃烧并放出热量。若生成液态水放出的热量为Q1 kJ;若生成气态水放出的热量为Q2 kJ,那么Q1与Q2的大小关系是
A.Q1>Q2 B.Q1<Q2 C.Q1=Q2 D.不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,充分燃烧一定量的丁烷放出热量Q kJ(Q>0),经测定完全吸收生成的CO2需消耗5 mol/L的KOH溶液100 mL,恰好生成正盐,则此条件下反应C4H10(g)+13/2O2(g)===4CO2(g)+5H2O(g)的ΔH为
A. +8Q kJ/mol B. +16Q kJ/mol
C. -8Q kJ/mol D. -16Q kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把6mol铜粉投入含8mol硝酸和2mol硫酸的稀溶液中,则标准状况下放出的气体的物质的量为( )
A.2 mol
B.3 mol
C.4 mol
D.5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在101kPa、25℃时,1.0g乙烷气体完全燃烧生成液态水时,放出热量52.0kJ,则乙烷燃烧的热化学方程式为( )
A.C2H6(g)+ ![]() O2(g)═2CO2(g)+3H2O(l)△H=﹣1560kJmol﹣1
O2(g)═2CO2(g)+3H2O(l)△H=﹣1560kJmol﹣1
B.2C2H6(g)+7O2(g)═4CO2(g)+6H2O(g)△H=﹣1560kJmol﹣1
C.C2H6(g)+ ![]() O2(g)═2CO2(g)+3H2O(l)△H=﹣52.0kJmol﹣1
O2(g)═2CO2(g)+3H2O(l)△H=﹣52.0kJmol﹣1
D.2C2H6(g)+7O2(g)═4CO2(g)+6H2O(l)△H=+3120 kJmol﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com