
【题目】制备氰氨基化钙的化学方程式为CaCO3+2HCN![]() CaCN2+CO↑+H2↑+CO2↑,下列说法正确的是
CaCN2+CO↑+H2↑+CO2↑,下列说法正确的是
A. 氢元素被氧化, 碳元素被还原
B. HCN被氧化, CaCO3被还原
C. HCN是氧化剂, CaCO3是还原剂
D. CaCN2是氧化产物, H2为还原产物
【答案】D
【解析】
CaCO3+2HCN=CaCN2+CO↑+H2↑+CO2↑中,N元素化合价不变,生成物CO2中碳元素来自碳酸钙,它的化合价没有发生变化,生成物CO中碳元素来自HCN,C的化合价没有发生变化,HCN中的H原子得电子由+1价变为0价(2个H原子),得到H2,HCN中的C原子失电子,由+2价变为+4价(1个C原子),得到CaCN2。
因HCN中的碳元素化合价升高,氢元素的化合价降低,则氢元素被还原,碳元素被氧化,A错误;因HCN中的碳元素化合价升高,氢元素的化合价降低,则HCN既是氧化剂又是还原剂,碳酸钙中没有元素的化合价发生变化,既不是氧化剂也不是还原剂,B、C错误;HCN中的碳元素化合价由+2升高到+4,对应的氧化产物为CaCN2,HCN中的氢元素化合价由+1价降低到0,对应的还原产物为H2,D正确。
故选D。


科目:高中化学 来源: 题型:
【题目】欲配制0.2mol/L 的NaOH溶液980mL,有以下仪器:
①烧杯②漏斗③托盘天平(带砝码)④玻璃棒⑤胶头滴管
(1)配制时,必须使用的仪器有____________(填代号),还缺少的玻璃仪器是____________________。该实验中两次用到玻璃棒,其作用分别是____________________,____________________。
(2)使用容量瓶前必须进行的一步操作是_____________________。
(3)根据计算应用托盘天平称量NaOH_______g。
(4)请你分析下列哪些操作会引起所配浓度偏大________(填写字母)。
A.将NaOH放在滤纸上称量
B.称取NaOH的砝码已生锈
C.容量瓶未干燥即用来配制溶液
D.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,并进行定容;
E.往容量瓶转移时,有少量液体溅出
F.在容量瓶中定容时视线如图所示
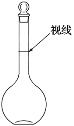
G.烧杯未进行洗涤
H.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线。
(5)若定容时不小心使液面超过了刻度线,应采取的措施是_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。

下列说法正确的是( )
A. 沸点 A2D<A2X
B. CA3 分子是非极性分子
C. B、C、D 形成的气态氢化物互为等电子体
D. C 形成的常见单质中 σ 键与 π 键个数之比为 1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】应用 VSEPR 理论判断下表中分子或离子的立体构型。
分子 | 中心原子上弧电子对数 | 中心原子结合的杂化类型 | 分子或离子的立体构型 |
NH2 | _______________ | _______________ | _______________ |
BF3 | _______________ | _______________ | _______________ |
H3O+ | _______________ | _______________ | _______________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)如何检验绿矾晶体中Fe2+是否被氧化?_______________________________
(2)已知本实验所用绿矾晶体没有被氧化。为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按下图连接好装置进行实验。

①将下列实验操作步骤正确排序__________(填标号);重复上述操作步骤,直至装置A恒重,记为m3g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量装置A的质量 f.冷却到室温
②根据实验记录,计算绿矾化学式中结晶水数目x=_____________(列式表示)。若实验时按a、d次序操作,则使x_____________(填“偏大”“偏小”或“无影响”)。
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热,实验后反应管中残留固体为红色粉末。
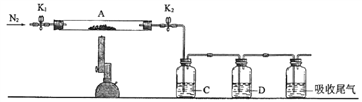
①C、D中的溶液依次为__________(填标号)。C、D中有气泡冒出,并可观察到的现象分别为_____________。
A.品红 B.NaOH C.BaCl2 D.Ba(NO3)2 E.浓H2SO4
②写出硫酸亚铁高温分解反应的化学方程式_______________。
(4)绿矾溶液在空气中久置出现红褐色沉淀,写出相关的离子方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中不正确的是
A. C60与石墨是同素异形体 B. H(氕)、D(氘)、T(氚)互为同位素
C. 甲烷和戊烷是同系物 D. 异丁烷与丁烷是同一种物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学按下图进行实验,在A中放的是干燥的红色纸条,B中放的是湿润的红色纸条,C中盛放的是氢氧化钠溶液。请回答下列问题。
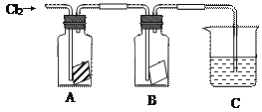
(1)通入Cl2一段时间后,A、B装置中,红色纸条的现象和结论为:
装置 | 现象 | 结论 |
A | ______________ | 潮湿的氯气______(填能或不能)使红色纸条褪色,因为反应生成的____________具有漂白性 |
B | ______________ |
(2)C装置的作用是__________________________
写出装置C中反应的化学方程式:_________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示对应化学反应的离子方程式正确的是 ( )
A. 向稀HNO3中滴加Na2SO3溶液: SO32-+2H+SO2↑+H2O
B. Na2CO3溶液中CO32-的水解:CO32-+H2O==HCO3-+OH-
C. 向Al2(SO4)3溶液中加入过量的NH3·H2O: Al3++4NH3·H2O[Al(OH)4]-+4N![]()
D. 向CuSO4溶液中加Na2O2:2Na2O2+2Cu2++2H2O4Na++2Cu(OH)2↓+O2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com