
【题目】某学习小组通过下列装置探究MnO2与FeCl3·6H2O能否反应产生Cl2,FeCl3的升华温度为315℃。
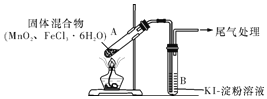
实验操作和现象:
操作 | 现象 |
点燃酒精灯,加热 | ⅰ.A中部分固体溶解,上方出现白雾 ⅱ.稍后,产生黄色气体,管壁附着黄色液滴 ⅲ.B中溶液变蓝 |
(1)现象ⅰ中的白雾是___。
(2)分析现象ⅱ,该小组探究黄色气体的成分,实验如下:
a.加热FeCl3·6H2O,产生白雾和黄色气体。
b.用KSCN溶液检验现象ⅱ和a中的黄色气体,溶液均变红。通过该实验说明现象ⅱ中黄色气体含有___。
(3)除了氯气可使B中溶液变蓝外,推测还可能的原因是:
①实验b检出的气体使之变蓝,反应的离子方程式是___。经实验证实推测成立。
②溶液变蓝的另外一种原因是:在酸性条件下,装置中的空气使之变蓝。通过进一步实验确认了这种可能性,其实验方案是___。
(4)为进一步确认黄色气体是否含有Cl2,小组提出两种方案,均证实了Cl2的存在。
方案1:在A、B间增加盛有某种试剂的洗气瓶C。
方案2:将B中KI淀粉溶液替换为NaBr溶液;检验Fe2+。
现象如下:
方案1 | B中溶液变为蓝色 |
方案2 | B中溶液呈浅橙红色,未检出Fe2+ |
①方案1的C中盛放的试剂是___(填字母)。
A.NaCl饱和溶液 B.NaOH溶液 C.NaClO溶液
②方案2中检验Fe2+的原因是___。
③综合方案1、2的现象,说明选择NaBr溶液的依据是___。
(5)将A中的产物分离得到Fe2O3和MnCl2,A中产生Cl2的化学方程式是:___。
【答案】盐酸小液滴 FeCl3 2Fe3++2I-=2Fe2++I2 另取一支试管,向其中加入KI淀粉溶液,再滴入几滴HCl溶液,在空气中放置,观察溶液是否变蓝 A 排除Fe3+将Br-氧化成Br2的可能性 该实验条件下,Br-可以被Cl2氧化成Br2,但不会被Fe3+氧化为Br2 3MnO2+4FeCl36H2O![]() 2Fe2O3+3MnCl2+3Cl2↑+24H2O
2Fe2O3+3MnCl2+3Cl2↑+24H2O
【解析】
(1)FeCl3![]() 6H2O受热失去结晶水,同时水解,生成HCI气体,HCl和H2O结合形成盐酸小液滴;
6H2O受热失去结晶水,同时水解,生成HCI气体,HCl和H2O结合形成盐酸小液滴;
(2)FeCl3溶液中滴入KSCN溶液,发生络合反应,用KSCN溶液检验现象ii和A中的黄色气体,溶液均变红,说明含有FeCl3;
(3)①氯化铁具有强氧化性,可以将碘离子氧化为碘单质;
②作对照实验,需要除去Cl2和Fe3+的干扰才能检验酸性情况下的O2影响,所以最好另取溶液对酸性情况下氧气的影响进行检验。因为原题中存在HC1气体,所以酸化最好选用盐酸;
(4)①方案1:除去Cl2中的FeCl3和O2(H+),若仍能观察到B中溶液仍变为蓝色则证明原气体中确实存在Cl2,Cl2中的氯化氢的去除使用饱和NaCl溶液,饱和NaCl溶液也可以让FeCl3溶解,并且除去O2影响过程中提供酸性的HCI气体,从而排除两个其他影响因素;
②方案2:若B中观察到浅橙红色,则证明有物质能够将Br-氧化成Br2,若未检查到Fe2+,则证明是Cl2氧化的Br-,而不是Fe3+另外,因为还原剂用的不是I-,可不用考虑O2(H+)的影响问题;
③方案2:将B中KI-淀粉溶液替换为NaBr溶液,结果B中溶液呈橙红色,且未检出Fe2+,Br-可以被Cl2氧化成Br2,但不会被Fe3+氧化为Br 2;
(5)二氧化锰与FeCl3![]() 6H2O反应生成Fe2O3、MnCl2、Cl2及水,据此结合原子守恒书写反应方程式。
6H2O反应生成Fe2O3、MnCl2、Cl2及水,据此结合原子守恒书写反应方程式。
(1) FeCl36H2O受热失去结晶水FeCl36H2O![]() FeCl3+6H2O,同时水解FeCl3+3H2O
FeCl3+6H2O,同时水解FeCl3+3H2O![]() Fe(OH)3+3HCl,生成HCl气体,HCl和H2O结合形成盐酸小液滴,而形成白雾,故答案为:HCl小液滴;
Fe(OH)3+3HCl,生成HCl气体,HCl和H2O结合形成盐酸小液滴,而形成白雾,故答案为:HCl小液滴;
(2) FeCl3溶液中滴入KSCN溶液,发生络合反应,Fe3++3SCN-= Fe(SCN)3,生成血红色的硫氰化铁,用KSCN溶液检验现象ii和A中的黄色气体,溶液均变红,说明含有FeCl3,故答案为:FeCl3;
(1) ①碘离子具有还原性,氯化铁具有强氧化性,两者反应,碘离子被氧化为碘单质,反应离子方程式为:2Fe3++2I-=2Fe2++I2,故答案为:2Fe3++2I-=2Fe2++I2;
②FeCl36H2O受热水解,生成HCl气体,作对照实验,需用盐酸酸化,另取一支试管,向其中加入KI-淀粉溶液,再滴入几滴HCl溶液,在空气中放置,观察一段时间后溶液是否变蓝,若一段时间后溶液变蓝则推测成立,故答案为:另取一支试管,向其中加入KI淀粉溶液,再滴入几滴HCl溶液,在空气中放置,观察溶液是否变蓝,进行推测;
(4) ①方案1:氯化铁能氧化碘离子,氧气在酸性条件下,能氧化碘离子,所以需除去Cl2中的FeCl3和O2(H+),若仍能观察到B中溶液仍变为蓝色,则证明原气体中确实存在Cl2,使用饱和NaCl溶液,可以让FeCl3溶解,并且除去O2影响过程中提供酸性的HCl气体,从而排除两个其他影响因素,故答案为:A;
![]() 方案2:若B中观察到浅橙红色,为溴水的颜色,则证明有物质能够将Br-氧化成Br2,铁离子不能氧化溴离子,若未检查到Fe2+,则证明是Cl2氧化的Br-,而不是Fe3+另外,因为还原剂用的不是I-,可不用考虑O2(H+)的影响问题,故答案为:排除Fe3+将Br-氧化成Br2的可能性;
方案2:若B中观察到浅橙红色,为溴水的颜色,则证明有物质能够将Br-氧化成Br2,铁离子不能氧化溴离子,若未检查到Fe2+,则证明是Cl2氧化的Br-,而不是Fe3+另外,因为还原剂用的不是I-,可不用考虑O2(H+)的影响问题,故答案为:排除Fe3+将Br-氧化成Br2的可能性;
![]() 选择NBr溶液的依据是Br-可以被Cl2氧化成Br2,但不会被
选择NBr溶液的依据是Br-可以被Cl2氧化成Br2,但不会被![]() 氧化为Br2,故答案为:该实验条件下,Br-可以被Cl2氧化成Br2,但不会被Fe3+氧化为Br2 ;
氧化为Br2,故答案为:该实验条件下,Br-可以被Cl2氧化成Br2,但不会被Fe3+氧化为Br2 ;
(5)二氧化锰与FeCl36H2O反应生成Fe2O3、MnCl2、Cl2及水,反应方程式为:3MnO2+4FeCl36H2O![]() 2Fe2O3+3MnCl2+3Cl2↑+24H2O,故答案为:3MnO2+4FeCl36H2O
2Fe2O3+3MnCl2+3Cl2↑+24H2O,故答案为:3MnO2+4FeCl36H2O![]() 2Fe2O3+3MnCl2+3Cl2↑+24H2O。
2Fe2O3+3MnCl2+3Cl2↑+24H2O。


科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是
A. 糖类、油脂、蛋白质在一定条件下均能水解
B. 乙二醇、苯乙烯在一定条件下均可聚合生成高分子化合物
C. 分子式为C4H8C12的有机物共有(不含立体异构)8种
D. ![]() 处于同一平面上的原子数最多为18个
处于同一平面上的原子数最多为18个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2+ +2OH- ![]() CH3COONH4 +3NH3+2Ag↓+H2O
CH3COONH4 +3NH3+2Ag↓+H2O
B. 苯酚钠溶液中通入少量CO2:CO2 +H2O+2C6H5O-→2C6H5OH+CO32-
C. 乙酸滴入氢氧化铜悬浊液中:2CH3COOH+Cu(OH)2=Cu2++2CH3COO-+2H2O
D. 氯乙烷中滴入AgNO3溶液检验其中氯元素:Cl-+Ag+=AgCl↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某离子反应中涉及![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 六种微粒.其中
六种微粒.其中![]() 的物质的量随时间变化的曲线如图所示.则下列判断正确的是( )
的物质的量随时间变化的曲线如图所示.则下列判断正确的是( )
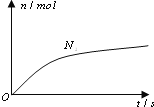
A.反应后溶液的酸性明显增强
B.消耗1mol还原剂,转移6mol电子
C.氧化剂与还原剂的物质的量之比为2:3
D.该反应的还原剂是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下:
元素 | 相关信息 |
A | 基态原子的价电子排布式为nSnnPn |
B | 元素原子的核外p电子数比s电子数少1个 |
C | 最外层电子数是电子层数的3倍 |
D | 简单离子是第三周期元素中离子半径最小的 |
E | 价电子层中的未成对电子数为4 |
请回答下列问题:
(1)写出下列元素的名称:A______, B_______, C________,D__________
(2)写出C元素在周期表的位置_________,E2+价电子的轨道表示式________________,B元素能量最高的电子为_____轨道上的电子,其轨道呈_______形.
(3)按原子轨道的重叠方式,1molA与C形成的最高价化合物中σ键有______个,π键有______个。
(4)B、C、D的简单离子的半径由大到小的顺序为_____________(用离子符号表示)。
(5)写出C的核外有18个电子的氢化物的电子式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.增大压强或升高温度,—定能使化学反应速率加快
B.合成氨工业中,将氨气液化分离来可以提高正反应速率和产率
C.500°C、30 MPa下,0.5 mol N2(g)和1.5mol H2(g)反应生成NH3(g) 放热QkJ,其热化学方程式为N2(g)+3 H2(g) ![]() 2 NH3(g) △H=-2QkJ/mol
2 NH3(g) △H=-2QkJ/mol
D.己知两个平衡体系:2NiO(s) ![]() 2Ni(s)+O2(g) 2CO(g)+O2(g)
2Ni(s)+O2(g) 2CO(g)+O2(g) ![]() 2CO2(g)是平衡常数分别为K1和K2,可推知平衡NiO(s)+CO(g)
2CO2(g)是平衡常数分别为K1和K2,可推知平衡NiO(s)+CO(g) ![]() Ni(s)+CO2(g)的平衡常数为
Ni(s)+CO2(g)的平衡常数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.反应TiO2(s) + 2Cl2(g)=TiCl4(g) + O2(g) ΔH>0能自发进行,其原因是ΔS>0
B.室温下,pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合,溶液pH>7
C.CH3COOH溶液加水稀释后,溶液中![]() 的值减小
的值减小
D.对于乙酸与乙醇的酯化反应(ΔH<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氢大麻酚(简称THC),是大麻中的主要精神活性物质,其结构如图。下列有关THC的说法不正确的是

A. THC难溶于水
B. 1mol THC最多可与含3mol溴单质的溴水发生反应
C. THC遇FeCl3溶液能发生显色反应
D. THC能与氢氧化钠溶液、碳酸钠溶液及碳酸氢钠溶液发生化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组学习了反应CO2+2Mg![]() 2MgO+C的相关知识后,欲探究镁是否与SO2气体反应,设计了下列实验装置图(注:石棉绒是一种耐火材料,不参与反应)。
2MgO+C的相关知识后,欲探究镁是否与SO2气体反应,设计了下列实验装置图(注:石棉绒是一种耐火材料,不参与反应)。

请回答下列问题:
(1)若可供选择固体试剂有:木炭、铜片、亚硫酸钠固体,则装置A中发生反应的化学方程式为____________________________________________。
(2)装置B中所盛入的药品是______________________。
(3)仪器a的名称是___________,其作用是______________________。
(4)实验完毕后观察到石棉绒上有黄色物质生成,将石棉绒及其附着物投入到稀盐酸中,会产生具有臭鸡蛋气味的气体,则镁与SO2除发生SO2+2Mg![]() 2MgO+S反应外,还发生的反应是____________。
2MgO+S反应外,还发生的反应是____________。
(5)在装置C、D间插入图所示装置,可以获得亚硫酸(H2SO3)溶液。
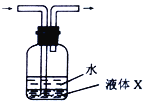
①液体X可以是下列试剂中的___________(填序号)。
A.苯 B.汽油 C.四氯化碳 D.酒精
②实验完毕后,通过___________(实验操作名称)可以将上、下两层液体分开。
③向亚硫酸溶液中通入空气,溶液的pH_______(填“增大”、“减小”或“不变”),其原因是______(用化学方程式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com