
【题目】恒温恒压下1 mol A和n mol B在一个容积可变的容器中发生如下反应:
A(g)![]() 2B(g) + 2C(g),一段时间后达到平衡,生成a mol C。则下列说法中正确的是
2B(g) + 2C(g),一段时间后达到平衡,生成a mol C。则下列说法中正确的是
A.物质A、B的转化率之比一定是1∶2
B.若起始时放入3 mol A+3n mol B,则达平衡时生成3a mol C
C.起始时刻和达平衡后容器中的压强比为 (1+n)/(1+n-a/2)
D.当v正(A) =2v逆(C)时,可断定反应达平衡
【答案】B
【解析】
A.B与C的系数之比为1:1,一段时间后达到平衡,生成a molC,A的转化率为![]() ,转化的B有amol,则B的转化率为
,转化的B有amol,则B的转化率为![]() ,无法确定转化率之比,选项A错误;
,无法确定转化率之比,选项A错误;
B.若起始时放入3 mol A+3n mol B,相当于3个题设平衡(初始投入1molA和nmolB的状态)在恒温恒压下叠加,气体体积加倍,故达平衡没有移动,各组分的量加倍,所以达到平衡时C的物质的量为3a mol,选项B正确;
C.反应在恒压条件下进行,反应前后压强不变,起始时刻和达平衡后容器中的压强比为1;1,选项C错误;
D.当2 v正(A) = v逆(C)时,正逆反应速率相等,反应达到平衡状态,选项D错误;
答案选B。


科目:高中化学 来源: 题型:
【题目】下列离子方程式中正确的是( )
A.氢氧化亚铁溶于稀硝酸中:Fe(OH)2 + 2H+ = Fe2+ + 2H2O
B.用惰性电极电解饱和食盐水:2Cl- + 2H2O![]() 2OH- + H2↑+ Cl2↑
2OH- + H2↑+ Cl2↑
C.湿润的醋酸铅试纸检验H2S气体的存在:Pb2+ + H2S = PbS + 2H+
D.在苯酚钠溶液中通入过量的CO2气体:2C6H5O- + CO2 + H2O → 2C6H5OH↓+ CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列各说法中,正确的是
A. 对于2SO2(g)+O2(g) ![]() 2SO3(g) ΔH=-Q kJ·mol-1,(Q>0),若反应中充入1mol SO2和足量的氧气反应时,放出的热量一定是Q/2 kJ
2SO3(g) ΔH=-Q kJ·mol-1,(Q>0),若反应中充入1mol SO2和足量的氧气反应时,放出的热量一定是Q/2 kJ
B. 热化学方程式中的化学计量数不能用分数表示
C. Zn(s)+H2SO4(aq) ===ZnSO4(aq)+H2(g) ΔH<0,该反应的化学能可以转化为电能
D. ΔH的大小与热化学方程式的化学计量数无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到沉淀的物质的量与加入NaOH溶液体积的关系如图所示,则溶液中MgCl2与Al2(SO4)3的物质的量浓度之比为( )
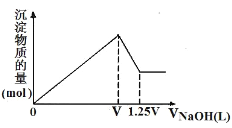
A.1:1B.1:2
C.3:2D.2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A.氢镍碱性电池原理为H2+2NiO(OH)=2Ni(OH)2,则该电池负极反应式为:H2—2e—+2OH—=2H2O
B.在测定中和热的实验中,盐酸物质的量一般要大于氢氧化钠物质的量,这样才能保证氢氧化钠中和完全
C.已知2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol,则氢气的燃烧热为241.8kJ/mol
D.已知S(s)+O2(g)=SO2(g);△H1 S(g)+O2(g)=SO2(g);△H2,则△H1<△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据最近的美国《农业研究》杂志报道,美国的科学家发现半胱氨酸能增强艾滋病毒感染者的免疫力,对控制艾滋病毒的蔓延有奇效。已知半胱氨酸的结构简式如图所示,则下列说法错误的是( )
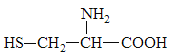
A.半胱氢酸是一种两性物质
B.两分子半胱氨酸,分子间脱去1个水分子形成的有机物结构简式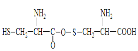
C.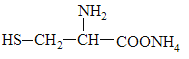 可与NaOH溶液反应放出一种碱性气体
可与NaOH溶液反应放出一种碱性气体
D.半胱氨酸属于α-氨基酸,可由某些蛋白质水解制取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应X(g)+3Y(g)![]() 2Z(g) ΔH=-a kJ·mol -1 ,一定条件下,1molX和3 mol Y在2L恒容密闭容器中发生反应,10min时测得Y 的物质的量为2.4 mol。下列说法正确的是
2Z(g) ΔH=-a kJ·mol -1 ,一定条件下,1molX和3 mol Y在2L恒容密闭容器中发生反应,10min时测得Y 的物质的量为2.4 mol。下列说法正确的是
A.10min时,容器内的压强是反应前的0.9倍
B.10min 时,X 的转化率为80%
C.10min内,用Y表示的平均反应速率为0.03 mol·L-1·s-1
D.前5分钟内,X 和Y 反应放出的热量等于0.1a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO2(亚氯酸纳)是常用的消毒剂和漂白剂,工业上可采用电解法制备,工作原理如图所示。下列叙述正确的是
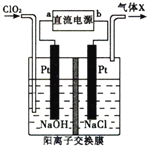
A. 若直流电源为铅蓄电池,则b极为Pb
B. 阳极反应式为ClO2+e-=ClO2-
C. 交换膜左测NaOH的物质的量不变,气体X为Cl2
D. 制备18.1gNaClO2时理论上有0.2molNa+由交换膜左侧向右侧迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组以粗盐和碳酸氢铵(![]() )为原料,采用如图所示流程制备纯碱和氯化铵。已知盐的热分解温度分别为
)为原料,采用如图所示流程制备纯碱和氯化铵。已知盐的热分解温度分别为![]() ;
;![]() ;
;![]() ;
;![]() 。
。
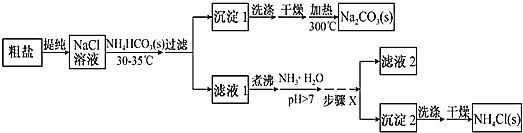
(1)粗盐中主要含有![]() 、
、![]() 、
、![]() 等杂质离子,粗盐提纯时使用的试剂有;①
等杂质离子,粗盐提纯时使用的试剂有;①![]() ;②
;②![]() ;③
;③![]() ;④
;④![]() ,其加入的顺序合理的是__________(填序号)。过滤中用到玻璃棒的作用是________。
,其加入的顺序合理的是__________(填序号)。过滤中用到玻璃棒的作用是________。
A.①③④② B.①②④③ C.③②④① D.①②③④
(2)如何运用简单的方法判断粗盐中![]() 是否已除尽?__________。
是否已除尽?__________。
(3)从![]() 溶液到沉淀1的过程中,需蒸发浓缩。在加入固体
溶液到沉淀1的过程中,需蒸发浓缩。在加入固体![]() 之前进行蒸发浓缩优于在加入
之前进行蒸发浓缩优于在加入![]() 之后,原因是___________。
之后,原因是___________。
(4)写出沉淀1受热分解的化学方程式:_________。
(5)为提高![]() 产品的产率,需在滤液中加入氨水,理由是_______;步骤X包括的操作有______。
产品的产率,需在滤液中加入氨水,理由是_______;步骤X包括的操作有______。
(6)某同学拟通过实验来测定该纯碱的纯度(假设杂质只含有![]() ),他称取w g该样品,将其完全溶解在盛有适量水的烧杯中,然后向烧杯中加入过量的
),他称取w g该样品,将其完全溶解在盛有适量水的烧杯中,然后向烧杯中加入过量的![]() 溶液,经过滤、洗涤、干燥,称得沉淀的质量为m g,试计算该样品中
溶液,经过滤、洗涤、干燥,称得沉淀的质量为m g,试计算该样品中![]() 的质量分数为____________。(用相关字母表示)
的质量分数为____________。(用相关字母表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com