
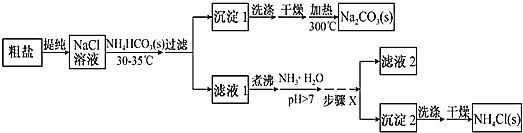
【题目】某研究小组以粗盐和碳酸氢铵(![]() )为原料,采用如图所示流程制备纯碱和氯化铵。已知盐的热分解温度分别为
)为原料,采用如图所示流程制备纯碱和氯化铵。已知盐的热分解温度分别为![]() ;
;![]() ;
;![]() ;
;![]() 。
。
(1)粗盐中主要含有![]() 、
、![]() 、
、![]() 等杂质离子,粗盐提纯时使用的试剂有;①
等杂质离子,粗盐提纯时使用的试剂有;①![]() ;②
;②![]() ;③
;③![]() ;④
;④![]() ,其加入的顺序合理的是__________(填序号)。过滤中用到玻璃棒的作用是________。
,其加入的顺序合理的是__________(填序号)。过滤中用到玻璃棒的作用是________。
A.①③④② B.①②④③ C.③②④① D.①②③④
(2)如何运用简单的方法判断粗盐中![]() 是否已除尽?__________。
是否已除尽?__________。
(3)从![]() 溶液到沉淀1的过程中,需蒸发浓缩。在加入固体
溶液到沉淀1的过程中,需蒸发浓缩。在加入固体![]() 之前进行蒸发浓缩优于在加入
之前进行蒸发浓缩优于在加入![]() 之后,原因是___________。
之后,原因是___________。
(4)写出沉淀1受热分解的化学方程式:_________。
(5)为提高![]() 产品的产率,需在滤液中加入氨水,理由是_______;步骤X包括的操作有______。
产品的产率,需在滤液中加入氨水,理由是_______;步骤X包括的操作有______。
(6)某同学拟通过实验来测定该纯碱的纯度(假设杂质只含有![]() ),他称取w g该样品,将其完全溶解在盛有适量水的烧杯中,然后向烧杯中加入过量的
),他称取w g该样品,将其完全溶解在盛有适量水的烧杯中,然后向烧杯中加入过量的![]() 溶液,经过滤、洗涤、干燥,称得沉淀的质量为m g,试计算该样品中
溶液,经过滤、洗涤、干燥,称得沉淀的质量为m g,试计算该样品中![]() 的质量分数为____________。(用相关字母表示)
的质量分数为____________。(用相关字母表示)
【答案】B 引流 取少量溶液,滴加![]() 溶液,观察是否有白色沉淀产生
溶液,观察是否有白色沉淀产生 ![]() 的分解温度较低,防止
的分解温度较低,防止![]() 在蒸发浓缩的过程中分解
在蒸发浓缩的过程中分解 ![]() 抑制
抑制![]() 的水解 蒸发浓缩、冷却结晶、过滤
的水解 蒸发浓缩、冷却结晶、过滤 ![]()
【解析】
从流程图中可以看出,粗盐首先提纯为![]() 溶液,向
溶液,向![]() 溶液中加入
溶液中加入![]() 固体并且控制温度不达到
固体并且控制温度不达到![]() 的分解温度,这一步与侯氏制碱法有异曲同工之妙,都是利用溶解度差异使溶解度较低的
的分解温度,这一步与侯氏制碱法有异曲同工之妙,都是利用溶解度差异使溶解度较低的![]() 析出,使复分解反应得以发生,因此沉淀1为
析出,使复分解反应得以发生,因此沉淀1为![]() ,再经过洗涤、干燥、加热分解后即得纯碱,再来看滤液1,滤液1即
,再经过洗涤、干燥、加热分解后即得纯碱,再来看滤液1,滤液1即![]() 溶液,因
溶液,因![]() 会水解,所以向其中加入氨水能抑制其水解,提高产率,再经蒸发浓缩、冷却结晶、过滤即可得到纯的
会水解,所以向其中加入氨水能抑制其水解,提高产率,再经蒸发浓缩、冷却结晶、过滤即可得到纯的![]() 固体,据此来分析各小题即可。
固体,据此来分析各小题即可。
(1)在粗盐提纯时,为了确保杂质除净,各除杂剂要稍微过量,后加入的试剂要能除去先加入的试剂,因此碳酸钠要在氯化钡之后加,盐酸要在碳酸钠和氢氧化钠之后加,过量的盐酸则可通过加热除去,因此答案选B,在过滤时玻璃棒的作用是引流;
(2)相当于在问我们如何检验溶液中是否含有![]() ,因此只需取少量溶液,滴加
,因此只需取少量溶液,滴加![]() 溶液,观察是否产生白色沉淀即可;
溶液,观察是否产生白色沉淀即可;
(3)![]() 的分解温度较低,因此在加入
的分解温度较低,因此在加入![]() 之前蒸发是为了防止
之前蒸发是为了防止![]() 受热分解;
受热分解;
(4)沉淀1即![]() ,
,![]() 受热分解的方程式为
受热分解的方程式为![]() ;
;
(5)![]() 会水解,因此加入氨水可以抑制其水解,提高
会水解,因此加入氨水可以抑制其水解,提高![]() 的产率,步骤X包括的操作有蒸发浓缩、冷却结晶和过滤;
的产率,步骤X包括的操作有蒸发浓缩、冷却结晶和过滤;
(6)m克沉淀即![]() ,代入其分子量可得碳酸钡的物质的量为
,代入其分子量可得碳酸钡的物质的量为![]() ,根据碳元素守恒,因此碳酸钠的物质的量也为
,根据碳元素守恒,因此碳酸钠的物质的量也为![]() ,代入其分子量可得碳酸钠的质量为
,代入其分子量可得碳酸钠的质量为![]() ,因此碳酸钠的质量分数为
,因此碳酸钠的质量分数为![]() ,本题得解。
,本题得解。


科目:高中化学 来源: 题型:
【题目】恒温恒压下1 mol A和n mol B在一个容积可变的容器中发生如下反应:
A(g)![]() 2B(g) + 2C(g),一段时间后达到平衡,生成a mol C。则下列说法中正确的是
2B(g) + 2C(g),一段时间后达到平衡,生成a mol C。则下列说法中正确的是
A.物质A、B的转化率之比一定是1∶2
B.若起始时放入3 mol A+3n mol B,则达平衡时生成3a mol C
C.起始时刻和达平衡后容器中的压强比为 (1+n)/(1+n-a/2)
D.当v正(A) =2v逆(C)时,可断定反应达平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物在工业生产上有许多用途。某工厂以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备不溶于水的碱式碳酸铜的流程如下:
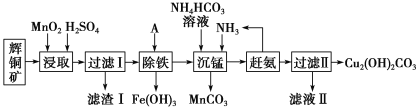
已知:①常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
金属离子 | Fe2+ | Fe3+ | Cu2+ | Mn2+ |
开始沉淀 | 7.5 | 2.7 | 5.6 | 8.3 |
完全沉淀 | 9.0 | 3.7 | 6.7 | 9.8 |
②Ksp[Fe(OH)3]=4.0×10-38
(1)滤渣I中的主要成分除了MnO2,S还有___________ (化学式),请写出“浸取”反应中生成S的化学方程式:_____。
(2)常温下“除铁”时加入的试剂A可用CuO等,调节pH调的范围为____,若加A后溶液的pH调为5,则溶液中Fe3+的浓度为____mol/L。
(3)写出“沉锰”(除Mn2+)过程中反应的离子方程式:_____。
(4)滤液Ⅱ经蒸发结晶得到的盐主要是____(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对实验方案的设计或评价合理的是( )
A. 经酸洗除锈的铁钉,用饱和食盐水浸泡后放入如图所示具支试管中,一段时间后导管口有气泡冒出
经酸洗除锈的铁钉,用饱和食盐水浸泡后放入如图所示具支试管中,一段时间后导管口有气泡冒出
B.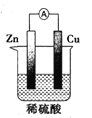 图中电流表会显示电流在较短时间内就会衰减
图中电流表会显示电流在较短时间内就会衰减
C.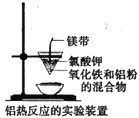 图中应先用燃着的小木条点燃镁带,然后插入混合物中引发反应
图中应先用燃着的小木条点燃镁带,然后插入混合物中引发反应
D. 可用图显示的方法除去酸式滴定管尖嘴中的气泡
可用图显示的方法除去酸式滴定管尖嘴中的气泡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种甲醇、氧气和强碱溶液做电解质的新型手机电池,可连续使用一个月,其电池反应为:2CH3OH+3O2+4OH﹣![]() 2CO32﹣+6H2O,则有关说法正确的是 ( )
2CO32﹣+6H2O,则有关说法正确的是 ( )
A.放电时CH3OH参与反应的电极为正极
B.放电时负极的电极反应为CH3OH+8OH﹣﹣6e﹣=CO32﹣+6H2O
C.标准状况下,通入5.6LO2并完全反应后,有0.5mol电子转移
D.放电一段时间后,通入氧气的电极附近溶液的pH降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学利用生活中或实验室中常用的物品,根据氧化还原反应知识和电化学知识,自己动手设计了一个原电池。请填写下列空白:
(1)实验原理:Fe+2H+=Fe2++H2↑
(2)实验用品:电极(______、______)、稀硫酸、______、________、耳机(或者电流表)(填写所缺的实验用品)。
(3)实验装置如图。
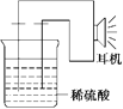
(4)原电池设计及注意的问题:
①按如图所示装置连接好实验仪器,注意观察(耳朵听)耳机是否有声音发出,如果没有,可将原电池的两个电极中的一极接触耳机插头上的一极(注意:接触的同时耳机的另一个极是连接在原电池的另一个电极上的),这时可以听见耳机发生“嚓嚓嚓……”的声音。其原因是在原电池中,由化学能转化为____________,在耳机中又由__________转化为声音这种能量;
②如果将装置中的耳机改为电流表,则铁钉应该接电流表的________极,电极反应式为_____________,发生了________反应;
③铜钉应该接电流表的________极,电极反应式为_____________,发生了_________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向一个一定容积的密闭容器中放入3 mol X和2 mol Y,发生反应:X(g)+Y(g)![]() 2Z(g)+R(g),达平衡时X的转化率为φ1。维持温度不变,若把6 mol X和3 mol Y放入该容器中,达平衡时X的转化率为φ2,则φ1与φ2的关系是( )
2Z(g)+R(g),达平衡时X的转化率为φ1。维持温度不变,若把6 mol X和3 mol Y放入该容器中,达平衡时X的转化率为φ2,则φ1与φ2的关系是( )
A.φ1>φ2B.φ1<φ2C.φ1=φ2D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子组成。取Wg该种氨基酸放在纯氧中充分燃烧,生成二氧化碳、水和氮气。按下图所示装置进行实验。

回答下列问题:
(1)实验开始时,首先通入一段时间的氧气,其理由是__________________。
(2)以上装置中需要加热的仪器有_______ (填写字母),操作时应先点燃_____处的酒精灯。
(3)A装置中发生反应的化学方程式是____________________________。
(4)D装置的作用是____________________________。
(5)读取氮气的体积时,应注意①_________________;②_________________。
(6)实验中测得氮气的体积为VmL(标准状况),为确定此氨基酸的分子式,还需要的有关数据有____________________。
A.生成二氧化碳气体的质量
B.生成水的质量
C.通人氧气的体积
D.氨基酸的相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是①CH3OH(g)+H2O(g) = CO2(g)+3H2(g) △H = + 49. 0 kJ·mol-1②CH3OH(g)+ ![]() O2(g) = CO2(g)+2H2(g) △H =-192. 9 kJ·mol-1,下列说法正确的是
O2(g) = CO2(g)+2H2(g) △H =-192. 9 kJ·mol-1,下列说法正确的是
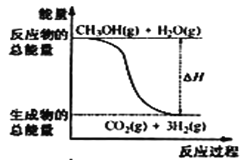
A.CH3OH的燃烧热为192. 9 kJ·mol-1
B.反应①中的能量变化如图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应:CH3OH(l) +![]() O2(g) = CO2(g) +2H2(g) △H >-192. 9kJ·mol-1
O2(g) = CO2(g) +2H2(g) △H >-192. 9kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com