
纳米钴(Co)是加氢反应的催化剂,500K时催化反应:CO(g)+3H2(g) CH4(g)+H2O(g) △H<0。有关说法正确的是
CH4(g)+H2O(g) △H<0。有关说法正确的是
A.纳米技术的应用,提高了催化剂的催化性能,但平衡常数不变
B.缩小容器体积,平衡向正反应方向移动CO的浓度减小
C.温度越低,越有利于CO催化加氢
D.从平衡体系中分H2O(g)能加快正反应速率
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源:2014-2015河北邢台一中高一3月月考化学试卷(解析版) 题型:选择题
室温时,将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中。然后向小烧杯中加入盐酸溶液,反应剧烈,大烧杯中的醋酸逐渐凝固(乙酸的熔点:16.6℃),下列说法正确的是
A.NH4HCO3和盐酸的反应是放热反应
B.该反应中,热能转化为化学能
C.反应物的总能量高于生成物的总能量
D.反应的热化学方程式为:NH4HCO3+HCl=NH4Cl+CO2↑+H2O ΔH>0
查看答案和解析>>
科目:高中化学 来源:2014-2015河北唐山市高一下学期开学调研考试化学试卷(解析版) 题型:选择题
“钴酞菁(分子直径1.3×10–9m)”分子结构和性质与人体内的血红素及植物体内的叶绿素非常相似,我国科学家在世界上第一次为“钴酞菁”分子恢复了磁性。下列关于“钴酞菁”的说法正确的是
A.在水中形成的分散系属于悬浊液
B.在水中形成的分散系属于胶体
C.分子直径比Na+小
D.“钴酞菁”分子既能透过滤纸,也能透过半透膜
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省唐山市高二下学期开学调研化学试卷(解析版) 题型:选择题
下列有关热化学方程式的叙述中,正确的是
A.含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,该反应的热化学方程式是 NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=+57.4 kJ·mol-1
B.已知C(石墨,s)=C(金刚石,s) △H>0,则金刚石一定比石墨稳定
C.已知2H2O(g)=2H2(g)+O2(g) △H=+483.6 kJ·mol-1,则提供483.6 kJ热量时,一定会使2 mol H2O (g)发生分解
D.已知C(s)+O2(g)=CO2(g) △H=a kJ·mol-1,2C(s)+O2(g)=2CO(g),△H=b kJ·mol-1,则2CO(g)+O2(g)=2CO2(g) △H=(2a﹣b) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省唐山市高二下学期开学调研化学试卷(解析版) 题型:选择题
常温下a mol·L-1稀氨水和b mol·L-1稀盐酸等体积混合,对混合后溶液判断一定正确的是
A.若a=b,则c(NH4+)=c(Cl-) B.若a>b,则c(NH4+)>c(Cl-)
C.若a>b,则c(OH-)>c(H+) D.若a<b,则c(OH-)<c(H+)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市高三联考一化学试卷(解析版) 题型:实验题
(18分)化学实验装置的科学设计是实验是否取得预期效果的关键。请回答下列有关实验装置的相关问题:
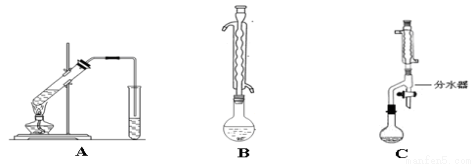
Ⅰ.下图A为“人教版”教材制备乙酸乙酯的实验装置,某同学甲认为下图B装置进行酯化反应效果比A要好,他的理由是_________________________;
某同学乙经查阅资料认为下图C装置进行酯化反应效果更好,他的理由是 ________________________。
Ⅱ.某实验小组欲探究碳与浓硝酸反应的情况。甲同学设计了图1装置,认为若有红棕色气体产生就说明碳与浓硝酸发生了反应。
(1)碳与浓硝酸反应的方程式_______________________。甲同学的实验应该在___________中进行,才符合化学实验安全性的要求。
(2)乙同学认为红棕色气体不一定是碳与浓硝酸发生反应而得,所以他认为甲同学观点是错误的,他的理由是________________(用化学方程式表示),所以他认为应该检验_____________(填化学式)的产生来证明碳与浓硝酸反应。为此乙同学查阅相关资料得知“0℃时四氧化二氮为液体”,从而改进了实验装置如图2所示。

(3)为了减少干扰,对于A装置有下面4种操作方案,其中最合理的是(填写数字序号)_________。
①将木炭与浓硝酸一同放在装置中加热;②先加热木炭,再将木炭投入冷浓硝酸。③先加热木炭,再加入冷浓硝酸;④先加热浓硝酸,然后将木炭投入其中;
(4)请用平衡移动原理解释B装置的作用_________(结合方程式与文字表述)。
(5)C装置中出现的现象是_________,经检测C的溶液中还含有少量氮元素,只以NO3-形式存在,写出生成该离子的化学方程式 ________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市高三联考一化学试卷(解析版) 题型:选择题
下列有关元素的性质及其递变规律正确的是
A.同主族元素形成的单质熔沸点自上而下逐渐升高
B.核外电子排布相同的微粒化学性质不一定相同
C.同主族元素含氧酸的酸性随核电荷数的增加而减弱
D.非金属元素的气态氢化物的稳定性越强其沸点就越高
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省宜宾市高三第二次诊断测试化学试卷(解析版) 题型:选择题
25℃时,将pH均为2的HCl与HX的溶液分别加水稀释,溶液pH随溶液体积变化的曲线如下图所示。下列说法正确的是

A.稀释前,c(HX)=0.01 mol/L B.稀释10倍,HX溶液的pH=3
C.a、b两点:c(X-)>c(Cl-) D.溶液的导电性:a>b
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济南市高三下学期一模考试理综化学试卷(解析版) 题型:填空题
(12分)【化学——有机化学基础】松油醇(G)可用于配制香精,其合成路线如下:


请回答下列问题:
(1)G所含两种官能团的名称分别是________、__________。
(2)同时符合下列两个条件的B的同分异构体有____________种。
i.含有六元碳环,碳环上仅有两个取代基且呈对位;
ii.在一定条件下能发生银镜反应、水解反应和消去反应。
(3)为了鉴别E和F,宜选用下列试剂中的_______作鉴别试剂(填下列序号字母)。
a.溴水 b.银氨溶液 c.酸性KMnO4溶液 d.NaHCO3溶液
(4)C→D的化学方程式为_________________。
(5)物质A(分子式为C7H10O3)催化氢化得到H(分子式为C7H12O3),H在一定条件下可以生成高聚物I,I的结构简式为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com