
【题目】在![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等物质中:
等物质中:
(1)只含有离子键的物质是_____________________;
(2)只含有共价键的物质是_______________________;
(3)既含有离子键又含有共价键的物质是_______________________;
(4)属于离子化合物的是______________;
(5)属于共价化合物的是_____________。
【答案】![]() 、
、 ![]()
![]() 、
、![]()
![]() 、
、![]()
![]() 、
、![]() 、
、![]() 、
、![]()
![]()
【解析】
根据所含元素的种类分析判断化合物类型,结合离子键和共价键的形成条件分析判断所含化学键类型。
NaF属于离子化合物,只含有离子键;
NaOH属于离子化合物,既含有离子键,又含有共价键;
CaO属于离子化合物,只含有离子键;
Cl2属于非金属单质,只含有共价键;
NH4Cl属于离子化合物,既含有离子键,又含有共价键;
H2O2属于共价化合物,只含有共价键;
(1)只含有离子键的物质是NaF、CaO,故答案为:NaF、CaO;
(2)只含有共价键的物质是Cl2、H2O2,故答案为:Cl2、H2O2;
(3)既含有离子键又含有共价键的物质是NaOH、NH4Cl,故答案为:NaOH、NH4Cl;
(4)属于离子化合物的是NaF、NaOH、CaO、NH4Cl,故答案为:NaF、NaOH、CaO、NH4Cl;
(5)属于共价化合物的是H2O2,故答案为:H2O2。


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
【题目】用以下三种途径来制取相同质量的硝酸铜:①铜与浓硝酸反应;②铜与稀硝酸反应;③铜与氧气反应生成氧化铜,氧化铜再与硝酸反应。下列叙述正确的是( )
A.三种途径所消耗的铜的物质的量不相等
B.三种途径所消耗的硝酸的物质的量相等
C.所消耗铜的物质的量是:途径③>途径①>途径②
D.所消耗硝酸的物质的量是:途径①>途径②>途径③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列说法正确的是
A.0.1 mol重水(D2O)分子中含有的中子数为NA
B.10g质量分数为46%的C2H5OH水溶液中含有的氧原子数目为0.1NA
C.标准状况下,2.24L已烷中含有的共价键数目为1.9NA
D.过氧化氢分解制得标准状况下2.24LO2,转移电子数目为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置(夹持和尾气处理装置已省略)进行的相应实验,不能达到实验目的的是
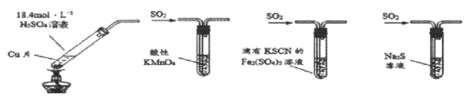
A.若将甲中上层清液倒入水中,观察到溶液呈蓝色,说明有CuSO4生成
B.图乙装置中溶液的颜色变浅,说明SO2具有漂白性
C.图丙装置中溶液的颜色变浅,说明SO2具有还原性
D.图丁装置中产生淡黄色沉淀,说明SO2或H2SO3具有氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过一硫酸氢钾复合盐(KHSO4·2KHSO5·K2SO4)常用作漂白剂和消毒剂,其制备流程如图:
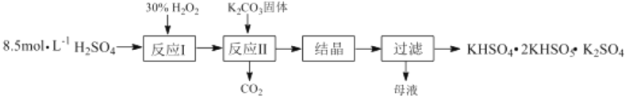
(1)反应Ⅰ的化学方程式为:H2O2+H2SO4H2SO5+H2O,△H<0;则反应Ⅱ中K2CO3与H2SO5反应生成KHSO5的化学方程式为___。
(2)生产原料的理论比值[n(H2O2):n(H2SO4)]为0.4:1,但实际生产最佳投料比为0.6:1,其原因是___。
(3)准确称取3.350g复合盐样品配制成250mL溶液,取25.00mL置于锥形瓶中,加入适量的稀硫酸和足量的KI溶液,摇匀后置于暗处,充分反应后,加入少量淀粉溶液,用0.1000mol·L-1Na2S2O3标准溶液滴定至终点,消粍标准溶液20.00mL。计算复合盐中有效成分KHSO5的质量分数。(写出计算过程)(已知:HSO5-+I-+H+→SO42-+I2+H2O,I2+S2O32-→I-+S4O62--未配平)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知元素X和Y的核电荷数都小于18,最外层电子数分别为n和(m-5),次外层分别有(n+2)个和m个电子。甲和乙分别为元素X、Y的最高价氧化物的水化物。
(1)元素名称X为____________________,Y为____________________。
(2)甲的化学式是____________________,乙的化学式是____________________。
(3)甲与乙反应的离子方程式是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,在“H2A—HA-—A2-”的水溶液体系中,H2A、HA-和A2- 三者中各自所占的物质的量分数(α)随溶液pH变化的关系如图所示。下列说法正确的是
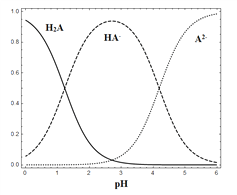
A. 在含H2A、HA-和A2- 的溶液中,加入少量NaOH固体,α(HA-)一定增大
B. 将等物质的量的NaHA和Na2A混合物溶于水,所得的溶液中α(HA-)=α(A2-)
C. NaHA溶液中,HA-的水解能力小于HA-的电离能力
D. 在含H2A、HA-和A2-的溶液中,若c(H2A)+2c(A2-)+c(OH-)=c(H+),则α(H2A)和α(HA-)一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下(T2> Tl),在3个体积均为2.0 L的恒容密闭容器中反应 2NO(g)+ Cl2(g) = 2ClNO(g)(正反应放热)达到平衡,下列说法正确的是

A. 达到平衡时,容器I与容器II中的总压强之比为1:2
B. 达到平衡时,容器III中ClNO的转化率小于80%
C. 达到平衡时,容器II中c(ClNO(/ c(NO)比容器I中的大
D. 若温度为Tl,起始时向同体积恒容密闭容器中充入0.20 mol NO(g)、0.2 mol Cl2(g)和0.20 mol ClNO(g),则该反应向正反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酒石酸托特罗定主要用于治疗泌尿系统疾病。工业合成该药物的中间体(F)的路线如下:
回答下列问题:
(1)D分子中的含氧官能团名称为 __________;B→C包含两步反应,反应类型分别为_______、_______;
(2)A的结构简式为________;
(3)写出苯甲醛与银氨溶液反应的化学方程式 _______;
(4)写出同时满足下列条件的B的一种同分异构体的结构简式:_____________;
①能使溴的CCl4溶液褪色;②能与FeCl3溶液发生显色反应;③苯环上的一氯代物有一种;④分子中有4种不同化学环境的氢。
(5)已知呋喃丙胺(![]() CH=CHCON(CH3)2 )是一种高效麻醉剂,写出以
CH=CHCON(CH3)2 )是一种高效麻醉剂,写出以![]() 、CH3CHO、NH(CH3)2为原料制备呋喃丙胺的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)_________________。
、CH3CHO、NH(CH3)2为原料制备呋喃丙胺的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com