
【题目】已知元素X和Y的核电荷数都小于18,最外层电子数分别为n和(m-5),次外层分别有(n+2)个和m个电子。甲和乙分别为元素X、Y的最高价氧化物的水化物。
(1)元素名称X为____________________,Y为____________________。
(2)甲的化学式是____________________,乙的化学式是____________________。
(3)甲与乙反应的离子方程式是___________________。
【答案】硫 铝 ![]()
![]()
![]()
【解析】
X、Y元素的核电荷数都小于18,说明都属于短周期元素,因为最外层电子数小于8,如果K层为最外层,则最外层电子数小于2,次外层电子数为2或8,根据X、Y的原子最外层分别有n个和(m-5)个电子,则m大于5,次外层分别有(n+2)个和m个电子,则n=6、m=8,所以X最外层有6个电子、次外层有8个电子,为S元素,Y原子最外层有3个电子、次外层有8个电子,则Y为Al元素,据此分析解答。
(1)X、Y元素的核电荷数都小于18,说明都属于短周期元素,因为最外层电子数小于8,如果K层为最外层,则最外层电子数小于2,次外层电子数为2或8,根据X、Y的原子最外层分别有n个和(m-5)个电子,则m大于5,次外层分别有(n+2)个和m个电子,则n=6、m=8,所以X最外层有6个电子、次外层有8个电子,为S元素,Y原子最外层有3个电子、次外层有8个电子,则Y为Al元素,故答案为:硫;铝;
(2)甲和乙分别为元素X、Y的最高价氧化物的水化物,在甲为H2SO4;乙为Al(OH)3,故答案为:H2SO4;Al(OH)3;
(3)硫酸与氢氧化铝反应的离子方程式为3H++ Al(OH)3= Al3++3H2O,故答案为:3H++ Al(OH)3= Al3++3H2O。


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:
【题目】为确认C6H5OH、H2CO3、CH3COOH的酸性强弱,某同学设计了如下图所示装置,一次实验即可达到目的(不必选用其他酸性物质)。
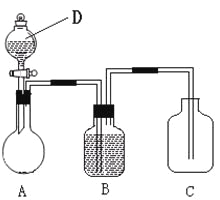
请据此实验回答下列问题:
(1)仪器D的名称是____________,所盛放的试剂应为___________(填化学式);
(2)在烧瓶中装某可溶性正盐溶液,则A中反应的离子方程式是______________;
(3)装置B中所盛的试剂是_____________,其作用是___________________;
(4)装置C中所盛的试剂是________,C中反应的化学方程式是____________;
(5)根据该实验可以得出C6H5OH、H2CO3、CH3COOH这三种物质的酸性强弱顺序为
______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A含碳76.6%,氢6.4%,氧17%,它的相对分子质量约为甲烷的5.9倍,求该有机物的分子式___________。在常温下,该有机物可与溴水反应生成白色沉淀,0.5mol恰好与1.5molBr2作用,据此确定该有机物的结构简式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态的三氧化二硼和液态水,放出649.5kJ热量,其热化学方程式为________。
(2)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式为:![]() ,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/ mol·L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
c(CO)/mol·L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
请回答下列问题:
①前2s内的平均反应速率υ(N2)=____;
②上述条件下,该反应的平衡常数为____;
③上述条件下,测得某时刻反应体系中各物质的物质的量浓度均为0.01mol/L,则此时反应处于___状态。(填“平衡”或“向右进行”或“向左进行”)
(3)实验室常用0.10mol/L KMnO4标准酸性溶液来测定H2C2O4样品的纯度(标准液滴待测液),其反应原理为:5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O。
①KMnO4标准液应装在____(填“酸式”或“碱式”)滴定管;
②清水洗净滴定管后直接装入标准液,则测定结果会____;(填“偏大”或“偏小”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等物质中:
等物质中:
(1)只含有离子键的物质是_____________________;
(2)只含有共价键的物质是_______________________;
(3)既含有离子键又含有共价键的物质是_______________________;
(4)属于离子化合物的是______________;
(5)属于共价化合物的是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ag2O2是银锌碱性电池的正极活性物质,用如下方法制备:在过量KOH溶液中加入适量AgNO3溶液,生成Ag2O沉淀;保持反应温度为80℃,再边搅拌边将一定量K2S2O8溶液缓慢加到上述混合物中。反应完全后,过滤、洗涤、真空干燥就可得到固体样品。整个制备过程可用下列化学反应方程式描述:2AgNO3+4KOH+K2S2O8 ![]() Ag2O2↓+2KNO3 +2K2SO4+2H2O。在上述制备过程中,沉淀表面吸附物质不含有( )
Ag2O2↓+2KNO3 +2K2SO4+2H2O。在上述制备过程中,沉淀表面吸附物质不含有( )
A. KNO3B. K2SO4C. KOHD. AgNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是( )

A.图中a和b分别为T1、T2温度下CdS在水中的溶解度
B.图中各点对应的Ksp的关系为:Ksp(m)=Ksp(n)<Ksp(p)<Ksp(q)
C.向m点的溶液中加入少量Na2S固体,溶液组成由m沿mpn线向p方向移动
D.温度降低时,q点的饱和溶液的组成由q沿qp线向p方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一恒温、恒容的密闭容器中存在化学平衡:H2(g)+I2(g) ![]() 2HI(g),已知H2和I2的起始浓度均为0.10molL-1,达到平衡状态时HI的浓度为0.16molL-1。若H2和I2的起始浓度均变为0.20molL-1,则平衡时H2的浓度为( )
2HI(g),已知H2和I2的起始浓度均为0.10molL-1,达到平衡状态时HI的浓度为0.16molL-1。若H2和I2的起始浓度均变为0.20molL-1,则平衡时H2的浓度为( )
A. 0.16molL-1 B. 0.08 molL-1 C. 0.04 molL-1 D. 0.02molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列有关说法正确的是_________________。
A.用金属的电子气理论能合理地解释金属易腐蚀的原因
B.手性催化剂只催化或者主要催化一种手性分子的合成
C.草酸二甲酯分子中σ键和π键个数比为6:1
D.MgCO3的热稳定性强于BaCO3
E.根据火山喷出的岩浆中冷却时ZnS比HgS先析出,能判断ZnS的晶格能大于HgS
(2)已知SbCl3、SbCl5、SnCl4的熔点依次为73.5℃、2.8℃、-33℃。依据上述实验事实回答:
①SnCl4中Sn的杂化类型为________,SbCl5的晶体类型为_______,SbCl3的空间构型为____________。
②实验测得在极性溶剂中SbCl5的溶解度比SbCl3的溶解度小得多,其主要原因是___________。
(3)人们一直致力于人工固氮的研究,以获得廉价的氮肥。科学家先后提出并合成了固氮酶的多种模拟物。其中一类是含Mo(钼)、Fe、S原子的类立方体结构,如下图所示:

图中所有实线均代表化学键,左右两边对称,各含一个类立方体的结构。每个类立方体含有4个Fe原子、4个S原子,它们位于立方体的8分顶点,且同种原子不相邻。(已知元素电负性分别为:S—2.5 Fe—1.8 Mo—1.8)
①Mo与Cr是同族元素,并且位于相邻周期,写出基态Mo原子的价电子的轨道表达式为_____________。
②钼是一种人体必需的微量元素。工业上可用辉钼矿(MoS2)焙烧除硫得三氧化钼,写出该过程的化学方程式___________________。
③上述一个类立方体中4个Fe原子所在的顶点连接所构成的空间几何体为_____________。
④在类立方体结构中,一种最近的S原子和S原子间距离为apm,该结构的密度为_______g/cm3(已知NA,只需列式,无需化简)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com