
【题目】100多年前,“化学守护神”德国化学家李比希发现了一种至今仍在临床使用的催眠药(化合物IV)。由源自石油的基本化工原料I合成化合物IV的一种途径为:
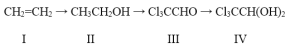
(1)由化合物I合成化合物II的反应类型为______;
(2)下列关于化合物I和化合物II的说法正确的有________(填字母)。
A. 化合物I可以作为植物生长调节剂
B. 化合物I能发生加聚反应,不能使酸性KMnO4溶液褪色
C. 化合物II能发生酯化反应
D. 化合物II不能与金属Na反应
(3)由化合物III合成化合物IV的反应的原子利用率为100%,则除化合物III外,另一种反应物是__。
(4)化合物II与IV都含有的官能团是______(填名称),化合物IV的分子式为____。
(5)为替代日益枯竭的化石资源,有人提出以富含纤维素的农林废弃物或副产物为原料获得乙醇,再制备化合物IV的方案,可用于这种用途的废弃物或副产物有____ (写两种)。
【答案】加成反应 AC 水 羟基 C2H3OCl3 一氯乙烷、三氯乙酸
【解析】
原料I合成化合物IV的一种途径为将乙烯和水在催化剂存在的条件下发生加成反应生成乙醇,将乙醇和氯气在光照条件下发生取代反应,得到三氯乙醛,三氯乙醛与水反应可以得到Cl3CCH(OH)2,然后分析。
(1)由化合物I合成化合物II是乙烯和水在催化剂条件下发生加成反应生成乙醇;
(2) A.化合物I是乙烯,乙烯可以促进植物的生长,故可以作为植物生长调节剂,故A正确;
B.化合物I是乙烯,乙烯含有碳碳双键,能发生加聚反应,可以使酸性KMnO4溶液褪色,故B错误;
C.化合物II是乙醇,乙醇和乙酸可以在浓硫酸作催化剂的条件下发生酯化反应,生成乙酸乙酯和水,故C正确;
D.化合物II是乙醇,可以和金属Na反应生成乙醇钠和氢气,故D错误;
答案选AC;
(3)由化合物III合成化合物IV的反应的原子利用率为100%,为化合反应,三氯乙醛与水反应可以得到Cl3CCH(OH)2,根据原子守恒规律,则另一种反应物为水;
(4)化合物II是CH3CH2OH,IV是Cl3CCH(OH)2,都含有的官能团是羟基;根据结构简式可知,化合物IV的分子式为C2H3OCl3;
(5)再制备化合物IV的方案,将乙醇和氯气在光照条件下发生取代反应,得到三氯乙醛,会生成氯化氢,副反应为乙醇与氯化氢生成一氯乙烷,或者三氯乙醛和次氯酸反应生成三氯乙酸和氯化氢,由三氯乙醛和水制备Cl3CCH(OH)2,副产物为一氯乙烷、三氯乙酸等。


 名师点拨卷系列答案
名师点拨卷系列答案科目:高中化学 来源: 题型:
【题目】在一定温度下的恒容密闭容器中发生反应:2SO2(g)+O2(g)![]() 2SO3(g),下列证据不能说明反应一定达到化学平衡状态的是( )
2SO3(g),下列证据不能说明反应一定达到化学平衡状态的是( )
A.容器内的压强不再改变B.c(SO2):c(O2):c(SO3)=2:1:2
C.SO2的转化率不再改变D.SO3的生成速率与SO3的消耗速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,氧化铁可以与一氧化碳发生下列反应:Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g)
2Fe(s)+3CO2(g)
(1)该反应的平衡常数表达式为K=________。
(2)该温度下,在2 L盛有Fe2O3粉末的密闭容器中通入CO气体,10 min后,生成了单质铁11.2 g。则10 min内CO的平均反应速率为________。
(3)该反应达到平衡后,加入Fe粉,平衡________移动;保持恒温恒容通入CO,平衡向________移动。(填“向左”、“向右”或“不”)
(4)表明该反应已达平衡状态的是______________
A.单位时间内生成nmolCO同时生成nmolCO2 B.恒容时混合气体的压强不变
C.混合气体的总质量不变 D.CO2的体积分数不变 E.Fe的浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把1mol X气体和0.5mol Y气体混合于2L的密闭容器中,发生如下反应:
![]() ,2min末生成0.2mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol·L-1·min-1,试计算
,2min末生成0.2mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol·L-1·min-1,试计算
(1)前2min内,用X表示的平均反应速率____________。
(2)前2min内Y的转化率____________。
(3)化学方程式中Z的化学计量数n____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂亚硫酰氯(Li/SOCl2)电池是实际应用电池系列中比能量最高的一种电池,剖视图如图所示,一种非水的LiAlCl4的SOCl2溶液为电解液。亚硫酸氯既是电解质,又是正极活性物质,其中碳电极区的电极反应式为2SOCl2+4e-=4Cl-+S+SO2↑,该电池工作时,下列说法错误的是( )

A. 锂电极区发生的电极反应:Li-e-=Li+
B. 放电时发生的总反应:4Li+2SOCl2=4LiCl+SO2↑+S
C. 锂电极上的电势比碳电极上的低
D. 若采用水溶液代替SOCl2溶液,电池总反应和效率均不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是人们在日常生活和工农业生产中应用极为广泛的一种金属。请回答下列问题:
(1)某研究性学习小组为了证明铁的金属性比铜的强,设计了如下几种方案,其中合理的有___(填序号)。
A.铁片置于硫酸铜溶液中置换出铜
B.铁、铜与氯气反应分别生成FeCl3、CuCl2
C.铜片置于FeCl3溶液中,铜片逐渐溶解
D.铁片、铜片分别置于盛有稀硫酸的烧杯中,铁片上有气泡产生,而铜片上无气泡产生
E.常温下,将铁片和铜片分别置于浓硝酸中,铁片不溶解,而铜片溶解
(2)请你另设计一个能证明铁的金属性比铜的强的实验。要求:该实验方案的原理不同于(1)中任何一个方案。
①画出实验装置图并注明所需药品___。
②写出实验过程中的主要现象:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2NO(g)+Br2(g)![]() 2NOBr(g) △H =-a kJ·mol-1 (a > 0),其反应机理如下:①NO(g)+Br2(g)
2NOBr(g) △H =-a kJ·mol-1 (a > 0),其反应机理如下:①NO(g)+Br2(g)![]() NOBr2 (g)快②NO(g)+NOBr2(g)
NOBr2 (g)快②NO(g)+NOBr2(g)![]() 2NOBr(g)慢,下列有关该反应的说法正确的是 ( )
2NOBr(g)慢,下列有关该反应的说法正确的是 ( )
A.该反应的速率主要取决于①的快慢
B.NOBr2是该反应的催化剂
C.正反应的活化能比逆反应的活化能小a kJ·mol-1
D.增大Br2 (g)浓度能增大单位体积内活化分子百分数,加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组查阅资料得知,漂白粉与硫酸溶液反应可制取氯气,化学方程式为![]() ,他们设计如下实验用于制取氯气并验证其性质。
,他们设计如下实验用于制取氯气并验证其性质。
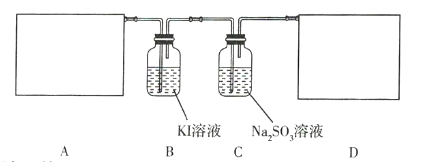
请回答下列问题。
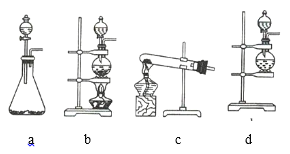
(1)该实验中A部分的装置是 _________________________________ (填序号)。
(2)B中的实验现象为 _____________________________。
(3)用离子方程式表示C中亚硫酸钠被氧化的主要原因: _____________________________。请你帮助他们设计一个实验,证明C中的亚硫酸钠已被氧化: _____________________________(简述实验步骤)。
(4)请根据题意画出D处的实验装置图,并注明装置中盛放的物质__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SF6 是一种优良的绝缘气体,分子结构中只有S─F键。已知:1 mol S(s)转化为气态硫原子吸收能量280 kJ,断裂1 mol F─F 、S─F键需吸收的能量分别为160 kJ、330 kJ。则1 mol 固体硫单质参加:S(s)+3F2(g)=SF6(g)反应,完全生成SF6(g)的热效应为( )
A. 吸收430 kJ B. 释放450 kJ
C. 释放1220 kJ D. 释放1780 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com