
【题目】已知反应:2NO(g)+Br2(g)![]() 2NOBr(g) △H =-a kJ·mol-1 (a > 0),其反应机理如下:①NO(g)+Br2(g)
2NOBr(g) △H =-a kJ·mol-1 (a > 0),其反应机理如下:①NO(g)+Br2(g)![]() NOBr2 (g)快②NO(g)+NOBr2(g)
NOBr2 (g)快②NO(g)+NOBr2(g)![]() 2NOBr(g)慢,下列有关该反应的说法正确的是 ( )
2NOBr(g)慢,下列有关该反应的说法正确的是 ( )
A.该反应的速率主要取决于①的快慢
B.NOBr2是该反应的催化剂
C.正反应的活化能比逆反应的活化能小a kJ·mol-1
D.增大Br2 (g)浓度能增大单位体积内活化分子百分数,加快反应速率
科目:高中化学 来源: 题型:
【题目】在1L定容的密闭容器中,可以证明可逆反应N2+3H2![]() 2NH3已达到平衡状态的是
2NH3已达到平衡状态的是
A. c(N2):c(H2):c(NH3)=1:3:2
B. 一个N≡N 断裂的同时,有3个H-H生成
C. 其他条件不变时,混合气体的密度不再改变
D. v正(N2)═2 v逆(NH3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学工业体现了化学科学的实际应用价值,下列化学工业过程,以生产盐类化合物为主要目标的是( )
A.侯氏制碱法B.煤的气化C.合成氨工业D.氯碱工业
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100多年前,“化学守护神”德国化学家李比希发现了一种至今仍在临床使用的催眠药(化合物IV)。由源自石油的基本化工原料I合成化合物IV的一种途径为:
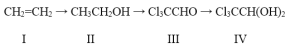
(1)由化合物I合成化合物II的反应类型为______;
(2)下列关于化合物I和化合物II的说法正确的有________(填字母)。
A. 化合物I可以作为植物生长调节剂
B. 化合物I能发生加聚反应,不能使酸性KMnO4溶液褪色
C. 化合物II能发生酯化反应
D. 化合物II不能与金属Na反应
(3)由化合物III合成化合物IV的反应的原子利用率为100%,则除化合物III外,另一种反应物是__。
(4)化合物II与IV都含有的官能团是______(填名称),化合物IV的分子式为____。
(5)为替代日益枯竭的化石资源,有人提出以富含纤维素的农林废弃物或副产物为原料获得乙醇,再制备化合物IV的方案,可用于这种用途的废弃物或副产物有____ (写两种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质A由三种元素组成。M是单质,空气的主要成分之一。B是一种固体单质,组成该物质的元素在A中的质量分数约为![]() 。C、D均由两种元素组成,C中两元素同主族。I是一种建筑用的黏合剂。各物质之间的转化关系如图:
。C、D均由两种元素组成,C中两元素同主族。I是一种建筑用的黏合剂。各物质之间的转化关系如图:
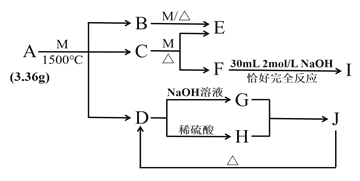
请回答:
![]() 中所含元素是_____________
中所含元素是_____________![]() 填元素名称
填元素名称![]() 。
。
![]() 与M反应的化学方程式为_______________________________________。
与M反应的化学方程式为_______________________________________。
![]() 写出
写出![]() 的离子方程式___________________________________________。
的离子方程式___________________________________________。
![]() 请设计实验方案证明E可能的成分___________________________________________。
请设计实验方案证明E可能的成分___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是( )
A. 开启啤酒瓶盖,瓶中立即泛起大量泡沫
B. 工业生产硫酸的过程中使用过量的空气以提高SO2的利用率
C. 将铜粉和锌粉混合后放入稀硫酸中,产生气体的速率比不加铜粉快
D. 在pH等于3的醋酸溶液中加入少量CH3COONa,溶液pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中的甲、乙、丙、丁代表化学中常见的四种物质,其中甲、乙、丙均含有同一种元素。相互转化的关系如下,请回答下列问题。
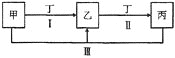
(1)甲气体的水溶液能使酚酞变红,乙为空气中含量最大的气体,写出反应![]() Ⅲ
Ⅲ![]() 的化学方程式:________________________________。
的化学方程式:________________________________。
(2)常温下![]() 的丁溶液pH为13,其焰色反应为黄色。甲、乙、丙为均含有同一种金属元素的无机化合物,反应
的丁溶液pH为13,其焰色反应为黄色。甲、乙、丙为均含有同一种金属元素的无机化合物,反应![]() Ⅲ
Ⅲ![]() 的离子方程式为___________________________________。
的离子方程式为___________________________________。
(3)若乙为淡黄色非金属单质,则反应![]() Ⅲ
Ⅲ![]() 中氧化产物与还原产物的物质的量之比为______________,
中氧化产物与还原产物的物质的量之比为______________,![]() 甲与含
甲与含![]() 的溶液充分反应后溶液呈碱性,溶液中所含乙元素的相关离子浓度的大小关系为________________。
的溶液充分反应后溶液呈碱性,溶液中所含乙元素的相关离子浓度的大小关系为________________。
(4)若甲、乙、丙的溶液均显碱性,丁为温室效应主要气体。浓度相同的乙、丙溶液pH较大的是______________![]() 填溶质的化学式
填溶质的化学式![]() 溶液,原因是______________________________。
溶液,原因是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图①Ⅰ、Ⅱ、Ⅲ是常见的气体发生装置,Ⅳ、Ⅴ、Ⅵ是气体收集装置。根据要求回答下列问题: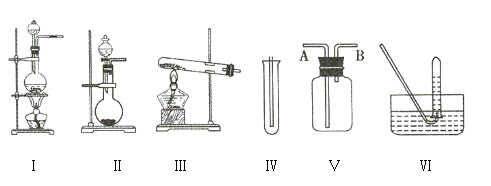
(1)若用![]() 与浓盐酸反应制取氯气,应选用装置 ___________________ 。
与浓盐酸反应制取氯气,应选用装置 ___________________ 。
(2)若用![]() 与浓盐酸反应制取氯气,应选用装置 ___________________ ,试完成并配平下列离子方程式:
与浓盐酸反应制取氯气,应选用装置 ___________________ ,试完成并配平下列离子方程式:
___________________ ![]() + ___________________
+ ___________________ ![]() + ___________________
+ ___________________ ![]() ___________________
___________________ ![]() + ___________________
+ ___________________ ![]() + ___________________ 。
+ ___________________ 。
(3)若选用装置Ⅳ为氯气的收集装置,则应该在试管口中放置一团棉花,该棉花团需用 ___________________ 溶液浸润,其作用是 ___________________ 。
(4)若选用装置Ⅴ为氯气的收集装置,则氯气应从 ___________________ (填“A”或“B”)口通入,利用化学原理检验氯气已收集满的方法是 ___________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知2H→H2放出437.6 kJ的热量,下列说法正确的是_______
A. 氢气分子内每个氢原子都达到稳定结构
B. 氢气分子的能量比两个氢原子的能量低
C. 1 mol H2 离解成 2 mol H 要放出437.6 kJ热量
D. 氢原子比氢气分子稳定
(2)已知原电池的总反应式:Cu + 2FeCl3 = CuCl2 + 2FeCl2,请写出电极反应方程式:
负极___________________________________
正极___________________________________
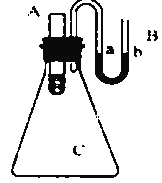
(3)如图所示,在锥形瓶放置装有水的小试管,往小试管中分别加入下列物质:①烧碱固体 ②浓硫酸 ③硝酸铵固体④NaCl固体,其中能使a端液面高于b端液面的是_______________。(填序号)
(4)科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术2H2O![]() 2H2↑+O2↑。制得的氢气可用于制作燃料电池.试回答下列问题:
2H2↑+O2↑。制得的氢气可用于制作燃料电池.试回答下列问题:
①分解海水时,实现了光能转化为______能;生成的氢气用于制作燃料电池时,实现了化学能转化为______能;分解海水的反应属于______反应(填“放热”或“吸热”)。
②某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,A极上发生的电极反应为:2H2 + 2O24e=2H2O,则A极是电池的______极,电子从该极______(填“流入”或“流出”),B极的电极反应式为:_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com