
【题目】用Na表示阿伏加德罗常数的值,下列叙述错误的是
A.含有NA个氢原子的氢气在标准状况下的体积约为11.2L
B.25℃,1.01×105Pa,64gSO2中含有的原子数为3Na
C.在常温常压下,35.5g Cl2含有的分子数为0.5Na
D.标准状况下,11.2LH2O含有的分子数为0.5NA
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】如图是SO2(g)和O2(g)反应生成SO3(g)的能量变化示意图,由图可知( )
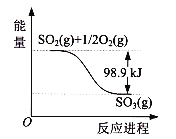
A. 2 SO2(g)+ O2(g)![]() 2 SO3(g) △H= -197.8 kJ/mol
2 SO3(g) △H= -197.8 kJ/mol
B. 2 SO2(g)+ O2(g)![]() 2 SO3(g) △H= +197.8 kJ/mol
2 SO3(g) △H= +197.8 kJ/mol
C. 2 SO2(g)+ O2(g)![]() 2 SO3(g) △H= +98.9 kJ/mol
2 SO3(g) △H= +98.9 kJ/mol
D. 2 SO2(g)+ O2(g)![]() 2 SO3(g) △H= -98.9 kJ/mol
2 SO3(g) △H= -98.9 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生为了探究锌与盐酸反应过程中的速率变化,在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气。(实验记录的体积为累计值,已换算成标准状况):
时间(min) | 1 | 2 | 3 | 4 | 5 |
氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5 min)反应速率最大___,原因是___。
(2)哪一段时段的反应速率最小___,原因是___。
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)___。
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:
A.蒸馏水 B.NaCl溶液 C.NaNO3溶液D.Na2CO3溶液
你认为可行的是(填编号)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲用240 mL1.0mol·L-1的NaOH溶液,实验操作步骤有:
A.用烧杯在天平上称出ag氢氧化钠固体,加入适量蒸馏水使它完全溶解并冷却至室温;
B.继续向容量瓶中加蒸馏水至液面距刻度线1~2 cm处,改用胶头滴管小心滴加蒸馏水至凹液面与刻度线相切;
C.把制得的溶液小心转移至容量瓶中;
D.将容量瓶瓶塞塞紧,充分摇匀。
E.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心注入容量瓶,轻轻振荡;
请填写下列空白:
(1)操作步骤的正确顺序为_____(填字母)。
(2)本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、____、____。
(3)某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图所示(左码右物)。烧杯的实际质量为___g,要完成本实验该同学应称出___gNaOH。
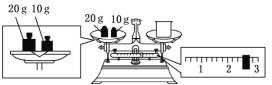
(4)使用容量瓶前必须进行的一步操作是____。
(5)在配制过程中,其他操作都是正确的,下列操作会引起误差偏高的是___。
A.用滤纸称量NaOH固体
B.定容时俯视刻度线
C.未冷却到室温就将溶液转移到容量瓶并定容
D.定容后塞上瓶塞反复倒转摇匀,静置后,液面低于刻度线,再加水至刻度线
(6)若加蒸馏水定容时不慎超过刻度线,处理方法是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B均是由两种元素组成的化合物,A中某种元素的质量分数为75%,B是一种淡黄色固体,C、J是同周期元素的气态氢化物,其中C是含氢量最高的烃,X为常见的无色液体。反应生成的水均已略去。它们有如下图所示的关系。
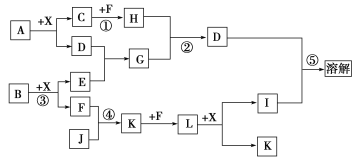
(1)写出化学式:A________,B________,J________;
(2)反应③中每生成1 mol F,转移电子的数目为______________;
(3)反应④的化学方程式为:______________________________;
(4)写出离子方程式:反应②________________________________,反应⑤________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )

A.FeCl3溶液、Fe(OH)3胶体与Fe(OH)3沉淀的本质区别是有没有丁达尔效应
B.将NaOH溶液与FeCl3溶液混合可制成Fe(OH)3胶体
C.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
D.胶体、分散系、混合物概念间的从属关系可用如图表示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是
A. Ba(HCO3)2溶液与少量的NaOH溶液反应:Ba2++HCO![]() +OH-=BaCO3↓+H2O
+OH-=BaCO3↓+H2O
B. 次氯酸钙溶液中通入过量的二氧化碳 Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO
C. 用氨水吸收少量二氧化硫 OH-+SO2=HSO3-
D. 硫酸与氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为除去括号内的杂质,所选用的试剂或方法不正确的是
A. Na2CO3溶液(NaHCO3),选用适量的NaOH溶液
B. NaHCO3溶液(Na2CO3),应通入过量的CO2气体
C. Na2O2粉末(Na2O),将混合物在氧气中加热
D. Na2CO3溶液(Na2SO4),加入适量Ba(OH)2溶液,过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产钠和烧碱的原理如下:
①电解熔融氯化钠制钠:2NaCl(熔融) ![]() 2Na+Cl2↑
2Na+Cl2↑
②电解饱和食盐水制烧碱:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
下列有关说法正确的是
A.在反应①和②中,氯化钠均既是氧化剂,又是还原剂
B.在反应①中氯气是还原产物,在反应②中氢气是还原产物
C.若标准状况下生成等体积的气体,则反应①和②中消耗的氯化钠质量相等
D.若消耗等质量的氯化钠,则反应①和②中转移电子总数相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com