
【题目】【2015四川卷】(NH4)2SO4是常见的化肥和化工原料,受热易分解。某兴趣小组拟探究其分解产物。
[查阅资料] (NH4)2SO4在260℃和400℃时分解产物不同。
[实验探究]该小组拟选用下图所示装置进行实验(夹持和加热装置略)
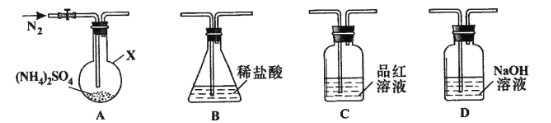
实验1:连接装置A-B-C-D,检查气密性,按图示加入试剂(装置B盛0.5000mol/L盐酸70.00mL)。通入N2排尽空气后,于260℃加热装置A一段时间,停止加热,冷却,停止通入N2。品红溶液不褪色,取下装置B,加入指示剂,用0.2000mol/L NaOH溶液滴定剩余盐酸,终点时消耗NaOH溶液25.00 mL。经检验滴定后的溶液中无SO42-。
(1)仪器X的名称是________________。
(2)滴定前,下列操作的正确顺序是_________(填字母编号)。
a.盛装0.2000mol/L NaOH溶液 b.用0.2000mol/L NaOH溶液润洗
c.读数、记录 d.查漏、清洗 e.排尽滴定管尖嘴的气泡并调整液面
(3)装置B内溶液吸收气体的物质的量是__________mol
实验2:连接装置A-D-B,检查气密性,按图示重新加入试剂。通入N2排尽空气后,于400℃加热装置A至(NH4)2SO4完全分解无残留物,停止加热,冷却,停止通入N2。观察到装置A、D之间的导气管内有少量白色固体。经检验,该白色固体和装置D内溶液中有SO32-,无SO42-。进一步研究发现,气体产物中无氮氧化物。
(4)检验装置D内溶液中有SO32-,无SO42-的实验操作和现象是__________.
(5)装置B内溶液吸收的气体是____________.
(6)(NH4)2SO4在400℃分解的化学方程式是______________________.
【答案】
(1)圆底烧瓶
(2)dbaec
(3)0.03 mol
(4)取少量装置D内溶液于试管中,滴加BaCl2溶液,生成白色沉淀;加入足量稀盐酸后沉淀完全溶解,放出无色刺激性气体
(5)NH3
(6)3(NH4)2SO4![]() 4NH3↑+ N2↑+3SO2↑ + 6H2O↑
4NH3↑+ N2↑+3SO2↑ + 6H2O↑
【解析】(1)仪器X为圆底烧瓶。
(2)滴定操作步骤为:首先查漏、水洗,再用待装的溶液润洗,再装液,再排尽滴定管尖嘴的气泡并调整液面,最后记录读数。
(3)由题意知:品红溶液不褪色,说明无SO2,滴定后的溶液中无SO42-,说明无SO3则装置B中吸收的气体为NH3。n(HCl)= n(NH3) +n(NaOH),则得答案为0.03 mol
(4)取装置D内溶液少许于试管中,加入BaCl2溶液,再加入稀盐酸,若产生白色沉淀且加入盐酸后白色沉淀能完全溶液,则说明原溶液中有SO32-,无SO42-
(5)NH3
(6)3(NH4)2SO4![]() 4NH3↑+ N2↑+3SO2↑ + 6H2O
4NH3↑+ N2↑+3SO2↑ + 6H2O


科目:高中化学 来源: 题型:
【题目】已知A 是一种相对分子质量为28的气态烃,现以A为主要原料合成一种具有果香味的物质E(分子式为C4H8O2),其合成路线如下图所示。

请回答下列问题:
(1)写出A的结构简式 __________________________ 。
(2)B、D分子中的官能团名称分别是 ___________、______________。
(3)写出下列反应的化学方程式:
①_____________________________________ ;反应类型:__________________ 。
④_____________________________________;反应类型:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于各图的说法,正确的是 ( )

A.①中阴极处能产生使湿润淀粉KI试纸变蓝的气体
B.②中待镀铁制品应与电源正极相连
C.③中钢闸门应与外接电源的正极相连
D.④中的离子交换膜可以避免生成的Cl2与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式是( )
A. 用银氨溶液检验乙醛的醛基: CH3CHO+2Ag(NH4)2OH![]() CH3COONH4+3NH3+2Ag↓+H2O
CH3COONH4+3NH3+2Ag↓+H2O
B. 苯酚钠溶于碳酸溶液:2C6H5O-+CO2+H2O→2C6H5OH+CO32-
C. 硫酸铜溶液与硫化氢的反应:Cu2++H2S=CuS↓+2H+
D. 溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+=AgBr↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数,下列叙述正确的是( )
A. 室温下,lLpH=13的NaOH溶液中,由水电离的OH-数目为0.1NA
B. 标准状况下,2.24LCl2通入水中充分反应,转移电子数目0.1NA
C. 常温常压下,42g乙烯和丁烯混合气体中,含原子数目为9NA
D. 氢氧燃料电池正极消耗22.4L (标准状况)气体时,电路中通过的电子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Glaser反应在研究新型发光材料、超分子化学等方面具有重要价值。一定条件下丙炔(CH≡CCH3)发生Glaser反应制备CH3C≡C—C≡CCH3时,主要副产物为CH3CH2CH3,发生的反应为
I.2CH≡CCH3(g)![]() CH3C≡C—C=CCH3(g)+H2(g) △H1=+60 kJ·mol-1
CH3C≡C—C=CCH3(g)+H2(g) △H1=+60 kJ·mol-1
II.CH≡CCH3(g)+2H2(g)![]() CH3CH2CH3(g) △H2=-179kJ·mol-1
CH3CH2CH3(g) △H2=-179kJ·mol-1
请回答:
(1)反应II的平衡常数表达式K=__________。
(2)为提高CH3C≡C—C=CCH3的产率,可采取的措施为______(任写两条)。
(3)己知:C—H、H —H 的键能分别为414 kJ·mol-1、436 kJ·mol-1,则C—C 的键能为____ kJ·mol-1。
(4)欲提高反应I的速率,向其中加入傕化剂,使该反应分两步进行,且均为吸热反应。下如图为未加催化剂时反应I的能量变化图,请画出加入催化剂后反应过程的能量变化图_____________。
(5)一定温度下,向某恒容密闭容器中充人一定量的CH≡CCH3(g)+2H2(g),发生反应II。一段时间内测定CH3CH2CH3(g)与H2(g)的消耗速率,二者关系如下如图中AB曲线所示。B点时,该反应_________(填“是”或“否”)达到平衡状态,原因为_____________;若此时升高温度,二者速率关系相应的点可能为______________(填字母)。
(6) CH3CH2CH3碱性燃料电池是一种高性能燃料电池,其工作原理如下如图所示。b电极为________(填“正极”或“负极”),该电极的反应式为_______________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com