
ЎѕМвДїЎїє¬Бт»ЇєПОпµДЦЦАаєЬ¶аЈ¬ПЦУРH2SO4ЎўH2SO3ЎўSO2ЎўNa2SO3ЎўBaSO4ЎўCuSO4ЎўNa2SO4Хв7ЦЦіЈјыµДє¬Бт»ЇєПОпЎЈ»ШґрПВБРОКМвЈє
(1)H2SO3ЧЄ»ЇОЄБтЛбКЗЛбУкРОіЙµДЦШТЄ№эіМЦ®Т»Ј¬РґіцЖд·ґУ¦µД»ЇС§·ЅіМКЅЈ¬Іў±кГчµзЧУЧЄТЖµД·ЅПтєНКэДїЈє_______________________________________ЎЈ
(2)іЈОВПВЈ¬Ѕ«Мъ°фЦГУЪЕЁБтЛбЦРЈ¬ОЮГчПФПЦПуЈ¬їО±ѕЙПЅвКНОЄ·ўЙъБЛ¶Ы»ЇЈ¬µ«УРИЛИПОЄОґ·ўЙъ·ґУ¦ЎЈОЄСйЦ¤ґЛ№эіМЈ¬ДіН¬С§ѕ№эЛјїјЈ¬ЙијЖБЛИзПВКµСйЈєЅ«ѕЕЁБтЛᴦАн№эµДМъ°фПґѕ»єуЦГУЪCuSO4ИЬТєЦРЈ¬ИфМъ°ф±нГж_______________________Ј¬Фт·ўЙъБЛ¶Ы»ЇЈ»ИфМъ°ф±нГж____________________Ј¬ФтОґ·ўЙъ·ґУ¦ЎЈ
(3)УГNa2SO3ОьКХ·ЁКЗЦОАнSO2ОЫИѕµДТ»ЦЦ·Ѕ·ЁЈ¬ЖдФАнОЄ(УГ»ЇС§·ЅіМКЅ±нКѕ)Јє _______________________________________________________________ЎЈ
(4)јхЙЩSO2µДОЫИѕІў±д·ПОЄ±¦Ј¬ОТ№ъХэФЪМЅЛчФЪТ»¶ЁМхјюПВУГCO»№ФSO2µГµЅµҐЦКБтµД·Ѕ·ЁАґіэИҐSO2Ј¬ёГ·ґУ¦µД»ЇС§·ЅіМКЅЈє______________________ЎЈ
Ўѕґр°ёЎї![]() ===2H2SO4ОЮємЙ«ОпЦКОціцУРємЙ«ОпЦКОціцNa2SO3Ј«SO2Ј«H2O===2NaHSO3SO2Ј«2CO
===2H2SO4ОЮємЙ«ОпЦКОціцУРємЙ«ОпЦКОціцNa2SO3Ј«SO2Ј«H2O===2NaHSO3SO2Ј«2CO![]() SЈ«2CO2
SЈ«2CO2
ЎѕЅвОцЎї
(1)СЗБтЛб±»Сх»ЇЙъіЙБтЛбЈ¬ёщѕЭµзЧУЧЄТЖКШєгЕдЖЅЈ¬±кіцµзЧУµзЧУЧЄТЖКэДїУл·ЅПтИзЈє ![]() =2H2SO4 Ј» (2)¶Ы»ЇКЗФЪЅрКф±нГжЙъіЙТ»ІгЦВГЬµДСх»ЇОп±Ј»¤Д¤Ј¬ЧиЦ№ДЪІїЅшРР·ґУ¦Ј¬Иф·ўЙъ¶Ы»ЇЈ¬ФтСх»ЇД¤±Ј»¤МъЈ¬І»ДЬєНБтЛбН·ўЙъЦГ»»·ґУ¦Ј¬јґМъ±нГжОЮємЙ«ОпЦКОціцЈ¬ИфІ»¶Ы»ЇЈ¬ФтМъ±нГжУРємЙ«ОпЦКОціцЈ»(3) СЗБтЛбДЖєН¶юСх»ЇБт·ґУ¦ЙъіЙСЗБтЛбЗвДЖЈ¬·ґУ¦·ЅіМКЅОЄЈєNa2SO3Ј«SO2Ј«H2O=2NaHSO3 (4) УГCO»№ФSO2µГµЅµҐЦКБтµД·Ѕ·ЁАґіэИҐЈ¬Т»Сх»ЇМјЙъіЙ¶юСх»ЇМјЈ¬·ґУ¦·ЅіМКЅОЄЈєSO2Ј«2CO
=2H2SO4 Ј» (2)¶Ы»ЇКЗФЪЅрКф±нГжЙъіЙТ»ІгЦВГЬµДСх»ЇОп±Ј»¤Д¤Ј¬ЧиЦ№ДЪІїЅшРР·ґУ¦Ј¬Иф·ўЙъ¶Ы»ЇЈ¬ФтСх»ЇД¤±Ј»¤МъЈ¬І»ДЬєНБтЛбН·ўЙъЦГ»»·ґУ¦Ј¬јґМъ±нГжОЮємЙ«ОпЦКОціцЈ¬ИфІ»¶Ы»ЇЈ¬ФтМъ±нГжУРємЙ«ОпЦКОціцЈ»(3) СЗБтЛбДЖєН¶юСх»ЇБт·ґУ¦ЙъіЙСЗБтЛбЗвДЖЈ¬·ґУ¦·ЅіМКЅОЄЈєNa2SO3Ј«SO2Ј«H2O=2NaHSO3 (4) УГCO»№ФSO2µГµЅµҐЦКБтµД·Ѕ·ЁАґіэИҐЈ¬Т»Сх»ЇМјЙъіЙ¶юСх»ЇМјЈ¬·ґУ¦·ЅіМКЅОЄЈєSO2Ј«2CO![]() SЈ«2CO2ЎЈ
SЈ«2CO2ЎЈ


 КојЩЅУБ¦ИьРВЅ®ЗаЙЩДкіц°жЙзПµБРґр°ё
КојЩЅУБ¦ИьРВЅ®ЗаЙЩДкіц°жЙзПµБРґр°ё
| Дкј¶ | ёЯЦРїОіМ | Дкј¶ | іхЦРїОіМ |
| ёЯТ» | ёЯТ»Гв·СїОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СїОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СїОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СїОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СїОіМНЖјцЈЎ | іхИэ | іхИэГв·СїОіМНЖјцЈЎ |
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїNa2S2O3Ў¤5H2OіЈУГЧчіеПґХХПаµЧЖ¬µД¶ЁУ°јБЈ¬КµСйКТТФNa2SЎўNa2CO3ЎўSO2ОЄФБПЈ¬АыУГПВНјЧ°ЦГїЙЦЖИЎЙЩБїNa2S2O3Ў¤5H2OЈ¬ЖдКµСйФАнОЄNa2CO3+SO2=Na2S2O3+CO2Ј»2Na2S+3SO2==2Na2SO3+3SЈ»Na2SO3+S=Na2S2O3ЎЈ»ШґрПВБРОКМв:
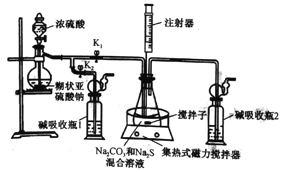
(1)ґтїЄK1Ј¬№Ш±ХK2Ј¬Ѕ«Ч¶РОЖїЦРµДИЬТєјУИИЦБ35ЎжЈ¬ґтїЄµОТєВ©¶·»оИыВэВэµОјУЕЁБтЛбЈ¬Ч¶РОЖїЦРµДПЦПуКЗ: ўЩµј№ЬїЪУРЖшЕЭГ°іцЈ»ўЪ__________________ЎЈ
(2)НЁ№эЧўЙдЖчИЎСщЈ¬јаїШЧ¶РОЖїЦРИЬТєpH=7Ў«8Ј¬Ч¶РОЖїЦРЛбРФІ»ДЬ№эЗїµДФТтКЗ_______ЎЈµ±Ч¶РОЖїЦРИЬТєµДpHЅУЅь7К±Ј¬У¦ЅшРРµДІЩЧчКЗ__________________________ЎЈ
(3)·ґУ¦ЅбКшєуЅ«Ч¶РОЖїЦР»мєПТєѕИзПВґ¦АнїЙNa2S2O3Ў¤5H2OґЦѕ§Ме:
![]()
ўЩіГИИ№эВЛµДДїµДКЗ______________________ЎЈ
ўЪґЦѕ§МеЦРє¬УРNa2CO3ЎўNa2SO3ЎўNa2SO4µИФУЦК,АыУГПВБРМṩµДКФјБЈ¬јмСйґЦІъЖ·ЦРє¬УРNa2CO3ЎЈ
їЙСЎКФјБ: a.Ж·ємИЬТє b.ЛбРФёЯГМЛбјШИЬТє c.іОЗеКЇ»ТЛ® d.NaOHИЬТє e.ПЎБтЛб
КµСй·Ѕ°ё:ИЎККБїЛщµГґЦѕ§МеЕдіЙИЬТєЈ¬µОјУЧгБїµДПЎБтЛбЈ¬Ѕ«ІъЙъµДЖшМеТАґОНЁ№эЛбРФёЯГМЛбјШИЬТєЎў_____(МоКФјБРтєЕ)ЎўіОЗеКЇ»ТЛ®Ј¬Иф______(МоПЦПу),ФтЦ¤ГчІъЖ·ЦРє¬УРNa2CO3ЎЈ
(4)ґЦѕ§МеЦРNa2S2O3Ў¤5H2OЦКБї·ЦКэµДІв¶Ё:іЖИЎ2.500gґЦѕ§МеИЬУЪЛ®Ј¬ЕдіЙ100mLИЬТєЈ¬ИЎ25.00mLИЬТєУЪЧ¶РОЖїЦР,УГ0.4000 mol/LµДЛбРФёЯГМЛбјШ±кЧјИЬТєµО¶Ё,ПыєД±кЧјИЬТєµДМе»эОЄ10.00mLЈ¬Na2S2O3Ў¤5H2OµДЦКБї·ЦКэОЄ______ (єцВФФУЦК¶ФµО¶ЁµДУ°ПмЈ»S2O32-±»ЛбРФёЯГМЛбјШИЬТєСх»ЇОЄSO42-)ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎї»ЇС§ЦРУРРн¶аОпЦКЦ®јдµД·ґУ¦·ыєППВБР№ШПµНјЈ¬НјЦРЖдЛыІъОпј°·ґУ¦ЛщРиМхјюѕщТСВФИҐЎЈ
![]()
![]()
![]()
![]()
![]()
![]()
![]()
¶ФУЪЙПНјµД±д»ЇПВБРЕР¶ПІ»ХэИ·µДКЗ(ЎЎЎЎ)
A. µ±AКЗХэСОЎўXКЗЗїЛбК±Ј¬DїЙДЬКЗЛбРФСх»ЇОп
B. µ±XКЗЗїјоИЬТєК±Ј¬BТ»¶ЁКЗNH3
C. BїЙДЬКЗµҐЦК
D. DїЙДЬКЗТ»ЦЦЛб
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїіЈОВПВЈ¬VL pHЈЅ2µДСОЛбУл0.2L pHЈЅ12µД°±Л®»мєПЈ¬ИфЛщµГИЬТєПФЛбРФЈ¬ПВБРУР№ШЕР¶ПХэИ·µДКЗ(ЎЎЎЎ)
A. VТ»¶ЁµИУЪ0.2
B. VґуУЪ»тµИУЪ0.2
C. »мєПИЬТєЦРАлЧУЕЁ¶ИТ»¶ЁВъЧгЈєc(ClЈ)>c(NH![]() )> c(HЈ«)>c(OHЈ)
)> c(HЈ«)>c(OHЈ)
D. »мєПИЬТєЦРАлЧУЕЁ¶ИТ»¶ЁВъЧгЈєc(NH![]() )Ј«c(HЈ«)ЈЅ c(ClЈ)Ј«c(OHЈ)
)Ј«c(HЈ«)ЈЅ c(ClЈ)Ј«c(OHЈ)
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїАыУГИзНјЛщКѕµДЧ°ЦГКХјЇТФПВЖшМеЈєўЩH2Ј¬ўЪCl2Ј¬ўЫO2Ј¬ўЬHClЈ¬ўЭNOЈ¬ўЮSO2Ј¬ўЯNO2ЎЈ
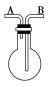
(1)ИфЙХЖїКЗёЙФпµДЈ¬ФтУЙBїЪЅшЖшЈ¬їЙКХјЇµДЖшМеКЗ________Ј¬ИфУЙAїЪЅшЖшЈ¬їЙКХјЇµДЖшМеУР________ЎЈ
(2)ИфФЪЙХЖїДЪідВъЛ®Ј¬їЙКХјЇµДЖшМеУР________Ј¬ЖшМеУ¦УЙ________їЪЅшИлЎЈ
(3)ИфЙХЖїЦРЧ°ИлККБїЕЁБтЛбЈ¬їЙТФУГЛьАґёЙФпµДЖшМеУР________Ј¬ЖшМеУ¦УЙ________їЪЅшИлЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїПВБРіэФУ·Ѕ·ЁСЎУГґнОуµДКЗ
ОпЦК(АЁєЕДЪОЄФУЦК) | іэФУ·Ѕ·Ё | |
A | Пх»щ±Ѕ(±Ѕ) | ХфБу |
B | ТТП©(SO2) | NaOHИЬТєЈ¬ПґЖш |
C | јєНй(јєП©) | деЛ®Ј¬·ЦТє |
D | µн·ЫИЬТє(NaCl) | ЙшОц |
A.AB.BC.CD.D
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїЦР№ъТ©С§јТНАЯПЯПТт·ўПЦЗаЭпЛШј°Ждї№Е±БЖР§Ј¬ИЩ»сЕµ±ґ¶ыЙъАнС§»тТЅС§Ѕ±ЎЈЗаЭпЛШЅб№№КЅИзУТНјЛщКѕЈ¬ПВБРУР№ШЗаЭпЛШСРѕїµДЛµ·ЁІ»ХэИ·µДКЗ
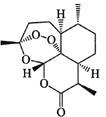
A. МбИЎ№эіМОЄ·АЦ№ЖЖ»µЗаЭпЛШЅб№№У¦±ЬГвёЯОВЈ¬№КУГµН·РµгИЬјБТТГСЅшРРЭНИЎ
B. їЙК№УГємНв№вЖЧІвіцХвёц·ЦЧУµДПа¶Ф·ЦЧУЦКБїЈ¬ТІїЙУГЦКЖЧТЗИ·¶ЁХвёц·ЦЧУµД»·ЧґЅб№№
C. ЗаЭпЛШКЗЦ¬ИЬРФµДЈ¬јИїЙїґЧчКЗГСАаТІїЙїґЧчКЗхҐАа»ЇєПОпЈ¬јИУРСх»ЇРФУЦУР»№ФРФ
D. ФЄЛШ·ЦОцТЗїЙТФИ·¶ЁЗаЭпЛШЦРКЗ·сє¬УРCЎўHЎўOµИФЄЛШ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎї¶ФёЦМъЦЖЖ·ЅшРРї№ёЇКґґ¦АнЈ¬їЙККµ±СУі¤ЖдК№УГКЩГьЎЈ
(1)ї№ёЇКґґ¦АнЗ°Ј¬ЙъІъЦРіЈУГСОЛбАґіэМъРвЈЁFe2O3Ј©ЎЈПЦЅ«Т»±нГжЙъРвµДМъјю·ЕИлСОЛбЦРЈ¬іэИҐМъРвµД»ЇС§·ґУ¦µДАлЧУ·ЅіМКЅОЄЈє___________ЎЈ
(2)АыУГИзНјЧ°ЦГЈ¬їЙТФДЈДвМъµДµз»ЇС§·А»¤ЎЈ

ўЩИфXОЄМј°фЈ¬ОЄјх»єМъјюµДёЇКґЈ¬їЄ№ШKУ¦ЦГУЪ________ґ¦ЎЈ
ўЪИфXОЄРїЈ¬їЄ№ШKЦГУЪMґ¦Ј¬ёГµз»ЇС§·А»¤·ЁіЖОЄ________ЎЈ
(3)ЙПНјЦРИфXОЄґЦНЈ¬ИЭЖчЦРєЈЛ®Мж»»ОЄБтЛбНИЬТєЈ¬їЄ№ШKЦГУЪNґ¦Ј¬Т»¶ОК±јдєуЈ¬µ±МъјюЦКБїФцјУ3.2 gК±Ј¬ ЧЄТЖµДµзЧУКэОЄ_______NAЎЈ
(4)Мъјю±нГж¶ЖНїЙУРР§·АЦ№Мъ±»ёЇКґЈ¬Из№ыМъјюІї·ЦОґ¶ЖЙПНЈ¬»т¶ЖІгЖЖЛ𣬶ЖНМъ±И¶ЖРїМъ·ґ¶шёьТЧ±»ёЇКґЈ¬ЗлјтТЄЛµГчФТтЈє______________________________ЎЈ
Ійїґґр°ёєНЅвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com