
����Ŀ��������������������Ҫ����������Ʒ���㷺���ڹ�����ʯ�͡���֯��ұ��ʳƷ�ȹ�ҵ������������ָ������������ᣬ ��������ָ�ռ�ʹ���ش��������⣺
(1)д������ϡ����ֱ�������������Һ��Ӧ�����ӷ���ʽ��________
(2)�뽫������������������λ�ڵ������ڵ�Ԫ�أ���ԭ�Ӱ뾶�ɴ�С��˳������_____
(3)�ȵķǽ����Ա���______(����ǿ����������)������������ʵ˵����Ľ���_______
(4)ij�ռ���Һ�к�0.1molNaOH�������Һͨ��һ����CO2����ַ�Ӧ��������Һ�������ɣ��õ��������ɿ���������������ֱ��ǣ�
��_____________________
��Na2CO3��
��_____________________
��NaHCO3��
���ù�������ˮ���μӹ������ᣬ�ٽ���Һ���ɣ��õ������������___g
(5)��Na2CO3����ˮ�õ��������ݣ�
ˮ | Na2CO3 | ���ǰ�¶� | ��Ϻ��¶� |
35ml | 3.2g | 20 | 24.3 |
Na2CO3����ˮ______(����������������)�ȣ�����ܽ������ЧӦ�ĽǶȼ��Խ���_________
(6) Na2CO3��Һ�Լ��Ե�ԭ����(д���ӷ���ʽ) ___________ ��д������Һ�еĵ���غ����ʽ��_______
���𰸡�H+ + OH�� = H2O ��2H+ + CO32�� = H2O + CO2�� Na��S��Cl ǿ Cl2+H2S=S��+2HCl������������Ա����������ǿ(HCl���ȶ��Ա�H2Sǿ) NaOH��Na2CO3 Na2CO3��NaHCO3 5.85 �� Na2CO3����ˮʱ��ˮ�Ϲ��̷ų�������������ɢ�������յ����� CO3 2��+ H2O ![]() HCO3�� + OH�� [Na+]+[H+]=2[CO3 2��]+[HCO3��]+[OH��]
HCO3�� + OH�� [Na+]+[H+]=2[CO3 2��]+[HCO3��]+[OH��]
��������
(1)������Ժ���������֮�䷴Ӧ���������ơ�ˮ�������̼����֮�䷴Ӧ���������ơ�ˮ�Լ�������̼�����ӷ���ʽΪ��H++OH-=H2O��2H++CO32-=H2O+CO2����
(2))������������������λ�ڵ������ڵ�Ԫ�طֱ���Na��S��Cl��������ԭ�Ӱ뾶��С����ԭ�Ӱ뾶��С˳���ǣ�Na��S��Cl��
(3)�ȽϷǽ���Ԫ�صķǽ�����ǿ�����ɸ��ݵ���֮����û���Ӧ����Ӧ����������ˮ��������ԡ��⻯����ȶ��ԵȽǶ��жϣ����ݷ�ӦCl2+H2S=S��+2HCl������������Ա����������ǿ��HCl���ȶ��Ա�H2Sǿ����ʵ���Եõ��ȵķǽ����Ա���ǿ��
(4)��0.1molNaOH����Һ����һ����CO2�������ն�����̼��������ͨ�������̼��������ʱ���������ƹ���������Na2CO3�������ɵõ�NaOH��Na2CO3���ڵ�CO2��NaOH��Һǡ����ȫ��Ӧʱ��������Na2CO3���������ɵõ�Na2CO3���۵�CO2�Թ���ʱ�����벿��Na2CO3��Ӧ����NaHCO3���������ɵõ�Na2CO3��NaHCO3���ܵ�CO2��������ʱ��Na2CO3��ȫת��ΪNaHCO3���������ɵõ�NaHCO3������Һ�������ɵõ���������Ϊ��NaOH��Na2CO3��Na2CO3��Na2CO3��NaHCO3��NaHCO3��
����Na�غ㣬���ù�������ˮ���μӹ������ᣬ�ٽ���Һ���ɣ��õ������Ȼ���0.1mol��������5.85g��
(5)���ݱ������ݿ�֪̼��������ˮ���ȣ�Na2CO3����ˮʱ��ˮ�Ϲ��̷ų�������������ɢ�������յ�����������Na2CO3����ˮΪ���ȷ�Ӧ��
(6)̼����ˮ��Һ�д���̼�����ˮ��CO32��+H2O![]() HCO3��+OH����������Һ�Լ��ԣ���Һ�еĵ���غ�Ϊ[Na+]+[H+]=2[CO32��]+[HCO3��]+[OH��]��
HCO3��+OH����������Һ�Լ��ԣ���Һ�еĵ���غ�Ϊ[Na+]+[H+]=2[CO32��]+[HCO3��]+[OH��]��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijҩ��ϳ��м���F�Ʊ�·�����£�
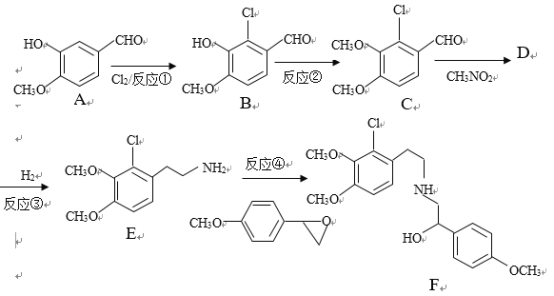
��֪��RCHO��R��CH2NO2![]()
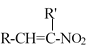 ��H2O
��H2O
(1)�л���A�ṹ�к��������ŵ�������__________________.
(2)��Ӧ���г�B�⣬����Ҫ�ķ�Ӧ��ͷ�Ӧ������___________________
(3)�л���D�Ľṹ��ʽΪ_____________________����Ӧ����1Ħ��D��Ҫ___Ħ��H2����ת��ΪE
(4)��Ӧ�ܵķ�Ӧ��![]() �ܶ���ͬ���칹�壬��д����������������һ��ͬ���칹��Ľṹ��ʽ_____________��
�ܶ���ͬ���칹�壬��д����������������һ��ͬ���칹��Ľṹ��ʽ_____________��
a.�ṹ�к�4�ֻ�ѧ������ͬ����ԭ��
b.�ܷ���������Ӧ
c.�ܺ�����������Һ��Ӧ
(5)��֪�������ϵ��Ȼ�Ϊ��λ��λ������![]()
![]()
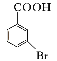 �����
��д����![]() Ϊԭ���Ʊ�
Ϊԭ���Ʊ�![]() �ĺϳ�·������ͼ(���Լ���ѡ)_____________��
�ĺϳ�·������ͼ(���Լ���ѡ)_____________��
![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ�ֳ���ˮ����������ʳ���������Ѹɣ�����֮�⣬���ѻ���������ơ�
(1)��������֭���������ǵķ����ǣ������мӼ�������ԣ��ټ������Ƶ�Cu(OH)2�����ȣ���������________��
(2)��������ƹ����У�������ת��Ϊ�ƾ��Ĺ������£�����������л�ѧ����ʽ��C6H12O6(������)![]() 2_________+ 2 C2H5OH
2_________+ 2 C2H5OH
(3)���Ѿ��ܷⴢ������л���������ζ�����࣬����Ҳ����ͨ����ѧʵ�����Ʊ���ʵ���ҿ�����ͼ��ʾװ���Ʊ�����������

���Թ�a���������������Ļ�ѧ����ʽ��__________��
���Թ�b��ʢ�ŵ��Լ��DZ���____________��Һ��
��ʵ�鿪ʼʱ���Թ�b�еĵ��ܲ�����Һ���µ�ԭ����________��
����Ҫ������Թ�b�е�������������Ҫ�õ���������_______(����ĸ)��
A.��ͨ©�� B.��Һ©�� C.����©��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ܹ�˵����ķǽ����Ա���������ʵ��
��![]() ������Ӧ����
������Ӧ����![]() ��S������Ӧ����FeS
��S������Ӧ����FeS
��![]() ��
��![]() �Ļ��������ǿ������ɾ��ҷ�Ӧ����S��
�Ļ��������ǿ������ɾ��ҷ�Ӧ����S��![]() ��Ӧ��ϸ��¶�
��Ӧ��ϸ��¶�
�۽�![]() ͨ���������п��û�����
ͨ���������п��û�����
�ܳ���ʱ����Ϊ��̬���ȵ���Ϊ��̬��
A.�٢�B.�٢ڢ�C.�ڢ�D.�٢ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�ΪԪ�����ڱ���һ���֡�
̼ | �� | Y | |
X | �� | Z |
����������
(1)��ԭ�ӵĵ����Ų�ʽΪ_________��ZԪ����Ԫ�����ڱ��е�λ��Ϊ______
(2)�ϱ���ԭ�Ӱ뾶����Ԫ����(дԪ�ط���) _____________����ԭ�ӵĺ������ռ��_____________���������___________���˶�״̬��
(3)������ʵ��˵��YԪ�صķǽ����Ա���Ԫ�صķǽ�����ǿ����______________
a.Y������H2S��Һ��Ӧ����Һ�����
b.��������ԭ��Ӧ�У�1moY���ʱ�1mol���ʵõ��Ӷ�
c.Y������Ԫ�ص���ͼ��⻯�����ȷֽ⣬ǰ�ߵķֽ��¶ȸ�
(4)X��Z��Ԫ�صĵ��ʷ�Ӧ����1molX�ĸۻ�����ָ������£�����687kJ����֪�û�������ۡ��е�ֱ�Ϊ-69���58�棬д����X�ĵ���ʽΪ______________�÷�Ӧ���Ȼ�ѧ����ʽ__________________
(5)����̼��ͬλ����һ��ԭ�ӵ���;___________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���̷���FeSO4��7H2O��������ȱ����ƶѪҩƷ����Ҫ�ɷ֡���������������м����������(Sn)�������������ʣ�Ϊԭ�����������̷���һ�ַ�����
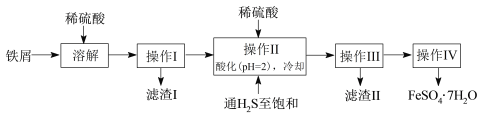
��֪�������±���H2S��Һ��pHԼΪ3.9��SnS������ȫʱ��Һ��pHΪ1.6��FeS��ʼ����ʱ��Һ��pHΪ3.0��������ȫʱ��pHΪ5.5��
(1)�ܽ�ʱ����ȣ�������_____________________________________(������)ʱӦֹͣ���ȣ������Ƚ��в���I��ԭ����______________________________________��
(2)����II�У�ͨ�����������͵�Ŀ����_______________________________������Һ���������ữ��pH= 2��Ŀ����_________________________________��
(3)����IV��˳������Ϊ��____________��____________��______________��
����IV�õ����̷�������������ˮϴ�ӣ���Ŀ���ǣ��ٳ�ȥ������渽�ŵ���������ʣ���_____________________________________________��
(4)�ⶨ�̷���Ʒ��Fe2+�����ķ����ǣ�a.��ȡ2.850g�̷���Ʒ���ܽ⣬��250 mL����ƿ�ж��ݣ�b.��ȡ25.00 mL������Һ����ƿ�У�c.�������ữ��0.01000 mol/L KMnO4��Һ�ζ����յ㣬����KMnO4��Һ�����ƽ��ֵΪ20.00 mL���ζ�ʱ������Ӧ�����ӷ���ʽΪ��5Fe2+��MnO4��8H+��5Fe3+��Mn2+��4H2O����
���жϴ˵ζ�ʵ��ﵽ�յ�ķ�����_________________________________��
�ڼ���������Ʒ��FeSO4��7H2O����������Ϊ_______����С����ʾ��������λС������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڳ����£�0.1000 mol/L Na2CO3��Һ25 mL��0.1000 mol/L����ζ�����ζ�������ͼ��
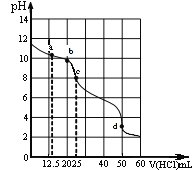
�Եζ�������������Һ���������Ũ�ȼ�Ĺ�ϵ�������й�˵����ȷ����
A.a�㣺c(CO32-)>c(HCO3-)>c(OH-)
B.b�㣺5c(Cl-)>4c(HCO3-)+4c(CO32-)
C.c�㣺c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
D.d�㣺c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������㷺�����ڶ�ֲ�����ڣ�����������������˵����ȷ���ǣ� ��
A.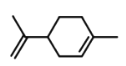 ��
��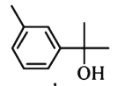 �����ڷ����廯����
�����ڷ����廯����
B. ��
��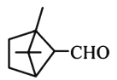 ����������̼ԭ�Ӿ�����ͬһƽ����
����������̼ԭ�Ӿ�����ͬһƽ����
C. ��
�� ��
�� ����ʹ����
����ʹ����![]() ��Һ��ɫ
��Һ��ɫ
D. ��
�� ���������Ƶ�
���������Ƶ�![]() ��Ӧ���ɺ�ɫ����
��Ӧ���ɺ�ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��������������ԭ�����͵��ǣ� ��
A.����2HI��g��![]() H2��g��+ I2��g������ƽ�����С���������ʹ��ϵ��ɫ����
H2��g��+ I2��g������ƽ�����С���������ʹ��ϵ��ɫ����
B.�ϳɰ���Ӧ��Ϊ��߰��IJ��ʣ�������Ӧ��ȡ�����¶ȵĴ�ʩ
C.ʵ��������FeCl3��Һʱ����FeCl3������뵽������Ũ�������ټ�ˮϡ��
D.�ñ���ʳ��ˮ����ȥ��Cl2�е�HCl
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com