
【题目】一种柔性水系锌电池为可充电电池,以锌盐溶液作为电解液,其原理如图所示。下列说法正确的是( )
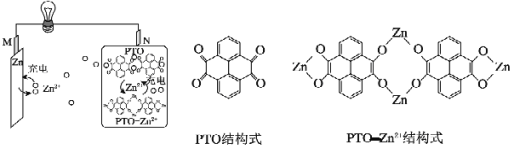
A.充电时,Zn2+向N极移动
B.充电时,N极的电极反应式为PTO—Zn2+-8e-= 2PTO + 4Zn2+
C.若维持电流强度为0.5A,放电10分钟,理论上消耗Zn的质量约为0.20g(已知F=96500C·mol-1)
D.放电时,每生成1mol PTO—Zn2+,M极溶解Zn的质量为65g
【答案】B
【解析】
柔性水系锌可充电电池工作原理为:放电时,金属Zn发生失电子的氧化反应生成Zn2+,即M电极为负极,则N电极为正极,电极反应式为2PTO+8e+4Zn2+═PTOZn2+;充电时,外加电源的正极连接原电池的正极N,外加电源的负极连接原电池的负极,阴阳极的电极反应与原电池的负正极的反应式相反,电解质中阳离子移向阴极、阴离子移向阳极,据此分析解答。
A.充电时,原电池的负极M连接外加电源的负极、作阴极,电解质中阳离子Zn2+移向阴极M,故A错误;
B.充电时,原电池的正极N连接外加电源的正极、作阳极,发生失电子的氧化反应,电极反应式为PTOZn2+8e=2PTO+4Zn2+,故B正确;
C.![]() ,
,![]() ,
,![]() ,
, ,理论上消耗Zn的质量约为
,理论上消耗Zn的质量约为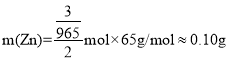 ,故C错误;
,故C错误;
D.放电时,正极反应式为2PTO+8e+4Zn2+═PTOZn2+,负极反应式为Zn2e=Zn2+,电子守恒有4Zn~PTOZn2+,所以每生成1molPTOZn2+,M极溶解Zn的质量=65g/mol×4mol=260g,故D错误;
故选:B。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】对于反应3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O,以下叙述正确的是( )
5NaCl+NaClO3+3H2O,以下叙述正确的是( )
A.Cl2是氧化剂,NaOH是还原剂
B.被氧化的氯原子和被还原的氯原子的物质的量之比为5∶1
C.Cl2既做氧化剂又做还原剂
D.氧化剂得电子数与还原剂失电子数之比为5∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法中正确的是( )
A.0.2 mol氧原子中含1.6NA个电子
B.1 mol 氯化镁中含有离子数为NA
C.12.4 g白磷中含有磷原子数为0.1NA
D.28 g一氧化碳气体所含的电子数为20NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用KMnO4氧化盐酸溶液,反应方程式如2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O,若产生的Cl2在标准状况下体积为56 L,计算:
(1)参加反应的HCl的物质的量________________
(2)反应中被氧化的HCl的物质的量__________________
(3)并用双线桥标出电子转移的方向和数目___________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下HClO的Ka=4.7×10-8,在c(H2SO3)+c(HSO![]() )+c(SO
)+c(SO![]() )=0.1mol·L-1的H2SO3和NaOH混合溶液中含硫微粒的物质的量分数ɑ随pH的变化曲线如图所示。下列叙述正确的是( )
)=0.1mol·L-1的H2SO3和NaOH混合溶液中含硫微粒的物质的量分数ɑ随pH的变化曲线如图所示。下列叙述正确的是( )
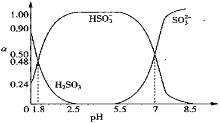
A.pH=7.2时,混合溶液中由水电离的c(H+)=10-7.2
B.等浓度的Na2SO3溶液pH比NaClO溶液的大
C.将等浓度、等体积的NaClO和Na2SO3溶液混合,混合液接近中性
D.Na2SO3溶液中:c(Na+)=2c(SO![]() )+c(HSO
)+c(HSO![]() )+c(H2SO3)
)+c(H2SO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t ℃时,pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下,1体积的稀硫酸和10体积的NaOH溶液混合后溶液呈中性,则稀硫酸的pH(pHa)与NaOH溶液的pH(pHb)的关系是( )
A.pHa+pHb=12B.pHa+pHb=13C.pHa+pHb=14D.pHa+pHb=15
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向25ml氢氧化钠标准溶液中逐滴加入0.2mol·L1的一元酸HA溶液,PH变化曲线如下图所示:
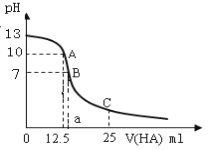
(1)该氢氧化钠溶液的物质的量浓度为__________mol·L1。
(2)A点对应酸的体积为12.5ml,则所得混合溶液中由水电离出的c(OH)= _______mol·L1。
(3)HA是____酸(选填“强”、“弱”)。
(4) 在B点所得混合溶液中,c(Na+)、c(A)、c(H+)、c(OH) 的大小的顺序是_____________。
(5)在C点所得混合溶液中,下列说正确的是________。
A.HA的电离程度小于NaA的水解程度
B.离子浓度由大到小的顺序是c(Na+)>c(A)>c(H+)>c(OH)
C.c(Na+) + c(H+) = c(A-) + c(OH)
D.c(HA) + c(A) = 0.2mol·L1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温下,甲、乙两种溶液体积都为1L,甲中溶有0.1molCH3COOH,乙中溶有0.1molHCl和0.1molCH3COOH,测得甲溶液中c(CH3COO-)=a molL-1,乙溶液中c(CH3COO-)=b molL-1,分别用含a、b的代数式表示醋酸的电离平衡常数___、___。(忽略水的电离)两溶液中CH3COOH的电离平衡常数甲__乙(填“>”“<”“=”,下同);两溶液中CH3COOH的电离度甲___乙;a和b的值:a___b。
(2)已知 常温下CH3COOH的电离平衡常数Ka=1.8×10-5,在0.1mol/L的CH3COOH溶液中加入NaOH溶液,当溶液中c(CH3COO-) =c(CH3COOH)时,该溶液pH=___(可用对数形式表示),当溶液的pH =7时,c(CH3COO-)/c(CH3COOH)=___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com