
【题目】镁和铝分别与等浓度等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)的关系如图所示,则下列关于反应中镁和铝的叙述正确的是
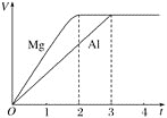
A. 二者物质的量之比为3∶2
B. 二者质量之比为3∶2
C. 二者摩尔质量之比为2∶3
D. 二者消耗H2SO4的物质的量之比为2∶3
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】如图为氟利昂(如CFCl3)破坏臭氧层的反应过程示意图,下列说法不正确的是
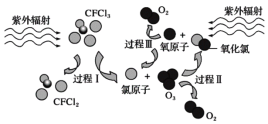
A.过程Ⅰ中断裂极性键C—Cl键
B.过程Ⅲ中O+O == O2是吸热过程
C.过程Ⅱ可表示为O3+Cl==ClO+O2
D.上述过程说明氟利昂中氯原子是破坏O3的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,对于密闭容器中进行的可逆反应:N2(g) + 3 H2(g) ![]() 2NH3(g)。下列说法中,表明这一反应已经达到化学平衡状态的是( )
2NH3(g)。下列说法中,表明这一反应已经达到化学平衡状态的是( )
A.N2、H2、NH3的浓度不再变化
B.N2、H2、NH3的浓度相等
C.N2、H2、NH3在密闭容器中共存
D.反应停止,正、逆反应速率都等于零
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物K是有机光电材料中间体。由芳香族化合物A制备K的合成路线如下:
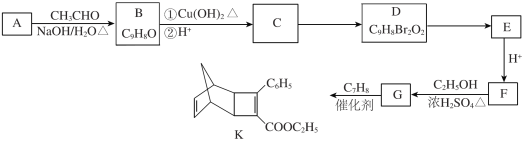
已知:![]()
![]()
回答下列问题:
(1)A的结构简式是________。
(2)C中官能团是________。
(3)D→E的反应类型是________。
(4)由F生成G的化学方程式是________。
(5)C7H8的结构简式是________。
(6)芳香族化合物X是G的同分异构体,该分子中除苯环外,不含其他环状结构,其苯环上只有1种化学环境的氢。X能与饱和碳酸氢钠溶液反应放出CO2,写出符合上述要求的X的结构简式:________。
(7)以环戊烷和烃Q为原料经四步反应制备化合物![]() ,写出有关物质的结构简式(其他无机试剂任选)。
,写出有关物质的结构简式(其他无机试剂任选)。![]() Q:____;中间产物1:________;中间产物2:____;中间产物3:________。
Q:____;中间产物1:________;中间产物2:____;中间产物3:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LiCoO2(钴酸锂)是锂离子电池的正极材料。以某海水为原料制备钴酸锂的一种流程如下:
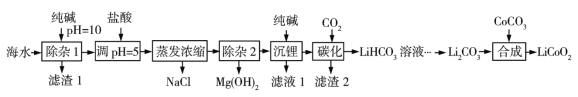
已知如下信息:①该海水中含浓度较大的LiCl,含少量MgCl2、CaCl2、MnCl2等。
②碳酸锂的溶解度与温度关系如图所示。
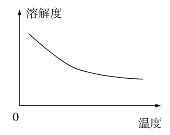
③常温下,几种难溶物质的溶度积数据如下:
物质 | Li2CO3 | MgCO3 | CaCO3 | MnCO3 | Mg(OH)2 |
Ksp | 2.5×102 | 6.8×106 | 2.8×109 | 2.3×1011 | 6.0×1010 |
请回答下列问题:
(1)LiCoO2中钴的化合价为____________ ,滤渣1主要成分有MgCO3、Mg(OH)2、CaCO3和____________________(填化学式)。
(2)调pH=5的目的是________________________。
(3) “沉锂”包括过滤、洗涤等,宜用_____________(填“热水”或“冷水”)洗涤Li2CO3。加入纯碱的量与锂回收率的关系如表所示:
序号 | n(Na2CO3)/n(LiCl) | 沉淀质量/g | 碳酸锂含量/% | 锂回收率/% |
① | 0.9∶1 | 10.09 | 92.36 | 77.67 |
② | 1.0∶1 | 0.97 | 90.19 | 82.46 |
③ | 1.1∶1 | 11.45 | 89.37 | 85.27 |
④ | 1.2∶1 | 12.14 | 84.82 | 85.45 |
从生产成本考虑,宜选择_______________(填序号)方案投料。
(4) “除杂2”中调pH=13时c(Mg2)=_______________mol·L1。
(5) “合成”中采用高温条件,放出一种能使澄清石灰水变浑浊的气体。写出“合成”发生反应的化学方程式_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体![]() 血液的pH需控制在7.35~7.45之间,过高过低都会引起身体不适,甚至危及生命。人体血液能维持在稳定的pH范围主要是人血浆中一定浓度的
血液的pH需控制在7.35~7.45之间,过高过低都会引起身体不适,甚至危及生命。人体血液能维持在稳定的pH范围主要是人血浆中一定浓度的![]() 和
和![]() 起调节作用。按要求回答下列问题。
起调节作用。按要求回答下列问题。
(1)用离子方程式解释血液呈弱碱性的原因____;
(2)当血液的![]() (即
(即![]() 浓度为
浓度为![]() )时,
)时,![]() 和
和![]() 浓度比值约为20:1,计算出此时碳酸的
浓度比值约为20:1,计算出此时碳酸的![]() 7.96×10-7,查阅资料得常温下碳酸的
7.96×10-7,查阅资料得常温下碳酸的![]() ,解释与计算所得数据存在差异的原因____。
,解释与计算所得数据存在差异的原因____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将2 mol SO2和1 mol O2充入一固定容积的密闭容器中,在催化剂作用下发生如下反应:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH=-197 kJ·mol-1,当达到化学平衡时,下列说法中正确的是
2SO3(g) ΔH=-197 kJ·mol-1,当达到化学平衡时,下列说法中正确的是
A.SO2和SO3共2 mol
B.生成SO3 2 mol
C.放出197 kJ热量
D.含氧原子共12 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Fe(s)+CO2(g) ![]() FeO(s)+CO(g) △H=akJ/mol,平衡常数为K;测得在不同温度下,K值如下:
FeO(s)+CO(g) △H=akJ/mol,平衡常数为K;测得在不同温度下,K值如下:
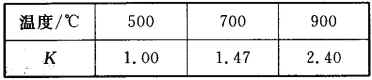
(1)若500℃时进行上述反应,CO2起始浓度为1 mol/L,CO的平衡浓度为_____。
(2)方程式中的a________0(填“大于”“小于”或“等于”)。
(3)900℃上述反应达到平衡,要使得该平衡向左移动,其他条件不变时,可以采取的措施有________(填序号)
A.缩小反应器体积 B.加入FeO
C.降低温度到500℃ D.使用合适的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型冠状病毒具有较强的传染性,中科院发现大约有三十种药物可能对新型冠状病毒有效,其中山豆根等中药材中含有的黄酮类化合物可能对新型冠状肺炎有治疗作用。某黄酮类化合物G的合成路线如下图所示,分子中Ar表示芳香基。
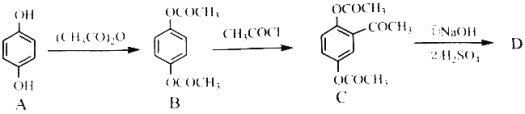
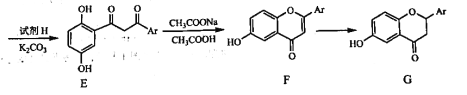
已知:![]()
回答下列问题:
(1)有机物A的名称为_________,A转化为B的目的是_________。C中含有的官能团的名称为_________。
(2)D转化为E的化学方程式为___________________________。E到F的转化率大约为78.6%,原因是易生成副产物X(分子中含有一个七元环),则X的结构简式为__________________,则此过程中涉及的反应的类型为__________________。
(3)某芳香族化合物K与D互为同分异构体,则符合下列条件的K的结构共有_________种。
(已知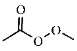 结构具有较强的氧化性,与还原性原子团不能共存)
结构具有较强的氧化性,与还原性原子团不能共存)
①与![]() 不发生显色反应 ②可发生水解反应和银镜反应
不发生显色反应 ②可发生水解反应和银镜反应
(4)请以丙酮(![]() )和
)和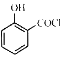 为原料,参照题中所给信息(其他试剂任选),设计合成
为原料,参照题中所给信息(其他试剂任选),设计合成![]() 的路线_____________________________________________________。
的路线_____________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com