
【题目】二氧化硫和氮氧化物都是常见的大气污染物,回答下列相关问题。
Ⅰ.某温度下氮氧化物与悬浮在大气中的海盐粒子相互作用时,涉及如下反应:
i. 2NO(g)+Cl2(g)![]() 2ClNO(g) △H1<0其平衡常数为K1
2ClNO(g) △H1<0其平衡常数为K1
ii. 2NO2(g)+NaCl(s) ![]() NaNO3(s)+ClNO(g) △H2<0 其平衡常数为K2
NaNO3(s)+ClNO(g) △H2<0 其平衡常数为K2
(1)现有反应4NO2(g)+2NaCl(s) ![]() 2NaNO3(s)+2NO(g)+Cl2(g), 则此反应的平衡常数K3=_______(用K1、K2表示),反应热△H3=_____(用△H1、△H2表示)。
2NaNO3(s)+2NO(g)+Cl2(g), 则此反应的平衡常数K3=_______(用K1、K2表示),反应热△H3=_____(用△H1、△H2表示)。
(2)为研究不同条件对反应ii的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO2和足够的NaCl(s),10min时反应ii达到平衡。测得平衡时NO2的转化率α1(NO2) =50%,则:10min内υ(ClNO) =___________________,平衡常数K2=_________________;
II.除氮氧化物外,SO2也是重要的大气污染物,需要对其进行吸收处理。
(3)若用一定量的NaOH溶液吸收SO2气体后所得吸收液恰好呈中性,下列有关吸收液中粒子关系正确的是______________。
A.c(Na+) = c(HSO3-)+ 2c(SO32-)
B.c(Na+) > c(HSO3-) =c(SO32-) > c(H+) = c(OH—)
C.2c(Na+) =3c(H2SO3)+3c(HSO3-)+3c(SO32-)
D.c(Na+) > c(HSO3—) + c(SO32—) +c(H2SO3)
(4)工业上也可以用Na2SO3溶液吸收SO2,并用电解法处理吸收后所得溶液以实现吸收液的回收再利用,装置如图所示,则

①工作一段时间后,阴极区溶液的pH______(填“增大”“减小”或“不变”);
②写出阳极的电极反应式_______________________。
【答案】![]() 2H2-H1 或-(H1-2H2) 2.5×10-3mol·L-1·min-1 10 L/mol AD 增大 HSO3--2e-+H2O=SO42-+3H+
2H2-H1 或-(H1-2H2) 2.5×10-3mol·L-1·min-1 10 L/mol AD 增大 HSO3--2e-+H2O=SO42-+3H+
【解析】
Ⅰ.(1)由i.2NO(g)+Cl2(g)2ClNO(g),ii.2NO2(g)+NaCl(s)NaNO3(s)+ClNO(g),结合盖斯定律可知②×2-①可得:4NO2(g)+2NaCl(s)2NaNO3(s)+2NO(g)+Cl2(g);
(2)10min时反应 ii达到平衡,测得平衡时NO2的转化率α1(NO2)=50%,则:
2NO2(g)+NaCl(s)NaNO3(s)+ClNO(g)
开始 0.2 0
转化 0.1 0.05
平衡 0.1 0.05
结合v=![]() 及K为生成物浓度幂之积与反应物浓度幂之积的比计算;
及K为生成物浓度幂之积与反应物浓度幂之积的比计算;
II.除氮氧化物外,SO2也是重要的大气污染物,需要对其进行吸收处理。
(3)常温下,用一定量的NaOH溶液吸收逸出的SO2气体,吸收后的吸收液恰好呈中性,c(H+)=c(OH-),结合溶液中的电荷守恒、元素守恒、电离平衡常数分析判断;
(4)①阴极区是溶液中的氢离子放电;
②由装置图可知,右边为亚硫酸根失电子易被氧化为硫酸根,为阳极。
Ⅰ.(1)由i.2NO(g)+Cl2(g)2ClNO(g),ii.2NO2(g)+NaCl(s)NaNO3(s)+ClNO(g),结合盖斯定律可知②×2-①可得:4NO2(g)+2NaCl(s)2NaNO3(s)+2NO(g)+Cl2(g),则此反应的平衡常数K3=![]() ,反应热△H3=2H2-H1;
,反应热△H3=2H2-H1;
(2)10min时反应 ii达到平衡,测得平衡时NO2的转化率α1(NO2)=50%,则:
2NO2(g)+NaCl(s)NaNO3(s)+ClNO(g)
开始 0.2 0
转化 0.1 0.05
平衡 0.1 0.05
则:10min内υ(ClNO) = =2.5×10-3molL-1min-1,平衡常数K2=
=2.5×10-3molL-1min-1,平衡常数K2=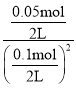 =10L/mol;
=10L/mol;
II.除氮氧化物外,SO2也是重要的大气污染物,需要对其进行吸收处理。
(3)常温下,用一定量的NaOH溶液吸收逸出的SO2气体,吸收后的吸收液恰好呈中性,c(H+)=c(OH-);
A.依据溶液中电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HSO3-)+2c(SO32-),得到c(Na+)=c(HSO3-)+2c(SO32-),故A正确;
B.若c(HSO3-)=c(SO32-),溶液呈酸性c(H+)>c(OH-),故B错误;
C.亚硫酸氢钠和亚硫酸钠按照1:1混合,溶液呈碱性,溶液中物料守恒为2c(Na+)=3c(H2SO3)+3c(HSO3-)+3c(SO32-),但溶液呈中性,亚硫酸氢钠和亚硫酸钠物质的量不相同,故C错误;
D.依据化学式可知,亚硫酸氢钠中硫元素物质的量和钠的物质的量相同,亚硫酸钠中钠离子大于亚硫酸根中硫元素,所以c(Na+)>c(HSO3-)+c(SO32-)+c(H2SO3),故D正确;
故答案为AD;
(4)①电解池中,阴极区是溶液中的氢离子放电,电极反应式为:2H++2e-=H2↑,则pH增大;
②由装置图可知,右边为亚硫酸根失电子易被氧化为硫酸根,为阳极,则电极反应式为HSO3--2e-+2H2O═SO42-+3H+。


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
【题目】分别按下图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中A为电流表。请回答下列问题:

(1)以下叙述中,正确的是_______________(填字母)。
A.甲中锌片是负极,乙中铜片是正极
B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大
D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu
F.乙溶液中![]() 向铜片方向移动
向铜片方向移动
(2)变化过程中能量转化的主要形式:甲为___________;乙为______。
(3)在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是___。
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,请写出铜电极的电极反应方程式及总反应离子方程式:铜电极:____,总反应:___。当电路中转移0.25 mol电子时,消耗负极材料的质量为_____g(Zn的相对原子质量65)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正确的是
现象 | 解释 | |
A | 用洁净的铂丝蘸取某溶液进行焰色反应,火焰呈黄色 | 该溶液中一定含有 |
B |
|
|
C | 某溶液中先加入稀盐酸无现象,再加入氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有 |
D | 铁加入稀硝酸中有气泡产生 | 铁与稀硝酸发生了置换反应 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解足量下列溶液一段时间后,再加入一定量括号内的纯净物,能使溶液恢复到原来的成分和浓度的是
A. AgNO3[AgNO3] B. NaOH[NaOH] C. KCl[H2O] D. CuSO4[CuO]
【答案】D
【解析】石墨电极为惰性电极,溶液中阳离子在阴极放电,阴离子在阳极放电。A、电解AgNO3溶液,Ag+在阴极放电生成Ag,OH-在阳极放电生成O2,且n(Ag)∶n(O2)=2∶1,则应加入Ag2O恢复浓度,故A错误;B、电解NaOH溶液,H+在阴极放电生成H2,OH-在阳极放电生成O2,且n(H2)∶n(O2)=2∶1,则应加入一定量的H2O恢复原样,故B错误;C、电解KCl溶液,H+在阴极放电生成H2,Cl-在阳极放电生成Cl2,且n(H2)∶n(Cl2)=1∶1,则应加入一定量HCl恢复原样,故C错误;D、电解CuSO4溶液,Cu2+在阴极放电生成Cu,OH-在阳极放电生成O2,且n(Cu)∶n(O2)=2∶1,则应加入一定量CuO恢复原样,故D正确。故选D。
点睛:分析电解反应的原理,在两极析出什么物质(固体或气体),相当于什么物质脱离反应体系,根据元素守恒和原子比例,加入对应的物质,即可使溶液完全复原。
【题型】单选题
【结束】
28
【题目】工业上用电解法处理含镍酸性废水并得到单质Ni的原理如图所示。下列说法不正确的是

已知:①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
A. 碳棒上发生的电极反应:4OH--4e-=O2↑+2H2O
B. 电解过程中,B中NaCl溶液的物质的量浓度将不断减少
C. 为了提高Ni的产率,电解过程中需要控制废水pH
D. 若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:pOH=﹣lgc(OH﹣),298K时,向20.00 mL 0.10 molL﹣1氨水中滴入0.10 molL﹣1的盐酸,溶液的pH和pOH与加入盐酸体积关系如图所示.下列说法正确的是( )

A.曲线PJN表示溶液中pH的变化
B.M点水的电离程度比J点大
C.M、P两点的数值之和a+b=14
D.pH与pOH交叉点J对应的V(盐酸)=20.00 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,能得出相应实验结论的是( )
选项 | ① | ② | ③ | 实验结论 |
|
A | 浓盐酸 | MnO2 | NaBr溶液 | 氧化性Cl2>Br2 | |
B | 浓氨水 | 碱石灰 | AgNO3溶液 | AgOH具有两性 | |
C | 浓硫酸 | Na2SO3 | FeCl3溶液 | SO2具有还原性 | |
D | 稀盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:Cl>C>Si |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[实验化学]
焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂,在空气中、受热时均易分解。实验室制备少量Na2S2O5的方法:在不断搅拌下,控制反应温度在40℃左右,向Na2CO3过饱和溶液中通入SO2,实验装置如下图所示。

当溶液pH约为4时,停止反应,在20℃左右静置结晶。生成Na2S2O5的化学方程式为
2NaHSO3===Na2S2O5+H2O
(1)SO2与Na2CO3溶液反应生成NaHSO3和CO2,其离子方程式为____________________。
(2)装置Y的作用是______________________________。
(3)析出固体的反应液经减压抽滤、洗涤、25℃~30℃干燥,可获得Na2S2O5固体。
①组成减压抽滤装置的主要仪器是布氏漏斗、________________和抽气泵。
②依次用饱和SO2水溶液、无水乙醇洗涤Na2S2O5固体。用饱和SO2水溶液洗涤的目的是______。
(4)实验制得的Na2S2O5固体中含有一定量的Na2SO3和Na2SO4,其可能的原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(化学——选修3:物质结构与性质)
钴及其化合物在生产中有重要作用,回答下列问题
(1)钴元素基态原子的电子排布式为________________,未成对电子数为________________。
(2)配合物[Co(NH3)4(H2O)2]Cl3是钴重要化合物
①H2O的沸点___ (填“高于”或“低于”)H2S,原因是_______;H2O中O的杂化形式为_____。H2O是_____分子(填“极性”或“非极性”)。
②[Co(NH3)4(H2O)2]Cl3中的Co3+配位数为___。阳离子的立体构型是___________。[Co(NH3)4(H2O)2]Cl3若其中有两个NH3分子被Cl取代,所形成的[Co(NH3)2Cl2(H2O)2]3+的几何异构体种数有(不考虑光学异构)___________种。
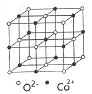
(3)一氧化钴的晶胞如图,则在每个Co2+的周围与它最接近的且距离相等的Co2+共有_____个,若晶体中Co2+与O2-的最小距离为acm,则CoO的晶体密度为_______(用含NA和a的代数式表示。结果g/cm3,已知:M(Co)=59g/mol;M(O)=16g/mol,设阿伏加德罗常数为NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了如图所示元素周期表,已知Z元素的最外层电子数是次外层的3倍。空格中均有对应的元素填充。下列说法正确的是
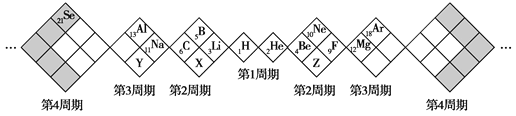
A.白格中都是主族元素,灰格中都是副族元素
B.X、Y分别与Z形成的化合物都只有两种
C.X、Y元素最高价氧化物对应的水化物酸性:X>Y
D.X、Y、Z的气态氢化物中最稳定的是X的氢化物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com