
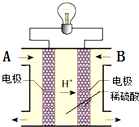
 为解决环境、能源等问题,科学家正研究将CO2转化为CH3OH技术. 该转化反应为CO2+3H2=CH3OH+H2O.
为解决环境、能源等问题,科学家正研究将CO2转化为CH3OH技术. 该转化反应为CO2+3H2=CH3OH+H2O.| 1 |
| 2 |
| 1 |
| 2 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 50 |
| 29 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
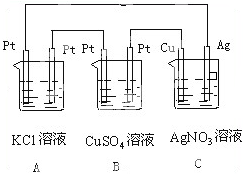 如图所示,若反应一段时间,5min时铜电极质量增加1.08g,试回答:
如图所示,若反应一段时间,5min时铜电极质量增加1.08g,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:
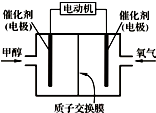 甲醇(CH3OH)燃料电池可用作电动汽车电源,如图为电池示意图.在电池的一极通入甲醇,另一极通入氧气,工作时H+由负极移向正极.下列叙述不正确的是( )
甲醇(CH3OH)燃料电池可用作电动汽车电源,如图为电池示意图.在电池的一极通入甲醇,另一极通入氧气,工作时H+由负极移向正极.下列叙述不正确的是( )| A、外电路通过0.6 mol电子时,理论上消耗甲醇3.2 g |
| B、通甲醇一端为负极 |
| C、正极反应为:O2+4H++4e-=2H2O |
| D、负极反应为:CH3OH+H2O+6e-=CO2↑+6H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某钾盐K2A 的水溶液显碱性,其原因是:A2-+2H2O?H2A+2OH- | ||||||
| B、在30mL 1mol?L-1的Na2SO3溶液中通入标准状况下的Cl2 224mL:H2O+3SO32-+Cl2═SO42-+2HSO3-+2Cl- | ||||||
C、碳酸氢铵溶液与足量的NaOH溶液混合加热:NH
| ||||||
D、在Ba(HCO3)2溶液中逐滴滴入NaHSO4 溶液至Ba2+恰好完全沉淀时:Ba2++2HCO
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com