
【题目】化合物I(4-对羟基苯基-2-丁酮)是国际公认的既安全又获广泛应用的合成香料。由化合物A制备I的一种合成路线如下:

回答下列问题:
(1)A的化学名称为________________。
(2)B中的官能团名称是_________________。
(3)F的结构简式为_______________。
(4)⑤的反应类型是________________。
(5)写出满足下列条件的G的同分异构体的结构简式:______________。
i.属于芳香族化合物;
ii.既能发生银镜反应,又能发生水解反应;
iii.核磁共振氢谱为三组峰,峰面积比为6︰2︰1。
(6)设计由氯乙烷和丙二酸制备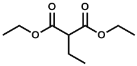 的合成路线:______(无机试剂任选)。
的合成路线:______(无机试剂任选)。
【答案】对甲基苯酚 (酚)羟基、醛基 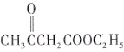 取代反应
取代反应 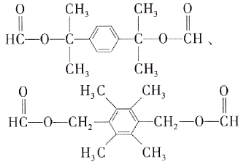
【解析】
![]() 中-CH3被氧化成-CHO,得到
中-CH3被氧化成-CHO,得到![]() ,酚-OH经过硫酸二甲酯甲基化,得到
,酚-OH经过硫酸二甲酯甲基化,得到![]() ,-CHO经NaBH4还原,得到
,-CHO经NaBH4还原,得到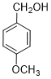 ,由化合物G可反推出F是
,由化合物G可反推出F是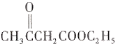 ,从而反推出E是
,从而反推出E是![]() ,化合物G通过NaOH、HCl脱去-COOC2H5,得到
,化合物G通过NaOH、HCl脱去-COOC2H5,得到 ,最后经过HBr和HOAc反应,得到
,最后经过HBr和HOAc反应,得到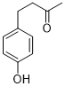 。
。
(1)A的化学名称为对甲基苯酚。
(2)B中的官能团名称是酚羟基和醛基。
(3)由D的结构简式及E的分子式可知E为![]() ,再结合G的结构简式及F的分子式可知,F的结构简式为
,再结合G的结构简式及F的分子式可知,F的结构简式为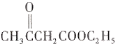 。
。
(4)由E、F、G的结构简式可知是F中的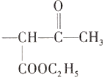 ,取代了E中的Cl,则反应类型是取代反应。
,取代了E中的Cl,则反应类型是取代反应。
(5)属于芳香族化合物,说明其分子中含有苯环;能发生银镜反应和水解反应且核磁共振氢谱为三组峰,峰面积比为6︰2︰1,说明该分子中有3种不同环境的氢,并且个数比为6︰2︰1,且该分子中含有的既能发生银镜反应又能发生水解反应的基团为HCOO—,则符合条件的同分异构体的结构简式有:
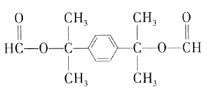 和
和 。
。
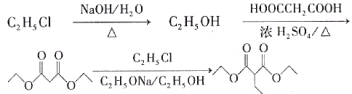
(6)由氯乙烷和丙二酸制备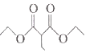 的合成路线为:
的合成路线为:
 。
。


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
【题目】尿素在生产生活中应用非常广泛,2NH3(g)+CO2(g)CO(NH2)2(s)+H2O(l)是工业上合成氮肥尿素的主要方法,在生产条件下,单位时间内获得尿素的产量与压强及n(NH3):n(CO2)的关 系如图甲所示。当氨碳比n(NH3):n(CO2)=4 时,CO2的转化率随时间的变化关系如图乙所示。下列说法不正确的是

A.生产过程中n(NH3):n(CO2)的 最佳配比为2:1
B.若开始投料按照n(NH3):n(CO2)为2:1投料,平衡后若压缩容器的体积,则再次平衡时c(NH3)比压缩前小
C.A点的逆反应速率小于B点的正反应速率
D.由图乙可知NH3的平衡转化率为30%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锆石(ZrSiO4)酷似钻石且价格低廉,是钻石很好的代用品。天然锆石的主要成分是ZrSiO4,另外还常含有Fe、Al、Cu的氧化物杂质。工业上以天然锆石为原料制备ZrO2的工艺流程如下:
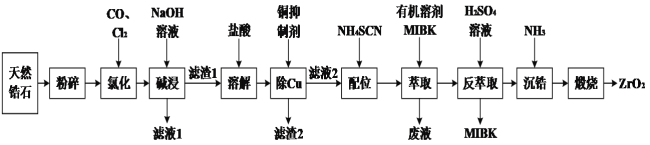
已知:i.氯化过程中除C、O外,其他元素均转化为其最高价氯化物;
ⅱ.Zr在化合物中通常显+4价;ZrC14易溶于水,400 ℃时升华;
ⅲ.“配合”生成的Fe(SCN)3难溶于MIBK,Zr(SCN)4在水中的溶解度小于在MIBK中的溶解度。
(1)将锆石“粉碎”的目的是_______________________________。
(2)“氯化”过程中,ZrSiO4发生反应的化学方程式为_______________,由下图可知,“氯化”过程选择的最佳反应条件是_________ ;若“氯化”温度过高会导致ZrC14产率降低,原因是________。
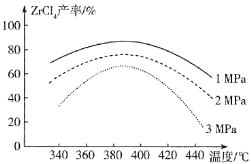
(3)常用的铜抑制剂为NaCN,它可与重金属离子生成沉淀,如Cu(CN)2,其Ksp=4.0×10-10。已知盐酸溶解后的溶液中Cu2+的浓度为1mol·L-1,若溶液中Cu2+的浓度小于等于1.0×10-6mol·L-1时可视为沉淀完全,则Cu2+沉淀完全时溶液中CN-的浓度为________molL-1。
(4)由于NaCN有剧毒,所以需要对“废液”中的NaCN进行处理,通常选用漂白液(有效成分是NaClO)在碱性条件下将其氧化,其产物之一是空气中的主要成分,则上述反应的离子方程式为___________。
(5)流程中“萃取”与“反萃取”可以分离铁、富集锆,简述“萃取”的原理:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不具有因果关系的是( )
A. 明矾溶于水后生成氢氧化铝胶体,因此具有净水能力
B. 纯碱水溶液呈碱性,因此可以去油污
C. 二氧化硅与氢氧化钠溶液反应生成硅酸钠,因此装氢氧化钠溶液的试剂瓶不能用玻璃塞
D. ![]() 具有漂白性,因此能使酸性高锰酸钾溶液褪色
具有漂白性,因此能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分类法在化学学习中起到了重要的作用。已知下列物质:①NaOH溶液、②NO2、③Fe(OH)3、④熔融NaCl、⑤SO2、⑥氨水。回答下列相关问题:
(1)属于混合物的有______________________(填序号,下同)。
(2)属于电解质的有_________________。
(3)能导电的有_____________________。
(4)实验室制备少量Fe(OH)3胶体的离子方程式是_____。
(5)实验室用NaOH溶液吸收NO2的化学方程式为2NO+2NaOH=NaNO2+ NaNO3+H2O,则该反应中氧化剂与还原剂的物质的量之比为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种红棕色金属氧化物,B、G是金属单质,F是一种难溶于水的白色化合物,受热后容易发生分解。
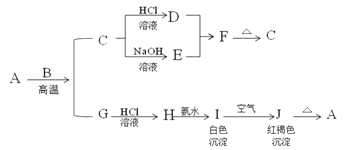
(1)写出下列物质的化学式:A:___ E:___ F:___ H:__。
(2)按要求写方程式:
①H与氨水反应的离子方程式:___。
②B与氢氧化钠溶液反应的离子方程式:___。
③I在空气中转化为J的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是 ( )
A. 2 mol H2O的摩尔质量和1 mol H2O的摩尔质量
B. 200 mL 1 mol·L-1氯化钙溶液中c(Cl-)和100 mL 2 mol·L-1氯化钾溶液中c(Cl-)
C. 64 g二氧化硫中氧原子数和标准状况下22.4 L一氧化碳中氧原子数
D. 20% NaOH溶液中NaOH的物质的量浓度和10% NaOH溶液中NaOH的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤燃烧排放的烟气含有SO2和NOx,是大气的重要污染源之一。用Ca(ClO)2溶液对烟气[n(SO2) ∶n(NO) =3∶2]同时脱硫脱硝(分别生成SO42-、NO3-),得到NO、SO2脱除率如下图,下列说法不正确的是

A.脱除NO的反应:2NO+3ClO-+H2O=2H++2NO3- +3Cl-
B.SO2脱除率高于NO的原因可能是SO2在水中的溶解度大于NO
C.依据图中信息,在80 min时,吸收液中n(NO3-)∶n(Cl-)=2∶3
D.随着脱除反应的进行,吸收剂溶液的pH逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验发现,298 K时,在氯化铁酸性溶液中加少量锌粒后,Fe3+立即被还原成Fe2+。某夏令营兴趣小组根据该实验事实设计了如图所示原电池装置。下列有关说法正确的是

A. 该原电池的正极反应是:Zn-2e-=Zn2+
B. 左烧杯中溶液的红色逐渐褪去
C. 该电池铂电极上立即有气泡出现
D. 该电池总反应为:3Zn+2Fe3+=2Fe+3Zn2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com