
【题目】分类法在化学学习中起到了重要的作用。已知下列物质:①NaOH溶液、②NO2、③Fe(OH)3、④熔融NaCl、⑤SO2、⑥氨水。回答下列相关问题:
(1)属于混合物的有______________________(填序号,下同)。
(2)属于电解质的有_________________。
(3)能导电的有_____________________。
(4)实验室制备少量Fe(OH)3胶体的离子方程式是_____。
(5)实验室用NaOH溶液吸收NO2的化学方程式为2NO+2NaOH=NaNO2+ NaNO3+H2O,则该反应中氧化剂与还原剂的物质的量之比为______________________。
【答案】①⑥ ③④ ①④⑥ Fe3++3H2O![]() FeOH)3(胶体)+3H+ 1:1
FeOH)3(胶体)+3H+ 1:1
【解析】
①NaOH溶液是混合物,既不是电解质也不是非电解质,能导电;②NO2是非金属氧化物,是非电解质,不能导电;③Fe(OH)3是碱,属于电解质,固态不能导电;④NaCl是盐,属于电解质,熔融状态下可以导电;⑤SO2非金属氧化物,是非电解质,不能导电;⑥氨水是混合物,既不是电解质也不是非电解质,能导电。
(1)由分析可知,属于混合物的有①⑥;
(2)由分析可知,属于电解质的有③④;
(3)由分析可知,能导电的有①④⑥;
(4)实验时将饱和氯化铁溶液滴加到沸水中制备氢氧化铁胶体,离子方程式为:Fe3++3H2O ![]() FeOH)3(胶体)+3H+;
FeOH)3(胶体)+3H+;
(5)反应2NO+2NaOH=NaNO2+ NaNO3+H2O中,NO既是氧化剂又是还原剂,一半是氧化剂,生成1个NaNO2;一半是还原剂,生成1个NaNO3,因此氧化剂与还原剂的物质的量之比为1:1。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】25℃时,下列各组离子在指定溶液中能大量共存的是 ( )
A. 在无色溶液中: Na+ 、Fe3+、NO3- 、Cl-
B. pH=11的透明溶液中:Na+、K+、MnO4-、CO32-
C. 在含有HCO3-的溶液中:H+、K+、SO42-、Cl-
D. 含有大量Fe2+的溶液中:H+、K+、SO![]() 、NO
、NO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:
2NH3(g)+NO(g)+NO2(g) ![]() 2N2(g)+3H2O
2N2(g)+3H2O![]()
在恒容的密闭容器中,下列有关说法正确的是
A. 平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
B. 平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小
C. 单位时间内消耗NO和N2的物质的量比为1:2时,反应达到平衡
D. 其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向100mL饱和的H2S溶液中通入SO2气体(气体体积换算成标准状况),发生反应:2H2S+SO2=3S↓+2H2O,测得溶液pH与通入SO2的关系如图所示。下列有关说法正确的是
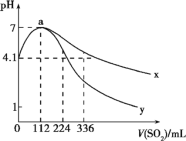
A.整个过程中,水的电离程度逐渐增大
B.该温度下H2S的Ka1数量级为10-7
C.曲线y代表继续通入SO2气体后溶液pH的变化
D.a点之后,随SO2气体的通入,![]() 的值始终减小
的值始终减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,在西藏自治区的铜金多金属成矿带多次发现罕见的金属互化物。金属互化物是合金中的一种,可表示为如Cu-Ni-Zn 或CaCux等形式。
(1)某种金属互化物具有自范性,原子在微观空间里呈现周期性的有序排列,该金属互化物属于____________(填“晶体”或“非晶体”)。
(2)铜在元素周期表中的位置是____________,基态Cu原子核外有__________种能量不同的电子。
(3)Ni2+能与许多配体形成配合物,如[Ni(CN)4]2-、二丁二酮肟合镍(Ⅱ)等。
①写出一种与CN-互为等电子体的分子:_______________(用化学式表示)。
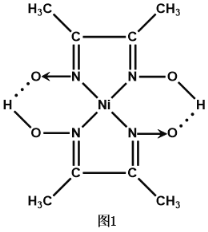
②二丁二酮肟合镍(Ⅱ)的结构如图1所示,Ni的配位数为____________,配位原子为____________,其中C原子的杂化方式为_____________。
(4)甲烷、氨气和水分子中的C、N、O原子均采用sp3杂化,VSEPR模型均为正四面体构型,比较三种分子的键角由大到小的顺序为_________,其原因是__________。
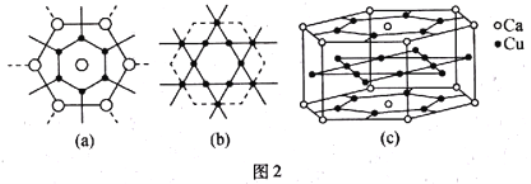
(5)CaCux可看作由如图2所示(a)(b)两种原子层交替堆积排列而成,图(c)表示CaCux晶胞结构图。合金CaCux中x=____________。已知同一层中Ca、Ca原子间的距离均为294pm,根据图示求同层的Ca、Ca原子间的距离为____________pm(取![]() =1.73,结果保留整数)。
=1.73,结果保留整数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物I(4-对羟基苯基-2-丁酮)是国际公认的既安全又获广泛应用的合成香料。由化合物A制备I的一种合成路线如下:

回答下列问题:
(1)A的化学名称为________________。
(2)B中的官能团名称是_________________。
(3)F的结构简式为_______________。
(4)⑤的反应类型是________________。
(5)写出满足下列条件的G的同分异构体的结构简式:______________。
i.属于芳香族化合物;
ii.既能发生银镜反应,又能发生水解反应;
iii.核磁共振氢谱为三组峰,峰面积比为6︰2︰1。
(6)设计由氯乙烷和丙二酸制备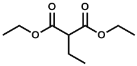 的合成路线:______(无机试剂任选)。
的合成路线:______(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案中,能达到相应实验目的的是
选项 | A | B | C | D |
目的 | 证明乙醇发生消去反应 | 证明乙炔可使溴水褪色 | 实验室制备乙酸乙酯 | 实验室制备氨气 |
实验方案 |
|
|
|
|
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)钠在自然界中只能以___________态存在,金属钠通常保存在____________里,它与水反应的化学方程式为:______________________________________________________。
(2)铝与氢氧化钠溶液反应的离子方程式为________________________________,实验室制备氢氧化铝常采用铝盐与氨水反应,写出氯化铝与氨水反应的离子方程式:_________________________。
(3)铁与水蒸气反应的化学方程式为:_____________________________。
(4)简述检验Fe3+的实验操作:___________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com