
����Ŀ�����������ֳƹ�ʯ�����Ʊ��輰���軯�������Ҫԭ�ϡ�����ת��������ͼ��ʾ������˵����ȷ����
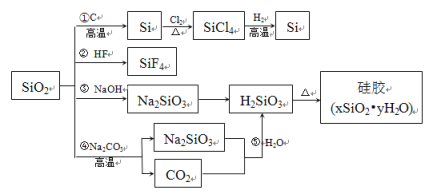
A.SiO2���ܷ����ڷ�Ӧ�����ܷ����۷�Ӧ��˵��SiO2��������������
B.�ܷ�Ӧ��ˮ�ҵ�Ļ�ѧ��Ӧԭ��֮һ���ݷ�Ӧ��֤��H2CO3����ǿ��H2SiO3
C.�ٷ�Ӧ���������Si���CO2���轺����������������
D.���˴ֹ���Ʊ����ᴿ�������漰�ķ�Ӧ�⣬ͼ����ʾ������Ӧ���Ƿ�������ԭ��Ӧ
���𰸡�D
��������
A. SiO2����HF��ӦSiF4��H2O������NaOH��Ӧ���ɹ����ƺ�����������������������Ķ��壬���������������A�����
B. SiO2��NaCO3�ķ�Ӧ�ǹ�ҵ���Ʋ����ķ�Ӧ����������CO2�ķ�Ӧ��������֤H2CO3����ǿ��H2SiO3��B�����
C. SiO2�ڸ�������C��Ӧ������Si���ʺ�CO�������в�����CO2��C�����
D. ���˴ֹ���Ʊ����ᴿ�������漰�ķ�Ӧ�⣬ͼ����ʾ������Ӧ���Ƿ�������ԭ��Ӧ��D����ȷ��
��ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������зḻ��ʳƷ���������Դ��ҩ���ˮ����Դ����ͼΪ��ˮ���õIJ��ֹ��̡�
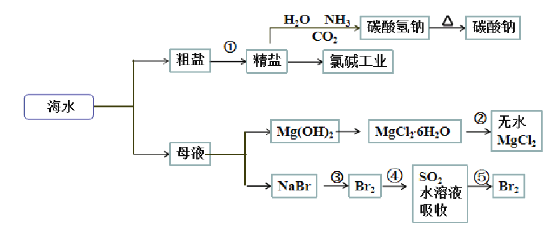
��֪��MgCl2��6H2O��������Mg(OH)Cl��HCl����ȡ�
�����й�˵����ȷ����
A.��ȡNaHCO3�ķ�Ӧ���������ܽ��С��NaCl
B.�ڹ��̢��н�MgCl2��6H2O���ռ����Ƶ���ˮMgCl2
C.�ڵڢ��������ݲ����У���Ԫ�ؾ�������
D.��ҵ�Ͻ�ʯ��ˮ���뵽��ˮ�еõ�Mg(OH)2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ�������ͼ��ʾ��װ�ã��ɱȽ�HNO3��H2CO3��H2SiO3������ǿ���������Ƚϵ���̼����Ԫ�طǽ�����ǿ������ѡ����Լ���ϡ���ᡢϡ���ᡢ̼��ƹ��塢̼���ƹ��塢��������Һ������ʯ��ˮ������̼��������Һ
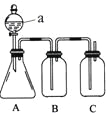
��1������a�����ƣ�________��
��2����ƿ��װ��ij���������Σ�a����ʢ�Լ�Ϊ________��
��3��װ��B��ʢ�Լ���____________________����������_____________��
��4��װ��C��ʢ�Լ���_______________��
C�з�Ӧ�����ӷ���ʽ��________________��
��5��ͨ��ʵ��֤��̼��������ķǽ�������ǿ������˳����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��������(Ag2SO4)���ܽ�ȴ����Ȼ�����������(Ag2SO4)���ܽ�����¶����߶�����T��ʱ��Ag2SO4��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵����ȷ���ǣ� ��
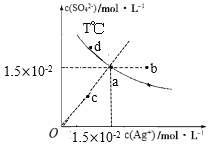
A.a����Һ�������������壬��a����������ƶ���b��
B.a����Һ�������¶ȣ���a����������ƶ���c��
C.��a�������Һ�м���NaCl���壬��Һ��ɿ��ܻ���a��d�����ƶ�
D.�����������ݼ����֪��T���£�Ksp(Ag2SO4)=2.25��10-4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ĵ���ƽ�ⳣ�������
���� | HCOOH | HClO | H2CO3 | H2SO3 |
����ƽ�� ������25�棩 | Ka��1.77��10��4 | Ka��4.0��10��8 | Ka1��4.3��10��7 Ka2��4.7��10��11 | Ka1��1.54��10��2 Ka2��1.02��10��7 |
��1�������¢�0.1mol��L-1HCOONa����0.1mol��L-1NaClO����0.1mol��L-1Na2CO3����0.1mol��L-1NaHCO3������Һ��pH�ɴ�С�Ĺ�ϵΪ________________�����������գ�
��2��Ũ�Ⱦ�Ϊ0.1 mol��L��1��Na2SO3��Na2CO3�Ļ����Һ�У�SO32-��CO32-��HSO3-��HCO3-Ũ�ȴӴ�С��˳��Ϊ________________��
��3���������ӷ���ʽ��ȷ����___________������ĸ����
A.2ClO-+H2O+CO2=2HClO+CO32- B.2HCOOH+CO32-=2HCOO-+H2O+CO2��
C.H2SO3+2HCOO-=2HCOOH+SO32- D.Cl2+H2O+2CO32-=2HCO3-+Cl-+ClO-
��4��ij�¶ȣ�T�棩�µ���Һ�У�c��H+��=10-xmol��L-1��c��OH-=10-ymol��L-1��x��y�Ĺ�ϵ��ͼ��ʾ��

�ٴ��¶��£�0.01mol/L��NaOH��Һ��ˮ�������OH-Ũ��Ϊ_______��
���ڴ��¶��£�0.1mol��L-1��NaHSO4��Һ��0.1mol��L-1��Ba(OH)2��Һ���±��мס��ҡ���������ͬ��ʽ��ϣ�
�� | �� | �� | �� | |
0.1mol��L-1��Ba��OH��2 | 10 | 10 | 10 | 10 |
0.1mol��L-1��NaHSO4 | 5 | 10 | 15 | 20 |
����ʽ��Ϻ�������Һ��pHΪ____________��
���ҷ�ʽ��Ϻ��䷴Ӧ�����ӷ���ʽ��_________________��
������ʽ��Ϻ�������Һ��____________����������������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ̽����ˮ�к��е����Ӽ������ʣ�ij��ѧС����������ʵ�飺
��1���۲���ˮ��ɫ��������ˮ��dz����ɫ��֤����ˮ�к��е�������____�������ӷ��ţ���
��2������ˮ�е���Na2CO3��Һ�����������ɣ�˵����ˮ�к��е�������___�������ӷ��ţ���
��3����ˮ�����պ۲쵽��������_______����Һ������_____�����ǿ�������䡱����������
��4����ˮ�о��������Եĺ�������_______�������ӷ��ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ի���������������������Ⱦ��кܴ��Ӱ�졣�밴Ҫ��ش��������⣺
��1����֪��4NH3(g)+6NO(g)=5N2(g)+6H2O(g) ��H1=-akJ/mol
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ��H2=-bkJ/mol
H2O(l)=H2O(g) ��H3=+ckJ/mol
��NH3(g)��������ȼ�����ɵ�����Һ̬ˮ���Ȼ�ѧ����ʽΪ___��
��2���ںϳɹ���ҵ�У������ڴ���Fe�ϵ������ֽⷴӦ��ܸߡ�����������˵����ķ�Ӧ���ʾ����˺ϳɰ��ķ�Ӧ���ʡ���ҵ�����У������¶�773K��ѹǿ3.0��105pa��ԭ����n(N2)��n(H2)=1��2.8�������˵��ԭ������N2����������___��
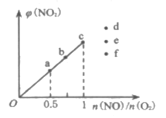
��3����֪��Ӧ2NO(g)+O2(g)![]() 2NO2(g)���ں��¡����ݵ��ܱ������а�һ���������������ʵ���һ����NO(g)��O2(g)��ƽ��ʱNO2���������[��(NO2)]��
2NO2(g)���ں��¡����ݵ��ܱ������а�һ���������������ʵ���һ����NO(g)��O2(g)��ƽ��ʱNO2���������[��(NO2)]��![]() �ı仯��ͼ��ʾ��NO��ת������С����___�㣨����a������b������c��)����
�ı仯��ͼ��ʾ��NO��ת������С����___�㣨����a������b������c��)����![]() =1.5ʱ���ﵽƽ��״̬ʱNO2���������������___�㣨����d������e������f��)��
=1.5ʱ���ﵽƽ��״̬ʱNO2���������������___�㣨����d������e������f��)��
��4�������еļ��쵰��(Mb)��O2�������MbO2����Ӧԭ���ɱ�ʾΪ��Mb(aq)+O2(g)![]() MbO2(aq)���÷�Ӧ��ƽ�ⳣ���ɱ�ʾΪ��K=
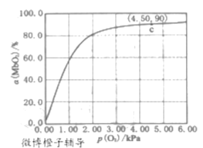
MbO2(aq)���÷�Ӧ��ƽ�ⳣ���ɱ�ʾΪ��K=![]() ��37��ﵽƽ��ʱ����ü��쵰�Ľ�϶�(a)��������ѹ[p(O2)]�Ĺ�ϵ��ͼ��ʾ[��=
��37��ﵽƽ��ʱ����ü��쵰�Ľ�϶�(a)��������ѹ[p(O2)]�Ĺ�ϵ��ͼ��ʾ[��=![]() ��100%]���о���������Ӧ����v��=k��c(Mb)p(O2)���淴Ӧ����v��=k��c(MbO2)������k����k���ֱ��ʾ�����淴Ӧ�����ʳ�������
��100%]���о���������Ӧ����v��=k��c(Mb)p(O2)���淴Ӧ����v��=k��c(MbO2)������k����k���ֱ��ʾ�����淴Ӧ�����ʳ�������
����(MbO2)������p(O2)������������������䣬ԭ����___��
����д��ƽ�ⳣ��K�����ʳ���k����k��֮��Ĺ�ϵʽK=___(�ú���k����k����ʽ�ӱ�ʾ)
�������ͼ��c��ʱ��������Ӧ��ƽ�ⳣ��K=___kPa-1��
.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ����٤��������ֵ������˵����ȷ����( )
A.3.9 g Na2O2������������Ϊ0.15 NA
B.��״���£�ÿ��22.4 L Cl2����ˮ��������Һ��H+����ĿΪNA
C.20 g �������������ӵ���ĿΪ0.5 NA
D.0.2 mol CO2�������� Na2O2��ַ�Ӧ��ת�Ƶĵ�������Ϊ0.4NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������[ KAl(SO4)2��12H2O ]����ֽ����ˮ�ȷ���Ӧ�ù㷺���Դ������ķϾ���������мΪԭ��(��Ҫ�ɷ�ΪAl������������Fe��Mg����)�Ʊ������Ĺ�������ͼ��ʾ��
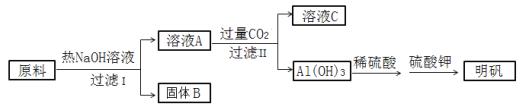
�ش��������⣺
��1��KAl(SO4)2�ĵ��뷽��ʽ______________________________��
��2��ԭ���ܽ�����з�Ӧ�����ӷ���ʽ��___________________________________��
��3��������Һ�������Ba(OH)2��Һ��Ӧ�����ӷ���ʽ��______________________________��
��4����ҺA��ͨ�����CO2����Ӧ�Ļ�ѧ����ʽ��_____________________________________��
��5��Ϊ֤������B�к�������ijͬѧ������ʵ�飺ȡ��������B������ϡ����ʹ���ܽ⣬�۲쵽����ɫ�������ɡ�����Һ�м���__________��__________����Һ������죬֤������B�к�������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com