
| ||
| ||
|
|


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
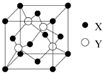 元素X位于第四周期,其基态原子的内层轨道全部排满电子,最外层电子数为2.元素Y基态原子的3p轨道有4个电子.元素Z的原子最外层电子数是内层的3倍.
元素X位于第四周期,其基态原子的内层轨道全部排满电子,最外层电子数为2.元素Y基态原子的3p轨道有4个电子.元素Z的原子最外层电子数是内层的3倍.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.08mol |
| B、0.10mol |
| C、0.12mol |
| D、0.18mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)将4molSO2和2molO2充入2L的密闭容器中,在一定条件下发生反应,经10s后达到平衡,测得SO3的浓度为0.6mol?L-1,请回答下列问题:
(1)将4molSO2和2molO2充入2L的密闭容器中,在一定条件下发生反应,经10s后达到平衡,测得SO3的浓度为0.6mol?L-1,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5g | B、4g | C、8g | D、10g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、恒温,压缩体积,平衡不移动,混合气体颜色加深 |
| B、恒压,充入HI(g),开始时正反应速率减小 |
| C、恒容,升高温度,正反应速率减小 |
| D、恒容,充入H2,I2(g)的体积分数降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
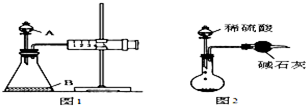 学校实验室现有含少量NaCl杂质的Na2CO3固体样品,某化学兴趣小组的同学决定测定样品Na2CO3的质量分数,甲、乙两位同学分别设计出下列两种实验方案:
学校实验室现有含少量NaCl杂质的Na2CO3固体样品,某化学兴趣小组的同学决定测定样品Na2CO3的质量分数,甲、乙两位同学分别设计出下列两种实验方案:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com