
【题目】2015年“812”天津港危化仓库爆炸,造成生命、财产的特大损失。据查危化仓库中存有大量的钠、钾,硝酸铵和氰化钠(NaCN)。NaCN属于剧毒物质,若处理不当,极易污染土壤和海水。请回答下列问题:
(1)钠、钾着火,下列可用来灭火的是______________。
A.水 B.泡沫灭火器 C.干粉灭火器 D.细沙盖灭
(2)NH4NO3为爆炸物,在不同温度下受热分解,可发生不同的化学反应:
在110℃时:NH4NO3=NH3+HNO3
在185~200℃时:NH4NO3=N2O+2H2O
在230℃ 以上时,同时有弱光:2NH4NO3=2N2+O2+4H2O
在400℃ 以上时,发生爆炸:4NH4NO3=3N2+2NO2+8H2O
上述反应过程中一定破坏了______________。(填“离子键”或“共价键”或“离子键和共价键”)
(3)NaCN 的电子式为______________。下列能说明碳与氮两元素非金属性相对强弱的是______________。
A.酸性:HNO2>H2CO3
B.相同条件下水溶液的 pH:NaHCO3>NaNO3
C.CH4比NH3更稳定
D.C 与H2的化合比N2与H2的化合更容易
(4)海水中含有Ca2+、Mg2+、HCO3- 等杂质离子。用惰性电极电解海水时阴极易产生水垢,其主要成分是 Mg(OH)2和CaCO3。写出电解海水的离子方程式______________;生成CaCO3的离子方程式是______________。
【答案】
(1)D;
(2)离子键和共价键;
(3)Na+[:C┇┇N:]﹣;B;
(4)2NaCl+2H2O![]() 2NaOH+H2↑+Cl2 ↑;Ca2++HCO3-+OH-=CaCO3↓+H2O
2NaOH+H2↑+Cl2 ↑;Ca2++HCO3-+OH-=CaCO3↓+H2O
【解析】
试题分析:(1)Na、K能和水反应生成氢气,在氧气中燃烧生成过氧化物,过氧化钠和水、二氧化碳反应都生成氧气,促进钠、钾燃烧,所以应该采用细沙灭火,故答案为:D;
(2)氯化铵属于离子化合物,含有离子键和共价键,氯化铵分解时破坏了共价键和离子键;故答案为:离子键、共价键;
(3)NaCN属于离子化合物,C、N原子周围都是8个电子,其电子式为:Na+[:C┇┇N:]-; A.酸性:HNO2>H2CO3,由于亚硝酸不是N元素的最高价氧化物对应的水化物,无法比较二者的非金属性大小,故A错误;B.相同条件下水溶液的pH:NaHCO3>NaNO3,说明硝酸的酸性强于碳酸,则证明非金属性N>C,故B正确;C、CH4的稳定性比NH3弱,与实际不符,故C错误;D、C 与H2的化合比N2与H2的化合更困难,与实际不符,故D错误;故答案为:Na+[:C┇┇N:]-;B;
(4)海水中含有Ca2+、Mg2+、HCO3- 等杂质离子。用惰性电极电解海水时阴极易产生水垢,其主要成分是 Mg(OH)2和CaCO3。写出电解海水的离子方程式为2NaCl+2H2O![]() 2NaOH+H2↑+Cl2 ↑;阴极生成氢气,电极附近水的电离被破坏,电极附近生成氢氧化钠,氢氧化钠和碳酸氢钙,碳酸氢镁反应生成氢氧化镁、碳酸钙沉淀,氢氧化钠和碳酸氢钙反应生成CaCO3的沉淀产生水垢,生成碳酸钙沉淀的反应离子方程式是:Ca2++HCO3-+OH-=CaCO3↓+H2O;
2NaOH+H2↑+Cl2 ↑;阴极生成氢气,电极附近水的电离被破坏,电极附近生成氢氧化钠,氢氧化钠和碳酸氢钙,碳酸氢镁反应生成氢氧化镁、碳酸钙沉淀,氢氧化钠和碳酸氢钙反应生成CaCO3的沉淀产生水垢,生成碳酸钙沉淀的反应离子方程式是:Ca2++HCO3-+OH-=CaCO3↓+H2O;


科目:高中化学 来源: 题型:
【题目】有机物X和Y可作为“分子伞”给药载体的伞面和中心支撑架(未表示出原子或原子团的空间排列)。
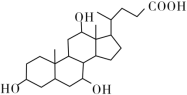
X(C24H40O5)
H2NCH2CH2CH2NHCH2CH2CH2CH2NH2 Y
下列叙述错误的是 ( )。
A.1 mol X在浓硫酸作用下发生消去反应,最多生成3 mol H2O
B.1 mol Y发生类似酯化的反应,最多消耗2 mol X
C.X与足量HBr反应,所得有机物的分子式为C24H37O2Br3
D.Y和癸烷的分子链均呈锯齿形,但Y的极性较强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,A是制取溴苯的实验装置,B、C是改进后的装置。请仔细分析,对比三个装置,回答以下问题:
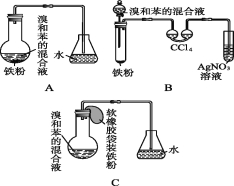
(1)写出三个装置中所共同发生的两个反应的化学方程式: 、 ;
(2)装置A和C均采用了长玻璃导管,其作用是 。
(3)B中采用了双球洗气管吸收装置,其作用是 ,反应后双球洗气管中可能出现的现象是 。
(4)B装置存在两个明显的缺点,使实验的效果不好或不能正常进行。这两个缺点是
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面的反应路线及所给信息填空。
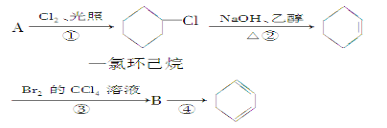
(1)A的结构简式是________________,名称是__________________。
(2)①的反应类型是____________,②的反应类型是________________
(3)反应①和②的化学方程式是____________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学实验室用如图所示装置制取少量溴苯。请填写下列空白。

(1)在烧瓶a中装的试剂是苯、溴和铁屑。导管b的作用有两个:一是导气,二是兼起_____的作用。
(2)反应过程中在导管c的下口附近可以观察到白雾出现,这是由于反应生成的_ _遇水蒸气而形成的。
(3)反应完毕后,向锥形瓶d中滴入AgNO3溶液,有__________生成。
(4)反应完毕后,将烧瓶a中的液体倒入盛有冷水的烧杯里,可以观察到烧杯底部有__________色不溶于水的液体。这是溶解了__________的粗溴苯。
(5)写出烧瓶a中发生反应的化学方程式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人设想合成具有下图结构的烃分子。
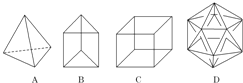
(1)结构D显然是不可能合成的,原因是____________________;
(2)在结构A的每两个碳原子之间插入一个CH2原子团,可以形成金刚烷的结构,金刚烷的分子式为_______;
(3)B的一种同分异构体是最简单的芳香烃,能证明该芳香烃中的化学键不是单双键交替排列的事实是_________;
a.它的对位二元取代物只有一种 b.它的邻位二元取代物只有一种
c.分子中所有碳碳键的键长均相等 d.能发生取代反应和加成反应
(4)C的一种属于芳香烃的同分异构体是生产某塑料的单体,写出合成该塑料的化学方式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298 K时,在20.0 mL 0.10 mol![]() 氨水中滴入0.10 mol
氨水中滴入0.10 mol![]() 的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10 mol
的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10 mol![]() 氨水的电离度为1.32%,下列有关叙述正确的是
氨水的电离度为1.32%,下列有关叙述正确的是

A.该滴定过程应该选择酚酞作为指示剂
B.M点对应的盐酸体积为20.0 mL
C.M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D.N点处的溶液中pH<12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(s)+3B(g)![]() 2C(g)+D(g),经2 min后,B的浓度减少了0.6 mol·L-1。对此反应速率的正确表示是( )
2C(g)+D(g),经2 min后,B的浓度减少了0.6 mol·L-1。对此反应速率的正确表示是( )
A. 用A表示的反应速率是0.8 mol·L-1·s-1
B. 分别用B、C、D表示反应的速率,其比值是3∶2∶1
C. 在2 min末时的反应速率,用反应物B来表示是0.3 mol·L-1·min-1
D. 在这2 min内用B和C表示的反应速率的值都是相同的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n。已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧热极高。Al2H6球棍模型如下图。下列有关说法肯定错误的是
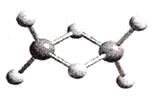
A. Al2H6在固态时所形成的晶体是分子晶体
B. 氢铝化合物可能成为未来的储氢材料和火箭燃料
C. Al2H6中含有离子键和极性共价键
D. Al2H6在空气中完全燃烧,产物为氧化铝和水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com