
【题目】由硫酸钾、硫酸铝和硫酸组成的混合溶液中,c(H+)=0.2molL-1,c(Al3+)=0.4molL-1,c(SO42-)=0.8molL-1,则c(K+)为( )
A. 0.2molL-1 B. 0.3molL-1 C. 0.4molL-1 D. 0.5molL-1
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:
【题目】下列实验操作能达到实验目的的是( )
A. 用排水法收集铜粉与浓硝酸反应产生的NO2
B. 用氨水鉴别NaCl、MgCl2、A1C13、NH4C1四种溶液
C. 用酸性KMnO4溶液验证草酸的还原性
D. 加热氯化铵固体制备氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氧化三铁(Fe3O4)的组成可表示为Fe2O3·FeO,下列说法不正确的是( )
A.四氧化三铁是一种混合物B.四氧化三铁是一种纯净物
C.四氧化三铁有固定的组成和结构D.四氧化三铁是一种黑色固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.CH4与C4H10不一定是同系物
B.苯分子中既含有碳碳单键,又含有碳碳双键
C.乙烯使溴水褪色属于取代反应
D.炒菜时,加入一点酒和醋能使菜味香可口,原因是有酯类物质生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究性学习小组的同学想通过下图实验装置探究SO2与Na2O2反应的产物。(夹持装置已略去,装置的气密性良好)
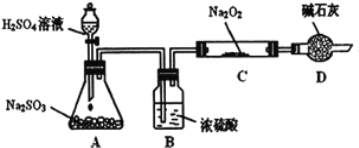
Ⅰ.实验中装置B可吸收水分,干燥SO2气体,其目的是:________________。装置D除了吸收过量的SO2,避免污染空气外,还起到的作用是:_______。
Ⅱ.对C中固体产物提出如下假设:(假设Na2O2已全部反应)
假设1:__________。
假设2:只有Na2SO4; 假设3:既有Na2SO3又有Na2SO4。
(1)甲同学认为SO2与Na2O2的反应不同于CO2,应为假设2成立,请据此写出C中所发生反应的化学方程式:_____________________。
(2)若假设2成立,为确定C中固体产物的成分,甲同学设计如下实验:
![]()
得出结论:C中固体产物只有Na2SO4。该方案是否合理?答:__________。(填“是”或“否”)理由是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气是城市空气的主要污染物,如何减少汽车尾气(CO,NOx等)的污染是重要的科学研究课题.
(1)已知:N2(g)+O2(g)═2NO(g)△H1
N2(g)+3H2(g)2NH3(g)△H2
2H2(g)+O2(g)═2H2O(g)△H3
则4NO(g)+4NH3(g)+O2(g)═4N2(g)+6H2O(g)△H=(用含△H1、△H2、△H3的式子表达)
(2)汽车尾气中的CO,NOx都需要除去,有人设想按下列反应除去CO;2CO(g)=2C(s)+O2(g)已知该反应在任何温度下都不能自发进行,因此该设想便不能实现.由此判断该反应的△H0
目前,在汽车尾气系统中装置催化转化器可以减少CO,NO的污染,其化学反应方程式为
(3)可用活性炭还原法处理氮氧化物.有关反应的化学方程式为:C(s)+2NO(g)N2(g)+CO2(g)△H>0某研究小组向密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如表:
浓度/molL﹣1 | NO | N2 | CO2 |
0 | 0.100 | 0 | 0 |
10 | 0.058 | 0.021 | 0.021 |
20 | 0.040 | 0.030 | 0.030 |
30 | 0.040 | 0.030 | 0.030 |
40 | 0.032 | 0.034 | 0.017 |
则,30min后,改变某一条件,平衡发生了移动,则改变的条件是;若升高温度,NO浓度将(填“增大”、“不变”或“减小”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)1mol NH4+质量为_____,其中含质子、电子的数目分别为_____、_____。
(2)标准状态下,672mL某气体质量为0.84g,该气体摩尔质量为_____。
CO 和CO2 混合气体的密度相对氢气为19,则CO 和CO2体积比为_________,若某原子的摩尔质量是M g /mol,则一个该原子的真实质量是____________g;将标准状况下的aLHCl(g)溶于1000g水中,得到的盐酸密度为bg/mL,则该盐酸的物质的量浓度是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com