
����Ŀ�����Ž��з���Ƶ�һ��Ԫ��������������������ε��ݱ䣬�����˶�����ʽ��Ԫ�����ڱ������ʾ�Ĺ����ڶ���Ƿ�������Ҫ���á��±���Ԫ�����ڱ��в��ֶ���������Ԫ�ص��й���Ϣ��
Ԫ�ر�� | Ԫ�����ʻ�ԭ�ӽṹ |
T | ������ 5 �ֲ�ͬ�����ĵ��ӣ���������� 2 �ԳɶԵ��� |
X | ����ϼ�Ϊ+7 �� |
Y | ����������Ԫ��ԭ���а뾶��� |
Z | ����������Ӧˮ����������� |
��1����������Ԫ���У�������ӵİ뾶��С����________�������ӷ��ţ���
��2��T �� X ��Ӧ��Ԫ�أ�����̬�⻯���ȶ��Խ�ǿ����_______���ѧʽ����
��3����ԭ�ӽṹ��֪ʶ��˵�� T �� X ��ӦԪ�صķǽ����Ե����ǿ������ T ��ӦԪ�ص���̬�⻯���ˮ��Һ�еμ� X ���ʵ�ˮ��Һ��������_______��д����Ӧ�����ӷ���ʽ _______��
��4��Y �� Z ��ӦԪ�أ�������������Ӧˮ����ɷ�����Ӧ��д���÷�Ӧ�����ӷ���ʽ________��
��5������ Z ��ӦԪ�صĵ��ʣ�����������Ӧ��ұ����������Ӧ��������11.2g���ʣ���ת�Ƶ��ӵ���ĿΪ___��
���𰸡�Al3+ HCl �е���ɫ�������� H2S+Cl2=2H++2Cl-+S�� Al(OH)3 + OH- = AlO2- + 2H2O 0.6NA��3.612��1023
��������
��������Ԫ�ض�Ϊ����������Ԫ�أ� Tԭ�Ӻ�����5�ֲ�ͬ�����ĵ��ӣ�ӦΪ��������Ԫ�أ�����ֲ�Ϊ1s��2s��2p��3s��3p������Ϊ������� 2 �ԳɶԵ��ӣ�3p�������4�����ӣ���TΪSԪ�أ�������������ϼ�Ϊ+7�۵�Ԫ��ΪClԪ�أ���XΪClԪ�أ�����������Ԫ��ԭ���а뾶����Ԫ��ΪNa����YΪNaԪ�أ�������������������Ӧˮ�����������Ϊ������������ZΪAlԪ�ء�
��1����������Ԫ�طֱ�Ϊ�ơ��������ȣ������Ӻ��������������Ӳ㣬�����Ӻ�������Ϊ�������Ӳ㣬�������Ӻ������ӵİ뾶���������Ӻ������ӣ������Ӻ������Ӻ�������Ų���ͬ���������ӵĺ˵�����뾶С��������ӵİ뾶��С����Al3+��
����Al3+��
��2��TΪSԪ�أ�XΪClԪ�أ�����̬�⻯��ֱ�Ϊ������Ȼ��⣬��̬�⻯����ȶ��ԣ��뻯ѧ���ļ��ܴ�С�йأ������ӵİ뾶С�������ӵİ뾶����H-Cl�ļ���С��H-S�ļ���������Խ�̣�����Խ������̬�⻯���ȶ��Խ�ǿ����HCl��
����HCl��
��3��TΪSԪ�أ�XΪClԪ�أ�T��̬�⻯��Ϊ���⣬��Ԫ��Ϊ��ͼۣ����л�ԭ�ԣ�X ���ʵ�ˮ��ҺΪ��ˮ����ˮ��ǿ�����ԣ��������ˮ����������ԭ��Ӧ���������ʺ��Ȼ��⣬�������ˮ��Һ�еμ���ˮ���ɹ۲쵽��Һ���ֻ�ɫ���ǣ����������ӷ�ӦΪ��H2S+Cl2=2H++2Cl-+S����
��Ϊ���е���ɫ�������ɣ�H2S+Cl2=2H++2Cl-+S����
��4��YΪNaԪ�أ�ZΪAlԪ�أ�������������Ӧˮ����ֱ�Ϊ�������ƺ�������������������Ϊ�����������������ǿ�Ӧ������ƫ�����κ�ˮ���÷�Ӧ�����ӷ���ʽAl(OH)3 + OH- = AlO2- + 2H2O��
����Al(OH)3 + OH- = AlO2- + 2H2O��
��5��ZΪAlԪ�أ���������ijЩ����������������ȼ����������ȷ�Ӧ���������ȷ�Ӧ����ұ��������������������Ӧ������������������Ӧ����ʽΪFe2O3+2Al![]() Al2O3+2Fe������Ӧ��������11.2g�����ʣ���0.2mol������+3�۱�Ϊ0�ۣ���ת�Ƶ��ӵ���ĿΪ0.2mol��3��6.02��1023=0.6NA��3.612��1023��
Al2O3+2Fe������Ӧ��������11.2g�����ʣ���0.2mol������+3�۱�Ϊ0�ۣ���ת�Ƶ��ӵ���ĿΪ0.2mol��3��6.02��1023=0.6NA��3.612��1023��
����0.6NA��3.612��1023��


 ��һ����ͬ���ɽ�����ϵ�д�
��һ����ͬ���ɽ�����ϵ�д� ������Ӧ���ϵ�д�
������Ӧ���ϵ�д� ��ʦ�㾦�ִʾ��ƪϵ�д�
��ʦ�㾦�ִʾ��ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ǰ�(NH2OH)��ˮ��Һ�еĵ��뷽��ʽΪ��NH2OH+H2O![]() NH3OH++OH-����0.1mol/L����ζ�20mL0.1mol/L NH2OH��Һ���㶨25��ʱ���ζ���������ˮ���������OH-Ũ�ȵĸ���������������Ĺ�ϵ��ͼ��ʾ������˵��������ǣ� ��
NH3OH++OH-����0.1mol/L����ζ�20mL0.1mol/L NH2OH��Һ���㶨25��ʱ���ζ���������ˮ���������OH-Ũ�ȵĸ���������������Ĺ�ϵ��ͼ��ʾ������˵��������ǣ� ��
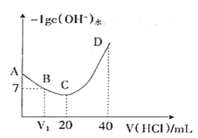
A.A��D��Һ�У�NH2OH���볣������
B.��A��D��ˮ�������c(OH-)��С
C.B���Ӧ����Һ��c(Cl-)=c(NH3OH+)
D.C���Ӧ����Һ��c(H+)=c(OH-)+ c(NH2OH)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��G��ҩ��ϳɵ��м��壬�䲿�ֺϳ�·�����£�
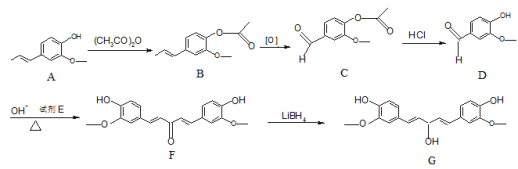
��֪��RCHO + CH3COR1 ![]() RCH=CHCOR1 + H2O
RCH=CHCOR1 + H2O
��ش��������⣺
(1)C��D�ķ�Ӧ����Ϊ_______________��
(2)�Լ�E������Ϊ_____________��G�ķ���ʽΪ_______________��
(3)д��A��B�Ļ�ѧ����ʽ__________________________________��
(4)���A��B�����Ŀ����__________________ ��
(5)�����廯����T��D��ͬ���칹�壬�������������Ľṹһ����___ �֡�
���ܷ���������Ӧ��
����FeCl3��Һ��������ɫ��Ӧ������ϡ�����е�ˮ�����֮һ��FeCl3��Һ�ܷ�����ɫ��Ӧ��
���ں˴Ź���������������壻
(6)�Ի�������![]() Ϊԭ�ϣ��ϳ�
Ϊԭ�ϣ��ϳ�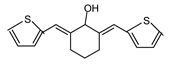 ��·��Ϊ__________________________��
��·��Ϊ__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л����˵����ȷ���ǣ� ��
A.��������(![]() )�Ķ��ȴ�����6�ֽṹ(�����������칹)
)�Ķ��ȴ�����6�ֽṹ(�����������칹)
B.����ϩ(![]() )���Է����ӳɷ�Ӧ���Ӿ۷�Ӧ��ȡ����Ӧ��������Ӧ��
)���Է����ӳɷ�Ӧ���Ӿ۷�Ӧ��ȡ����Ӧ��������Ӧ��
C.����ʽΪC5H10O2������������ͬ���칹�干��8��(�����������칹)
D.�����Ǻ��ǻ�Ϊͬϵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ����٤����������ֵ������������ȷ����
A. 78g���к��е�̼̼˫������ĿΪ3NA
B. 16gCu2S��CuO��ɵĻ�����к��е���������Ϊ0.2NA
C. ��1mol H2�� 1 mol I2����һ�ܱ������г�ַ�Ӧ��ת�Ƶĵ�����Ϊ2NA
D. 1 mol Fe ��������Ũ���Ṳ�ȷ�Ӧ������SO2�ķ�����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС�������ͼװ��(���ּг�װ������ȥ),��̽����ʪ��Cl2��Na2CO3��Ӧ�õ��������ʵijɷ֡�

(1)�Լ�X�Ļ�ѧʽ________��A����ȡCl2�����ӷ���ʽ____________________��
(2)�Լ�Y������Ϊ______________��
(3)ͨ��һ������ʪ��Cl2��Ӧ��,�����,D��ֻ��Cl2Oһ������,C�г���һ��������,ͬʱ����NaHCO3��,ijͬѧ��C�����ù�������ijɷֽ���̽����
������������衣
����1:�������ֳɷ�:NaHCO3��____________________________;
����2:�������ֳɷ�:NaHCO3��__________________________��
����Ʒ���,����ʵ�顣д��ʵ�鲽���Լ�Ԥ������ͽ��ۡ�_______
��ѡʵ���Լ�������:����ˮ��ϡ���ᡢBaCl2��Һ������ʯ��ˮ��AgNO3��Һ���Թܡ�С�ձ���

(4)��֪Cl2O��ˮ��Ӧ���ɴ�����,��D��Cl2O����E��Ӧ�Ļ�ѧ����ʽΪ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��W��X��Y��Z��ԭ�������������ӣ�K��L��M��������ЩԪ����ɵĶ�Ԫ������ס��ҷֱ���Ԫ��X��Y�ĵ���,���dz����Ĺ��壬���dz��������塣K����ɫ���壬����Ҫ�Ĵ�����Ⱦ��֮һ��0.05mol/L����Һ��pHΪl���������ʵ�ת����ϵ��ͼ��ʾ������˵����ȷ����
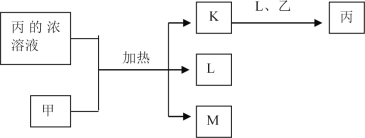
A. ԭ�Ӱ뾶��W<X<Y B. Ԫ�صķ�ȫ���ԣ�Z>Y>X
C. ������XYZ��ֻ�����ۼ� D. K��L��M�зе���ߵ���M
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������٤��������ֵΪNA������˵����ȷ����( )
A.�ڳ��³�ѹ�£� lmol �������е�ԭ����ĿΪ2NA
B.7. 1������ͨ������������������Һ�У�ת�Ƶĵ�����Ϊ0.2NA
C.��״���£�2.24L N2��O2�Ļ��������ԭ����Ϊ0.2NA
D.��״���£�2.24LHCl����500mLˮ��������ҺŨ��Ϊ2mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CuCl�㷺Ӧ���ڻ�����ӡȾ����ҵ��ij�о���ѧϰС�����ȷֽ�CuCl2��2H2O�Ʊ�CuCl�����������̽����
�����ϲ��ģ�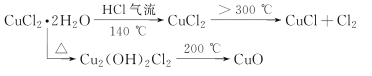
��С������ͼ��ʾװ�ý���ʵ��(�г�������)
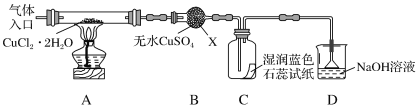
��ش��������⣺
��1������X��������___��
��2��ʵ��������Ⱥ�˳����a��___��e(������ı��)��
a�����װ�õ������Ժ����ҩƷ
b��Ϩ��ƾ��ƣ���ȴ
c���ڡ�������ڡ���ͨ�����HCl
d����ȼ�ƾ��ƣ�����
e��ֹͣͨ��HCl��Ȼ��ͨ��N2
��3����ʵ������У��۲쵽B�������ɰ�ɫ��Ϊ��ɫ��C����ֽ����ɫ�仯��___��
��̽����˼��
��4����Ӧ������ȡ��CuCl��Ʒ����ʵ�飬�������к���������CuCl2��CuO���ʡ�����������Ϣ
����������CuCl2���������ԭ����___��
����������CuO���������ԭ����___��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com