
【题目】下列除去杂质的实验方法正确的是
A. 除去乙酸乙酯中的少量乙酸:加入KOH溶液,充分反应后,弃去水溶液
B. 除去苯酚中的少量甲苯:加入酸性高锰酸钾溶液,充分反应后,弃去水溶液
C. 除去苯中少量的甲苯:加高锰酸钾溶液,振荡,分液
D. 除去乙醇中少量的水:加足量生石灰,蒸馏
科目:高中化学 来源: 题型:
【题目】乙二醛(OHC-CHO)化学性质活泼,是纺织工业中常用的一种有机原料,能增加棉花、尼龙等纤维的防缩性和防皱性。其工业生产方法主要是乙二醇(HOCH2CH2OH)气相催化氧化法和乙醛液相硝酸氧化法。请回答下列相关问题:
(1)乙二醇气相催化氧化法
以乙二醇、氧气为原料,在催化剂存在的条件下,250℃左右开始缓慢进行,生成乙二醛和副产物乙醇酸[CH2(OH)COOH]的反应方程式:
I.HOCH2CH2OH(g)+O2(g) ![]() OHC-CHO(g)+2H2O(g)△H1
OHC-CHO(g)+2H2O(g)△H1
II.HOCH2CH2OH(g)+O2(g) ![]() CH2(OH)COOH(g)+H2O(g)△H2
CH2(OH)COOH(g)+H2O(g)△H2
已知反应I中相关化学键键能数据如下:
化学键 | C-H | C-O | H-O | O==O | C==O | C-C |
E/kJ·mol-1 | 413 | 343 | 465 | 498 | 728 | 332 |
①△H1=_____kJ/mol,反应I的化学平衡常数表达式为K=________。
②欲提高I的平衡产率,可以采取的措施是______(填标号)。
A.升高温度 B.增大压强 C.降低温度 D.减小压强
③提高乙二醛反应选择性的关键因素是_________________________。
④保持温度和容积不变,下列描述能说明反应I达到平衡状态的是________(填标号)。
A.v正(O2)=2v逆(H2O)
B.混合气体的压强不再随时间变化而变化
C.混合气体的密度不再发生变化
D.乙二醇与OHC-CHO的物质的量之比为1:1
E.混合气体中乙二醛的体积分数不再发生变化
(2)乙醛(CH3CHO)液相硝酸氧化法
11.0g40%的乙醛溶液和40%的硝酸,按一定比例投入氧化反应釜内,在Cu(NO3)2催化下,控制温度在38~40℃时,反应10h,再通过萃取等操作除去乙醛、硝酸等,最后经减压浓缩得4.35g40%乙二醛溶液。
①用稀硝酸氧化乙醛制取乙二醛时,有N2O产生。其化学方程式为______________________。
②利用上面数据,计算乙二醛的产率为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,探究铜与稀HNO3,反应过程如下:
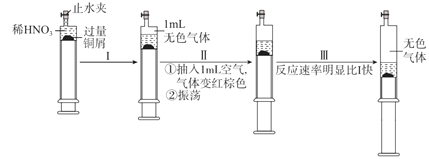
下列说法不正确的是
A. 过程I中生成无色气体的离子方程式是3Cu+2 NO3-+8H+ =3Cu2++2NO↑+4H2O
B. 步骤III反应速率比I快的原因是NO2溶于水,使c(HNO3)增大
C. 由实验可知,NO2对该反应具有催化作用
D. 当活塞不再移动时,再抽入空气,铜可以继续溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向0. 10 mol·L-1的Na2CO3溶液中逐滴加入稀盐酸,加入的HCl与原溶液中Na2CO3的物质的量之比f[f=![]() ]与混合液pH的关系如图所示。下列说法正确的是
]与混合液pH的关系如图所示。下列说法正确的是
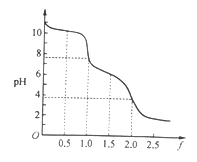
A. f=0时,溶液中:c(Na+)=2c(CO32-)
B. f=0.5时,溶液中:c(HCO3-)>c(CO32-)
C. f= 1时,溶液中:c(Na+) + c(H+) = 2c(CO32-) + c(HCO3-)+c(OH-)
D. f=2时,溶液中:1/2c(Na+)=c(CO32-)+c( HCO3-)+c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“十三五”期间,云南省将推进8条支线天然气管道的建设,促成云南真正迈入“气化时代”。根据下列有关天然气的研究和应用回答问题:
(l)在一定温度和压强下,由最稳定单质生成lmol化合物的焓变称为该物质的摩尔生成焙。根据此定义,稳定单质的摩尔生成焓为0。某些化合物的摩尔生成焓如下表所示:
化合物 | CO2 | CH4 | CO |
摩尔生成焓(kJ·mol) | -395 | -74.9 | -110.4 |
CH4(g)与CO2(g)反应生成CO(g)和H2(s)的热化学方程式为______。
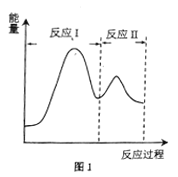
(2)若上述反应分Ⅰ、Ⅱ两步进行,其能量曲线如图1所示。则总反应的反应速率取决于反应_______(填“I”或“Ⅱ”)。
(3)一定温度下反应:CO2(g)+CH4(g) ![]() 2CO(g)+2H2(g)的平衡常数表达式Kp=___(用平衡分压代替平衡浓度表示).
2CO(g)+2H2(g)的平衡常数表达式Kp=___(用平衡分压代替平衡浓度表示).
(4)在压强为p1、p2、p3的三个恒压密闭容器中分别通入1.0molCH4(g)与1.0mol CO2(g),发生反应:CO2(g)+CH4(g)![]() 2CO(g)+2H2(g).测得平衡时CH4的体积分数与温度、压强的关系如图2所示。
2CO(g)+2H2(g).测得平衡时CH4的体积分数与温度、压强的关系如图2所示。

① a点时CH4的转化率为_______。
② 压强p1、p2、p3由大到小的顺序为______,判断理由是_____。
温度为Tl℃、压强为P3时,b点处v(正)_____v(逆)(填“<”、“>”或“=”)。
(5)某种燃料电池以熔融碳酸钠、碳酸钾为电解质,其工作原理如图3所示,该电池负极的电极反应式为________。若电极B附近通入1m3空气(假设空气中O2的体积分数为20% )并完全反应,理论上可消耗相同条件下CH4的体积为_______m3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表前四周期的一部分,下列有关R、W、X、 Y、Z五种元素的叙述中,正确的是( )
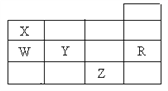
A. 通常情况下五种元素的单质中,Z单质的沸点最高
B. Y、Z的阴离子电子层结构都与R原子的相同
C. W的电负性比X的的电负性大
D. 第一电离能:R>W>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X是一种具有果香味的合成香料,如图所示为合成X的一种流程。 E是日常生活中常见的一种有机物,碳、氢的质量分数分别约为52.17% 、13.04% ,其余为氧,E的相对分子质量为46,其中含有甲基和亚甲基(—CH2—)。
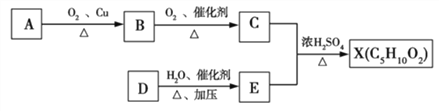
请根据以上信息,回答下列问题:
(1)A分子中官能团的名称是_____,E的结构简式是_______。
(2)D→E的化学反应类型为________。
(3)上述A、B、C、D、E、X六种物质中,互为同系物的是___。
(4)写出和E是同系物且差2个碳原子能和钠反应的所有同分异构体的结构简式_______________________________________________。
(5)反应C + E![]() X的化学方程式为____________________________。
X的化学方程式为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应式正确的是
A. 铅蓄电池充电时阴极的反应式:Pb2++2e-=Pb
B. 碱性锌锰干电池放电时,负极反应式:Zn-2e-=Zn2+
C. 酸性高锰酸钾与草酸溶液:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑-8H2O
D. I用铁氰化钾检验Fe2+:3FeCl2+2K3[Fe(CN)6]=Fe3[Fe(CN)6]2↓+6KCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对氨基苯甲酸酯类是一类局部麻醉药,化合物M是该类药物之一。用烯烃A和芳烃E合成M的一种路线如下:
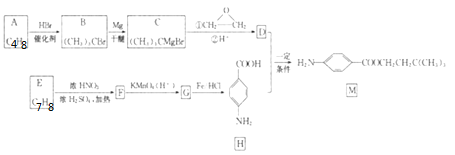
回答下列问题:
(1)A的结构简式为_______;B的化学名称为_______。
(2)检验B中官能团所用的试剂为_______;由E生成F的化学方程式为_______。
(3)由G生成H的反应类型为_______;H在一定条件下发生聚合反应的化学方程式为_______。
(4)M的同分异构体有多种,写出其中符合下列条件的两种同分异构体的结构简式:_______________。
①苯环上只有两个取代基;②核磁共振氢谱有五组峰,且峰面积比为12∶2∶2∶2∶1。
(5)参照上述合成路线,写出以乙烯和环氧乙烷为原料(其他试剂任选)制备1,6-己二醛的合成路线图:_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com