
【题目】实验室模拟工业上侯德榜制碱原理制备纯碱,下列操作未涉及的是
A.  B.
B.  C.
C.  D.
D. 
【答案】B
【解析】
侯氏制碱法是依据离子反应会向着离子浓度减小的方向进行。先在饱和食盐水中通入氨气,再向其中通入二氧化碳,制得溶解度较小的NaHCO3,再利用碳酸氢钠不稳定性分解得到纯碱。据此分析解答。
A.实验室模拟工业上侯德榜制碱原理制备纯碱过程中需要加热固体碳酸氢钠分解以制得碳酸钠,装置A是固体加热灼烧的装置,涉及此操作,故A不选;
B.装置B是蒸发溶液得到晶体的过程,侯德榜制碱原理中不需要蒸发溶液操作,故B选;
C.该装置为过滤操作,溶液中析出碳酸氢钠晶体需要过滤得到碳酸氢钠晶体,涉及此操作,故C不选;
D.工业上利用侯德榜制碱原理制备纯碱,需要向氨化的饱和食盐水中通入足量二氧化碳气体析出碳酸氢钠,涉及此操作,故D不选;
答案选B。


科目:高中化学 来源: 题型:
【题目】下列实验操作、现象和结论均正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 将铜粉加入1.0mol/LFe2(SO4)3溶液中 | 溶液变为蓝色 | 金属铁比铜活泼 |
B | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝不滴落下来 | 氧化铝的熔点高于铝的熔点 |
C | 常温下,用pH计测0.1mol/LNaX溶液和0.1mol/LNa2CO3溶液的pH | 前者小于后者 | 酸性:HX>H2CO3 |
D | 向10%的蔗糖溶液中加入少量稀硫酸,水浴加热一段时间,再加入银氨溶液 | 未出现光亮银镜 | 蔗糖未发生水解 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在固定容积、体积为2 L的密闭容器中充入1 mol N2和3 mol H2发生反应,当反应进行到10 s末时反应达到平衡,此时容器中c(NH3)=0.1mol·L-1。下列有关判断错误的是
A.反应达平衡时N2的转化率为10%
B.反应进行到10 s末时,H2的平均反应速率是0.03 mol·(L·s)-1
C.该反应达到平衡时,N2的平衡浓度为0.45 mol/L
D.该反应达到平衡时的压强是起始时压强的0.95倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环丙叉环丙烷(n)由于其特殊的结构,一直受到结构和理论化学家的关注。它有如下转化关系,下列说法正确的是( )
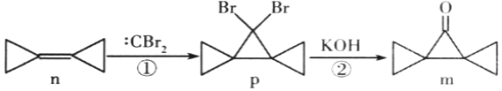
A. n的所有原子都在一个平面内B. 反应②是消去反应
C. n与![]() 互为同分异构体D. m的同分异构体中属于芳香族化合物的共有四种
互为同分异构体D. m的同分异构体中属于芳香族化合物的共有四种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物X含C、 H 、O三种元素,现已知下列条件:①碳的质量分数 ②氢的质量分数 ③X蒸气的摩尔体积(STP) ④X对H2的相对密度 ⑤X的质量。确定X的分子式需要的最少条件是
A. ①②B. ①③⑤C. ①②④D. ①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在杠杆的两端分别挂着质量相同的铝球和铁球,此时杠杆平衡。然后将两球分别浸没在溶液质量相等的稀烧碱溶液和硫酸铜溶液中一段时间,如图所示,下列说法正确的是( )

A. 铝球表面有气泡产生,溶液中有白色沉淀生成;杠杆不平衡
B. 铝球表面有气泡产生,溶液澄清;铁球表面有红色物质析出;溶液蓝色变浅,杠杆右边下沉
C. 反应后去掉两烧杯,杠杆仍平衡
D. 右边球上出现红色,左边溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质的叙述正确的是
A. 二氧化硫能使紫色石蕊溶液变红但不褪色B. 氯水久置后,漂白性和酸性均减弱
C. 常温下,铁片不能与浓硝酸发生反应D. 植物油酸性条件下水解生成肥皂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 64 g SO2含有氧原子数为1NA
B. 物质的量浓度为0.5 mol·L-1的MgCl2溶液,含有Cl-数为1 NA
C. 标准状况下,22.4 L H2O的分子数为1NA
D. 常温常压下,14 g N2含有分子数为0.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,体积一定的密闭容器中进行如下反应:X(g)+Y(g) ![]() Z(g)+W(s), △H>0下列叙述正确的是( )
Z(g)+W(s), △H>0下列叙述正确的是( )
A. 加入少量W,逆反应速度增大 B. 当容器中气体压强不变时,反应达到平衡
C. 升高温度,平衡逆向移动 D. 平衡后加入X,上述反应的△H增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com