
 FeO(s)+CO(g)��H=Q1��ƽ�ⳣ��ΪK1��
FeO(s)+CO(g)��H=Q1��ƽ�ⳣ��ΪK1�� FeO(s)+H2(g)��H=Q2��ƽ�ⳣ��ΪK2���ڲ�ͬ�¶��£�K1��K2��ֵ���£�
FeO(s)+H2(g)��H=Q2��ƽ�ⳣ��ΪK2���ڲ�ͬ�¶��£�K1��K2��ֵ���£�| �¶�(T) | K1 | K2 |
| 973 | 1��47 | 2��38 |
| 1173 | 2��15 | 1��67 |
 CO(g)+H2O(g)��H=Q3
CO(g)+H2O(g)��H=Q3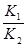 ��DE��Q3=Q1�DQ2
��DE��Q3=Q1�DQ2 CO(g)+H2O(g)��H=Q3����˷�ӦӦ�۵�K3=
CO(g)+H2O(g)��H=Q3����˷�ӦӦ�۵�K3=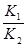 ���ӱ��е����ݿ�֪�������¶ȵ����ߣ�K3��ֵ�������ߵģ���˸÷�Ӧ�����ȷ�Ӧ����С���������ƽ�ⲻ�ƶ��������¶ȣ�ƽ�������ƶ���ʹ�ú��ʵĴ�����ƽ�ⲻ�ƶ����跨����CO��������С���������Ũ�ȣ�ƽ�����ƣ������¶ȣ�ƽ���������ȵķ����ƶ������ѡDE��Q3=Q1�DQ2
���ӱ��е����ݿ�֪�������¶ȵ����ߣ�K3��ֵ�������ߵģ���˸÷�Ӧ�����ȷ�Ӧ����С���������ƽ�ⲻ�ƶ��������¶ȣ�ƽ�������ƶ���ʹ�ú��ʵĴ�����ƽ�ⲻ�ƶ����跨����CO��������С���������Ũ�ȣ�ƽ�����ƣ������¶ȣ�ƽ���������ȵķ����ƶ������ѡDE��Q3=Q1�DQ2

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3 (g)����H����197 kJ��mol-1����ͬ�¡�ͬ����������ܱ������зֱ�������壺(��) 2 mol SO2��1 mol O2��(��) 1 mol SO2��0.5 mol O2��(��) 2 mol SO3�����¡������·�Ӧ��ƽ��ʱ�����й�ϵһ����ȷ����
2SO3 (g)����H����197 kJ��mol-1����ͬ�¡�ͬ����������ܱ������зֱ�������壺(��) 2 mol SO2��1 mol O2��(��) 1 mol SO2��0.5 mol O2��(��) 2 mol SO3�����¡������·�Ӧ��ƽ��ʱ�����й�ϵһ����ȷ����| A��������ѹǿP��P����P�� > 2P�� |
| B��SO3������m��m����m�� > 2m�� |
| C��c(SO2)��c(O2)֮��k��k����k�� > k�� |
| D����Ӧ�ų���������������ֵQ��Q����Q�� > 2Q�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
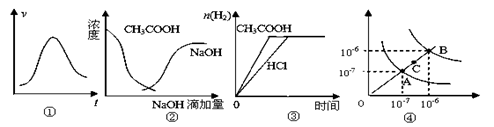
| A��ͼ�ٱ�ʾһ��������ij��ѧ��Ӧ��������ʱ��仯������ͼ���÷�Ӧһ��Ϊ���ȷ�Ӧ |
| B��ͼ�������߱�ʾ������������Һ�μӵ�������ҺŨ�ȵı仯����ͼ |
| C��ͼ�۱�ʾ������������ʵ���Ũ�ȵ�����ʹ�����Һ���ֱ��������þ�ۣ�����H2�����ʵ����ı仯 |
| D��ͼ��Ϊˮ�ĵ���ƽ������ͼ������A�㵽C�㣬�ɲ�����ˮ�м�������NaOH����ķ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
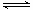 B(g) + C(g)����H = ?48��25 kJ/L
B(g) + C(g)����H = ?48��25 kJ/L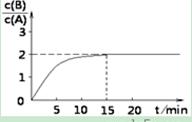
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NO(g)��O2(g)��H>0���ﵽƽ�⡣���ı�����һ������X��Y��X�ı仯����ͼ�����ߵ���
2NO(g)��O2(g)��H>0���ﵽƽ�⡣���ı�����һ������X��Y��X�ı仯����ͼ�����ߵ���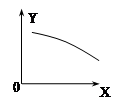
| A��X��ʾ�¶�ʱ��Y��ʾNO2���ʵ��� |
| B��X��ʾNO2���ʵ�����Y��ʾO2�����ʵ��� |
| C��X��ʾ��Ӧʱ��ʱ��Y��ʾ���������ܶ� |
| D��X��ʾѹǿʱ��Y��ʾNO2�ĺ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NO2��H>0���ܱ������з�Ӧ���ﵽƽ��״̬��Ҫʹ���������ɫ����ɲ�ȡ�ķ����� �ټ�Сѹǿ ����С����������¶Ȣ�����N2O4��Ũ�� �� ��
2NO2��H>0���ܱ������з�Ӧ���ﵽƽ��״̬��Ҫʹ���������ɫ����ɲ�ȡ�ķ����� �ټ�Сѹǿ ����С����������¶Ȣ�����N2O4��Ũ�� �� �� | A���ڢۢ� | B���٢ڢ� | C���٢ۢ� | D���٢ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2R(g) ��H��0����ͼ��Y����ָ
2R(g) ��H��0����ͼ��Y����ָ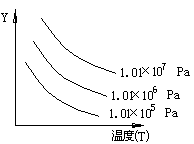
| A��ƽ��������R���������� | B��G��ת���� |
| C��ƽ��������G��������� | D��L��ת���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ɫ��NO2����ѹ����ɫ�ȱ�����dz |
| B����ѹ�ȳ�ѹ�����ںϳ�SO3�ķ�Ӧ |
| C����H2(g)��I2(g)��HI(g)������ɵ�ƽ����ϵ��ѹ����ɫ���� |
| D������ɫ����ˮ���պ���ɫ��dz |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2Z(g)���������ı�ʹ��ѧƽ��������Ӧ�����ƶ�ʱ������������ȷ����
2Z(g)���������ı�ʹ��ѧƽ��������Ӧ�����ƶ�ʱ������������ȷ����| A���٢ڢ� | B���ۢܢ� | C���ڢ� | D���ܢ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com