“低碳循环”已引起各国家的高度重视,而如何降低大气中CO
2的含量和有效地开发利用CO
2正成为化学家研究的主要课题.
(l)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
C+
KMnO
4+
H
2SO
4→
CO
2↑+
MnSO
4+
K
2SO
4+
H
2O
(2)将不同量的CO(g)和H
2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H
2O(g)?CO
2(g)+H
2(g),得到如下两组数据:
| 实验组 |
温度℃ |
起始量/mol |
平衡量/mol |
达到平衡所需时间/min |
| CO |
H2O |
H2 |
CO |
| 1 |
650 |
4 |
2 |
1.6 |
2.4 |
6 |
| 2 |
900 |
2 |
1 |
0.4 |
1.6 |
3 |
①实验2条件下平衡常数K=
.
②实验3,若900℃时,在此容器中加入CO、H
2O、CO
2、H
2均为1mol,则此时v
正
v
逆(填“<”,“>”,“=”).
③由两组实验结果,可判断该反应的正反应△H
0(填“<”,‘‘>”,“=”).
(3)己知在常温常压下:
①2CH
3OH(l)+3O
2(g)═2CO
2(g)+4H
2O(g)△H=-1275.6kJ/mol
②2CO(g)+O
2(g)═2CO
2(g)△H=-566.0kJ/mol
③H
2O(g)═H
2O(l)△H=-44.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
2CO(g)═2C(s)+O
2(g)
①已知该反应的△H>0,简述该设想能否实现的依据:
.
②目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为
.
(5)CO
2在自然界循环时可与CaCO
3反应,CaCO
3是一种难溶物质,其Ksp=2.8×10
-9.CaCl
2溶液与Na
2CO
3溶液混合可形成CaCO
3沉淀,现将等体积的CaCl
2溶液与Na
2CO
3溶液混合,若Na
2CO
3溶液的浓度为1×10
-4mol/L,则生成沉淀所需CaCl
2溶液的最小浓度为
mol/L.



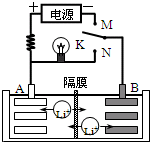 如图是一种可充电的锂离子电池充、放电的工作示意图.放电时该电池的电极反应式为:
如图是一种可充电的锂离子电池充、放电的工作示意图.放电时该电池的电极反应式为: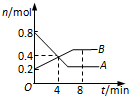 某温度时,在2L密闭容器中某一反应的A、B物质的量随时间变化的曲线如图所示.下列说法不正确的是( )
某温度时,在2L密闭容器中某一反应的A、B物质的量随时间变化的曲线如图所示.下列说法不正确的是( )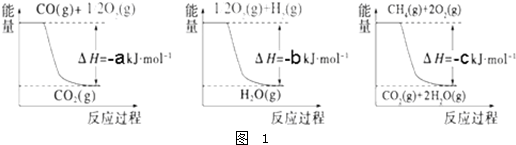
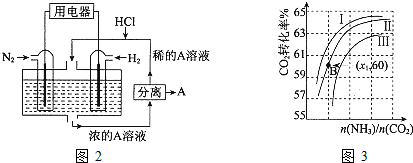
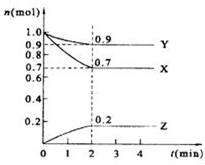 某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.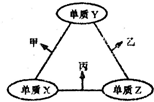 x、y、z三种短周期元素的原子半径依次变小,原子序数之和为16;这三种元素形成的常见单质分别为X、Y、Z,它们在适当条件下可发生如图所示转化关系;其中乙和丙均为l0电子气体分子,且二者相遇生成弱碱.下列说法正确的是( )
x、y、z三种短周期元素的原子半径依次变小,原子序数之和为16;这三种元素形成的常见单质分别为X、Y、Z,它们在适当条件下可发生如图所示转化关系;其中乙和丙均为l0电子气体分子,且二者相遇生成弱碱.下列说法正确的是( )