
����Ŀ����ҵ���þ������ˮú���ڴ��������£���ˮ����������Ӧ��ȡ��������ѧ����ʽΪCO(g)+H2O(g) ![]() H2(g)+CO2(g)��һ�������£���4 mol CO��2 mol H2O(g)�������Ϊ2 L���ܱ������У���ϵ�и����ʵ�Ũ����ʱ��ı仯��ͼ��ʾ��
H2(g)+CO2(g)��һ�������£���4 mol CO��2 mol H2O(g)�������Ϊ2 L���ܱ������У���ϵ�и����ʵ�Ũ����ʱ��ı仯��ͼ��ʾ��

��1����0��4 minʱ�Σ���Ӧ����v(H2O)Ϊ_________mol��L1��min1���������·�Ӧ��ƽ�ⳣ��KΪ_______(������λ��Ч����)��
��2���÷�Ӧ��4 minʱ��CO��ת����Ϊ_______________��
��3����6 minʱ�ı���ⲿ����Ϊ���£���÷�Ӧ�Ħ�H_______________0(�>����=����<��)����ʱ��Ӧ��ƽ�ⳣ��_________________(�������С�����䡱)��
��4���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������____________��
a�����������ܶȲ���
b�����������c(CO)����
c��v(H2O)��=v(H2)��
d������2 mol H��O����ͬʱ����1 mol H��H��
��5����������4 minʱ��ͬ���¶ȣ���һ�ݻ��ɱ���ܱ�������ͬʱ����0.5 mol CO��1.5 mol H2O(g)��
0.5 mol CO2��a mol H2����a=2.5ʱ��������Ӧ��________________(�����Ӧ�����淴Ӧ��)������С���Ҫʹ������Ӧ��ʼʱ���淴Ӧ������У���a��ȡֵ��ΧΪ_____________��
���𰸡���1��0.2 2.7 ��2��40% ��3��< ��С ��4��bc ��5������Ӧ a>4.05
����������1��v(H2O)=(1.0 mol/L0.2 mol/L)��4 min=0.2 mol��L1��min1���ɷ�Ӧ�Ļ�ѧ����ʽ��ͼ���֪��4 min�ﵽƽ��ʱc(CO)=1.2 mol/L��c(H2O)=0.2 mol/L��c(CO2)=c(H2)=0.8 mol/L����ƽ�ⳣ��K=![]() =
=![]() ��2.7��
��2.7��
��2��CO��ת����Ϊ(2.01.2)/2.0��100%=40%��
��3��6 minʱ���£���Ӧ��CO��H2O��Ũ������ƽ�������ƶ���������ӦΪ���ȷ�Ӧ������H��0������ƽ�������ƶ�����ƽ�ⳣ����С��
��4���÷�Ӧ�з�Ӧ����������Ϊ���壬����������ʼ�ղ��䣬�ַ�Ӧ����������䣬�ʷ�Ӧ�����л��������ܶ�ʼ�ղ��䣬���ܶȲ��䲻����Ϊ��Ӧ�ﵽƽ��ı�־��a�����Ӧ������ij�ַ�Ӧ����������Ũ�Ȳ��䣬������Ӧ�ﵽƽ�⣬b����ȷ���÷�Ӧ����ʽ��H2O��H2��ϵ����ȣ���v(H2O)��=v(H2)��=v(H2)��ʱ������Ӧ�ﵽƽ�⣬c����ȷ������H��O��������H��H������ָ����Ӧ���ʸ������Ϊ��Ӧ�ﵽƽ��ı�־��d�����
��5���������ݻ��ɱ䣬�������ݻ�ΪV L����Qc=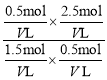 ��1.7��2.7���ʷ�Ӧ������Ӧ������У�����Ӧ��ʼʱ���淴Ӧ������У���Qc=
��1.7��2.7���ʷ�Ӧ������Ӧ������У�����Ӧ��ʼʱ���淴Ӧ������У���Qc= ��2.7����a��4.05��
��2.7����a��4.05��


 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʻ���ӽ�ʱ���ܷ�����Ӧ�����д����������ɵ��ǣ� ��
A. Ũ��ˮ������ B. Ũ�����Ũ��ˮ
C. �Ȼ����Һ���ռ� D. ������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʲ����ڼ������ʵ���(����)
A. ��ȫȼ��ʱ���ɶ�����̼��ˮ
B. ���³�ѹ��������ˮ
C. ����������±�ص��ʷ���ȡ����Ӧ
D. ͨ������£���ǿ�ᡢǿ���ǿ����������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��ȥ����CO2�е�SO2��O2�������Լ���ʹ��˳����ȷ���ǣ� (�� ��)
������Na2CO3��Һ��������NaHCO3��Һ����ŨH2SO4��Һ�������ȵ�ͭ��������ʯ��
A���٢ۢ� B���ڢۢ� C���ڢܢ� D���ۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ź�ҵ�ķ�չ��������CO2��Ũ�Ȳ������ӣ���μ���CO2�ŷ��ѳ�Ϊȫ�����ע���ȵ㣬��̼���ú͵�̼�����Ϊ���Ż��⣬�����������̼Ҫ����Υ������ ( )
A�����Ƹ��ܺ���ҵ���� B��������ʹ��һ���Կ���
C���ᳫ�����г����˹��������� D������ú����磬�ӿ쾭�÷�չ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ܷ���������Ӧ��4NH3+5O2=4NO+6H2O���ı���������ʹ��Ӧ���ʼӴ���������������������������İٷ��������� ��
A. ����NH3Ũ�� B. ��С�������ѹǿ
C. �����¶� D. �����¶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���⻯�(NH4H)���Ȼ�淋Ľṹ���ƣ���֪NH4H��ˮ��Ӧ���������ɣ�����������ȷ����
A��NH4H�ǹ��ۻ�����
B��NH4H����ˮ���γɵ���Һ������
C��NH4H��ˮ��Ӧʱ��NH4H��������
D��NH4H����Ͷ������ˮ�У���������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���淴Ӧ��A��g��+3B��g��![]() 2C��g������H��0���м��������ݻ�Ϊ0.5L���ܱ���������������м���1molA�ĺ�3molB��һ�������´ﵽƽ��ʱ�ų�����ΪQ1 kJ������ͬ�����£����������м���2mol C�ﵽƽ��ʱ��������ΪQ2kJ����֪Q2=3Q1��������������ȷ����
2C��g������H��0���м��������ݻ�Ϊ0.5L���ܱ���������������м���1molA�ĺ�3molB��һ�������´ﵽƽ��ʱ�ų�����ΪQ1 kJ������ͬ�����£����������м���2mol C�ﵽƽ��ʱ��������ΪQ2kJ����֪Q2=3Q1��������������ȷ����
A. ����C��ת����Ϊ75%
B. ��Ӧ�ﵽƽ��ǰ������ʼ����v������v�棬����ʼ����v��С��v��
C. �ڸ������£���Ӧ 2C��g��![]() A��g��+3B��g����ƽ�ⳣ��Ϊ27��1.54
A��g��+3B��g����ƽ�ⳣ��Ϊ27��1.54
D. ���е��Ȼ�ѧ����ʽΪ2C��g��![]() A��g��+3B��g������H=+Q2kJ/mol
A��g��+3B��g������H=+Q2kJ/mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com