
����Ŀ�����ݻ�Ϊ2L�ĸ����ܱ������м���1molCO2��3molH2��������Ӧ��CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)���������������������£��¶ȶԷ�Ӧ��Ӱ����ͼ��ʾ(ע��T1��T2������300��)������˵����ȷ���ǣ� ��
CH3OH(g)+H2O(g)���������������������£��¶ȶԷ�Ӧ��Ӱ����ͼ��ʾ(ע��T1��T2������300��)������˵����ȷ���ǣ� ��
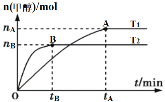
A.�÷�Ӧ��T1ʱ��ƽ�ⳣ������T2ʱ��С
B.����A��ķ�Ӧ��ϵ��T1�䵽T2���ﵽƽ��ʱ![]() ��С
��С
C.T2ʱ����Ӧ�ﵽƽ��ʱ���ɼ״��ķ�Ӧ����v(CH3OH)=![]() mol��L-1��min-1
mol��L-1��min-1
D.T1ʱ������Ӧ�ﵽƽ���CO2��ת����Ϊx���������ڵ�ѹǿ����ʼѹǿ֮��Ϊ(2-x)��2
���𰸡�D
��������
A��ͼ�������֪�ȹ���ƽ�¶ȸߣ�T1��T2���¶�Խ��ƽ��ʱ���ɼ״����ʵ���ԽС��˵������ӦΪ���ȷ�Ӧ�����¶�Խ�ߣ�ƽ�ⳣ��ԽС���÷�Ӧ��T1ʱ��ƽ�ⳣ����T2ʱ�Ĵ�A����
B��������֪T1��T2��A�㷴Ӧ��ϵ��T1�䵽T2������ƽ��������У��ﵽƽ��ʱ![]() ����B����
����B����
C��T2�´ﵽƽ��״̬�״����ʵ���nB����Ӧ�ﵽƽ��ʱ���ɼ״���ƽ������Ϊv��CH3OH����![]() molL��1min��1����C����
molL��1min��1����C����
D��T1�£�����Ӧ�ﵽƽ���CO2ת����Ϊx����
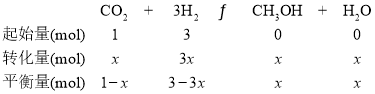
�������ڵ�ѹǿ����ʼѹǿ֮�ȣ�![]() ����D��ȷ����ѡD��
����D��ȷ����ѡD��


 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д� ���ƽ̸�������ѡ����ĩ���100��ϵ�д�
���ƽ̸�������ѡ����ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2 L�ܱ�������ͨ��a mol����A��b mol����B����һ�������·�����Ӧ��xA(g)��yB(g)pC(g)��qD(g)��֪��ƽ����Ӧ����v(C)��![]() v(A)����Ӧ2 minʱ��A��Ũ�ȼ�����
v(A)����Ӧ2 minʱ��A��Ũ�ȼ�����![]() a mol��B�����ʵ���������
a mol��B�����ʵ���������![]() mol����a mol D���ɡ�
mol����a mol D���ɡ�
�ش��������⣺
(1)��Ӧ2 min�ڣ�v(A)��________��v(B)��________��
(2)��ѧ����ʽ�У�x��________��y��________��p��________��q��________��
(3)��Ӧƽ��ʱ��DΪ2a mol����B��ת����Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ָ����Ӧ�����ӷ���ʽ��ȷ���ǣ� ��
A.��������ˮ��Cl2��H2O=2H����Cl-��ClO-
B.FeSO4��Һ�백ˮ��Ӧ�����ӷ���ʽ��Fe2����2NH3��H2O=Fe(OH)2����2NH4+
C.������Һ��KIO3��KI��Ӧ����I2��IO3-��I-��6H��=I2��3H2O
D.NaHCO3��Һ�м�����Ba(OH)2��Һ��2HCO3-��Ba2����2OH-=BaCO3����2H2O��CO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ����С������ʵ���ʾ��ͼ��ͼ��ʾ��ͼ�С�������ʾ�������� M��һ�ִ�������������壬YΪ��һ�����壬E���к���ɫ���������ʵ����������ֻ��������������ѡȡ��Na2CO3��Na2O2��NaCl��Na2O��CaCl2��(NH4)2CO3����ʯ�ҵȹ��弰����ˮ���ݴ�ʵ�飬���������գ�

(1)A������װ�õ���Ҫ������ҩƷ��______________________��
(2)B����ѡ�ĸ������________����������______________________________��
(3)C�з�������Ҫ��Ӧ�Ļ�ѧ����ʽ��________________________________��
(4)��ȡY�����Dװ�����õ���Ҫ������__________________________��
��ȡY����Ļ�ѧ����ʽ��________________________��
(5)F�з�����Ӧ�Ļ�ѧ����ʽΪ__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ҫ����Ԥ��ͬ������������ų���Ӧ����ṹ��ʽ����ͼ��ʾ��
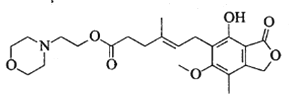
����˵����ȷ����
A. ���������ķ���ʽΪC23H30O7N
B. ���������ɷ����ӳɡ�ȡ������ȥ��Ӧ
C. ������������������̼ԭ��һ������ͬһƽ��
D. 1mol����������NaOH��Һ��ַ�Ӧ�������3mol NaOH��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС������ȷ�Ӧʵ��չ���о����ԡ����ȷ�Ӧ��������������������������Ӧ�ų��������ȣ�������ҫ�۵Ĺ�â����ֽ©�����²����մ���������������ɳ�С�����֪Al��Al2O3��Fe��Fe2O3���ۡ��е����������
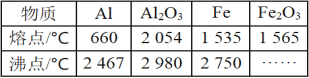
��1��ijͬѧ�Ʋ⣬���ȷ�Ӧ���õ�������������������Ͻ�������___��
��2��ijͬѧ�������Ӧ�ų��������ȣ�������ҫ�۵Ĺ�â���������п���ֻ�Ƿ����������ʵ�ȼ�շŴ����ȡ������û�ѧ�������ʵ����֤���ȷ�Ӧ�ķ�����___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص�Ũ�����Լ���ǩ�ϵIJ������ݡ�

�����ø�Ũ�������Ƴ�1mol/L��ϡ���ᣬ��ʵ���ҽ���Ҫ����ϡ����220mL���Իش��������⣺
��1������Ͳ��ȡ��Ũ����____________mL��
��2������ʱ������ʹ�õ���������Ͳ���ձ����������⣬��ȱ�ٵ�������____��
��3��������Һ�Ĺ����У�������������ȷ�����в�����ʹ������ҺŨ��ƫ�ߵ���__________��
A������Ͳ��ȡŨ����ʱ����
B��ϡ��Ũ����ʱ��δ��ȴ�����¼�ת�Ƶ�����ƿ��
C����ȡŨH2SO4�����Ͳ����ϴ�ӣ�����ϴ��Һת�Ƶ�����ƿ��
D������ҡ�Ⱥ���Һ����ڿ̶��ߣ����ý�ͷ�ιܼ�����ˮ����Һ����ʹ���̶�������
E������ƿ������
F������ʱ����������ƿ�̶���
��4��ijͬѧ�ù���Na2CO3����500 mlL 0.1molL-1��Һ�Ĺ�����ͼ��ʾ��

����Ϊ��ͬѧ�Ĵ�������__________����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ����������ij�ܱ������м��� 0.3 mol A��0.1 mol C ��һ������ B �������壬ͼ 1 ��ʾ������Ũ����ʱ��ı仯��ͼ 2 ��ʾ������ʱ��ı仯��t2��t3��t4��t5 ʱ�̸��ı�һ���������Ҹı����������ͬ����t4ʱ�� �ı��������ѹǿ��������˵���������

A.�� t1=15 s����ǰ 15 s ��ƽ����Ӧ���� v(C)=0.004 mol��L-1��s-1
B.�÷�Ӧ�Ļ�ѧ����ʽΪ 3A(g)![]() B(g)+2C(g)
B(g)+2C(g)
C.t2��t3��t5 ʱ�̸ı�������ֱ��������¶ȡ��������������Ӧ��Ũ��
D.�� t1=15 s���� B ����ʼ���ʵ���Ϊ 0.04 mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com