
【题目】某条件下,在 2L 密闭容器中发生如下反应:2NO2(g) ![]() 2NO(g)+O2(g)。若反应在三种不同条件下进 行,其中实验 I、II 都在 800℃,实验 III 在 850℃,NO、O2 的起始浓度都为 0 mol/L,NO2 的浓度(mol·L-1) 随时间(min)的变化如图所示,请回答下列问题:
2NO(g)+O2(g)。若反应在三种不同条件下进 行,其中实验 I、II 都在 800℃,实验 III 在 850℃,NO、O2 的起始浓度都为 0 mol/L,NO2 的浓度(mol·L-1) 随时间(min)的变化如图所示,请回答下列问题:
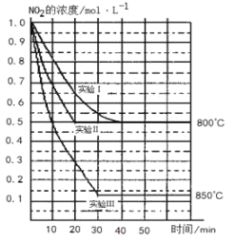
(1)对比实验I、II和III,得出的下列结论中正确的是___________。
A.实验II和实验I相比,可能隐含的反应条件是:反应容器的体积缩小了
B.实验II和实验I相比,可能隐含的反应条件是:使用效率更高的催化剂
C.实验I条件下该反应的平衡常数大于实验III条件下该反应的平衡常数
D.对比实验I和III可知,该反应正反应是吸热反应
(2)若实验I中NO2的起始浓度改为2.0mol·L-1,其它条件不变,则达到平衡时所需用的时间________40min(填“大于”、“等于”或“小于”),NO2的转化率将____(填“增大”、“减小”或“不变”)。
(3)该反应的平衡常数表达式是___________,若实验I达平衡后,再向密闭容器中通入2mol由物质的量之比为1:1组成的NO2与NO混合气体(保持温度不变),则平衡将___________(填“向左”、“向右”或“不”)移动,达到新平衡时,NO2的物质的量浓度为_________mol·L-1。
(4)若改变外界条件,使该反应的平衡常数数值变大,下列说法正确的是_______。
A. 一定向正反应方向移动 B. 在平衡移动时,正反应速率先增大后减小
C. 一定向逆反应方向移动 D. 在平衡移动时,逆反应速率先增大后减小
【答案】BD 小于 减小 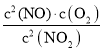 不 1.0 AB
不 1.0 AB
【解析】
(1)A.实验Ⅱ和实验I相比,反应都从浓度为1.0mol/LNO2的分解开始建立平衡,温度相同,平衡时NO2的浓度相同,到达平衡的时间实验Ⅱ比实验I少,即条件改变只加快反应速率,不影响平衡移动,反应前后为气体体积减小的反应,故只能是实验Ⅱ使用催化剂,故A错误,
B. 由A分析可知,实验Ⅱ使用催化剂,故B正确;
C. 对比实验Ⅰ和Ⅲ,实验Ⅲ温度升高,平衡时二氧化氮的浓度减少,平衡向正反应进行,所以实验Ⅲ平衡常数更大,故C错误;
D. 对比实验Ⅰ和Ⅲ,实验Ⅲ温度升高,平衡时二氧化氮的浓度减少,平衡向正反应进行,升高温度平衡向吸热方向移动,所以正反应为吸热反应,故D正确;
故答案为:BD;
(2)实验 I 中 NO2 的起始浓度改为 2.0mol·L1,其它条件不变,浓度增大,压强增大,反应加快,缩短到达平衡时间,达到平衡时所需用的时间小于40min;增大压强平衡向气体体积减小的方向移动,即向逆反应方向移动,NO2转化率减小;
故答案为:小于;减小;
(3)化学平衡常数为生成物浓度系数次幂之积与反应物浓度系数次幂之积的比值,则该反应的平衡常数表达式K=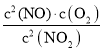 ;
;
实验Ⅰ中达平衡后,c(NO2)=0.5mol/L,
2NO2(g)2NO(g)+O2(g)
开始(mol/L):1 0 0
变化(mol/L):0.5 0.5 0.25
平衡(mol/L):0.5 0.5 0.25
平衡常数K=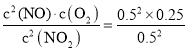
![]() =0.25,
=0.25,
再通入2mol由物质的量之比为1:1组成的NO2与NO混合气体(保持温度不变),此时为c(NO2)=0.5mol/L+![]() =1mol/L,c(NO)=0.5mol/L+
=1mol/L,c(NO)=0.5mol/L+![]() =1mol/L,c(O2)=0.25mol/L,
=1mol/L,c(O2)=0.25mol/L,
浓度商为Qc=![]() =0.25,等于平衡常数,所以平衡不移动;NO2的物质的量浓度为 1mol/L,
=0.25,等于平衡常数,所以平衡不移动;NO2的物质的量浓度为 1mol/L,
故答案为: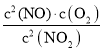 ;不;1.0;
;不;1.0;
(4)化学平衡常数只与温度有关,△H>0,该反应为吸热反应,升温,平衡右移,K增大,v(正)、v(逆)均增大,随着反应进行v(正)逐渐减小、v(逆)逐渐增大,最终达到新平衡,A、B正确,
故答案为:AB。


科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为短周期元素,在元素周期表中的相对位置如图所示。A、C两元素原子的核外电子数之和等于B原子的质子数,B原子的质子数和中子数相等。
A | C | |
D | B | E |
请回答下列问题:
(1)E元素位于元素周期表中第________周期第________族。
(2)几种元素中最高价氧化物对应的水化物的酸性最强的是(用化学式表示)____________________。
(3)C元素的原子结构示意图为________,用电子式表示C的氢化物的形成过程:____________。
(4)由元素A、C及氢元素形成的化合物中含有的化学键类型为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化钠是重要的化工原料,大多采用无水芒硝(Na2SO4)—炭粉还原法制备,原理为:Na2SO4+2CNa2S+2CO2↑。其主要流程如下:
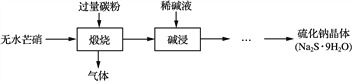
(1) 上述流程中采用稀碱液比用热水更好,理由是________________________________________________________________________。
(2) 已知:I2+2S2O32-===2I-+S4O62-。所制得的Na2S·9H2O晶体中含有Na2S2O3·5H2O等杂质。为测定产品的成分,进行下列实验,步骤如下:
a. 取试样10.00 g配成500.00 mL溶液。
b. 取所配溶液25.00 mL于碘量瓶中,加入过量ZnCO3悬浊液除去Na2S后,过滤,向滤液中滴入2~3滴淀粉溶液,用0.050 00 mol·L-1 I2溶液滴定至终点,用去5.00 mL I2溶液。
c. 再取所配溶液25.00 mL于碘量瓶中,加入50.00 mL 0.050 00 mol·L-1的I2溶液,并滴入2~3滴淀粉溶液,振荡。用标准Na2S2O3溶液滴定多余的I2,用去15.00 mL 0.100 0 mol·L-1 Na2S2O3溶液。
①步骤b中用ZnCO3除去Na2S的离子方程式为____________。
②判断步骤c中滴定终点的方法为______________。
③计算试样中Na2S·9H2O和Na2S2O3·5H2O的质量分数,写出计算过程__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学利用所学知识探究Na2O2与H2能否反应,设计了如下装置图,回答下列问题:
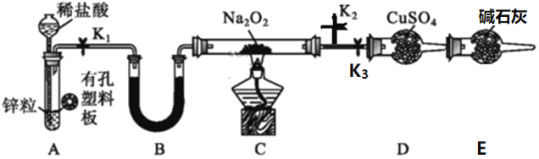
(1)装置A的气密性的检查方法是_______;A中发生反应的离子方程式为____________。
(2)Na2O2的电子式为_______________。装置中装硫酸铜固体的仪器名称是__________。装置B中盛放的试剂名称为__________。
(3)装置E的作用是_____________。
(4)实验中涉及到下列操作,其正确的顺序是____________。
①关闭K2,打开K1、K3,点燃C处酒精灯 ②在K2出口处收集一小试管气体验纯
③关闭K3,打开K1、K2 ④装置冷却后关闭K1 ⑤熄灭C处酒精灯
(5)若观察到D处干燥管中固体变蓝,则C中发生反应的化学方程式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知图一表示的是可逆反应 CO(g)+H2(g)![]() C(s)+H2O(g)-Q(Q>0)的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)
C(s)+H2O(g)-Q(Q>0)的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)![]() N2O4(g)+Q(Q>0)的浓度(c)随时间 t 的变化情况,下列 说法中正确的是
N2O4(g)+Q(Q>0)的浓度(c)随时间 t 的变化情况,下列 说法中正确的是
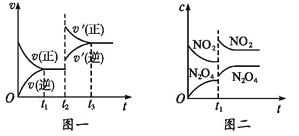
A.图一 t2 时刻改变的条件可能是升高了温度或增大了压强
B.图一 t2 时刻改变的条件可能是通入了 CO 气体
C.图二 t1 时刻改变的条件可能是升高了温度或增大了压强
D.图二 t1 时刻改变的条件是增大压强,则混合气体的平均相对分子质量将减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应NH4Cl+NaNO2![]() NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列表示反应中相关微粒的化学用语正确的是
NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列表示反应中相关微粒的化学用语正确的是
A. 中子数为18的氯原子:![]()
B. N2的结构式:N=N
C. Na+的结构示意图: 
D. H2O的电子式: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘在不同状态下(固态或气态)与氢气反应的热化学方程式如下所示:
①H2(g) + I2(?)![]() 2HI(g)+9.48kJ
2HI(g)+9.48kJ
②H2(g) + I2(?)![]() 2HI(g)-26.48kJ
2HI(g)-26.48kJ
下列判断正确的是
A.①中的I2为固态,②中的I2为气态
B.②的反应物总能量比①的反应物总能量低
C.①的产物比反应②的产物热稳定性更好
D.1mol 固态碘升华时将吸热17kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应N2 + 3H2![]() 2NH3,下列判断正确的是( )
2NH3,下列判断正确的是( )
A.3体积H2和足量N2反应,必定生成2体积NH3
B.工业上采用氮氢循环操作的主要目的是提高H2和N2的利用率
C.500℃左右比室温更有利于向合成氨的方向进行
D.其他条件不变,增大压强,平衡必定向右移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答:
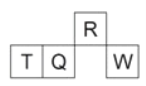
(1)T的原子结构示意图为___________
(2)元素的非金属性:Q_________W(填“强于”或“弱于”)
(3)R有多种氧化物,其中相对分子质量最小的氧化物为_____________
(4)原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是___________
(5)T的最高价氧化物对应的水化物和强碱溶液反应的离子方程式为___________
(6)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为 _________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com