
【题目】已知:pBa=-lgc(Ba2+),Ksp(BaSO4)=1.0×10-10,Ksp(BaCO3)=3.0×10-9。常温下,用 0.1 mol·L-1Na2SO4溶液滴定 20 mL 0.1 mol·L-1BaCl2溶液的曲线如图所示,V0达到滴定终点,下列说法错误的是
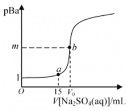
A.图像中,m=5,V0=20
B.若将c(BaCl2)从 0.1 mol· L-1变为 0.2 mol· L-1,m 值将减小
C.a 点溶液中离子浓度大小关系为:c(Cl-)>c(Na+)>c(Ba2+)>c(OH-)
D.向b点溶液中滴加Na2CO3溶液至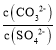 ≥30 时将生成BaCO3
≥30 时将生成BaCO3
【答案】B
【解析】
A. 图像中,m=5,pBa=-lgc(Ba2+)=5,c(Ba2+)=10-5mol· L-1,Ksp(BaSO4)=1.0×10-10,c(SO42-)=10-5mol· L-1,沉淀完全,反应的钡离子和硫酸根离子的量相同,20 mL× 0.1 mol·L-1=V0×0.1 mol·L-1,V0=20mL,故A正确;
B. 若将c(BaCl2)从 0.1 mol· L-1变为 0.2 mol· L-1,m为沉淀完全时,pBa=-lgc(Ba2+),m 值不变,故B错误;
C. a 点溶液中离子浓度大小关系为:c(Cl-)=![]() ,c(Na+)=
,c(Na+)=![]() ,c(Ba2+)=
,c(Ba2+)=![]() ,c(OH-)来源于水电离,c(Cl-)>c(Na+)>c(Ba2+)>c(OH-),故C正确;
,c(OH-)来源于水电离,c(Cl-)>c(Na+)>c(Ba2+)>c(OH-),故C正确;
D. BaSO4+CO32-![]() BaCO3+SO42-,K
BaCO3+SO42-,K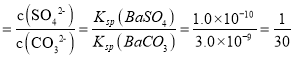 ,向b点溶液中滴加Na2CO3溶液至
,向b点溶液中滴加Na2CO3溶液至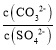 ≥30 时将生成BaCO3,故D正确;
≥30 时将生成BaCO3,故D正确;
故选B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】按要求写热化学方程式:
(1)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应的中和热化学方程式____。
(2)25℃、101 kPa条件下充分燃烧一定量的丁烷气体放出热量为Q kJ,经测定,将生成的CO2通入足量澄清石灰水中产生25 g白色沉淀,写出表示丁烷燃烧热化学方程式_____。
(3)已知下列热化学方程式:①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol;
②C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ/mol;
③2H2(g)+O2(g)=2H2O(l ) ΔH3=-571.6kJ/mol,
写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,四支电极均为铂电极,供选择的四组电解质溶液如下表:
组 | A | B | C | D |
甲槽 | NaOH溶液 | AgNO3溶液 | H2SO4溶液 | NaCl溶液 |
乙槽 | CuSO4溶液 | CuCl2溶液 | AgNO3溶液 | AgNO3溶液 |
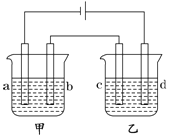
要满足的条件是:①工作一段时间后,甲槽电解液pH上升,而乙槽电解液pH下降;②b、c两极放电离子的物质的量相等。则:
(1)应选用的电解液是________组。
(2)甲槽的电解方程式为:_____________;乙槽的电解方程式为:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应mA(g)+nB(g) ![]() pC(g)+qD(g)的v-t图象如下图,如若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如下图:
pC(g)+qD(g)的v-t图象如下图,如若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如下图:
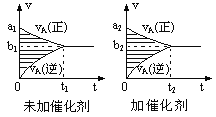
①a1>a2 ②a1<a2 ③b1>b2 ④b1<b2 ⑤t1>t2 ⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧右图中阴影部分面积更大,以上说法中正确的是
A. ②④⑤⑦B. ①④⑥⑧C. ②③⑤⑧D. ①③⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据氧化还原反应CuSO4+Zn=ZnSO4+Cu,可设计如下原电池装置:

⑴该原电池电解质溶液中的溶质是_______。
⑵电极A可选用:____,该电极的反应现象是:_____。
⑶电极B只能用:____,该电极的反应现象是:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CH3OH(g)+![]() O2(g)=CO2(g)+2H2(g) ΔH=﹣190kJ/mol。下列说法正确的是
O2(g)=CO2(g)+2H2(g) ΔH=﹣190kJ/mol。下列说法正确的是
A.CH3OH的燃烧热为190kJ/mol
B.该反应说明CH3OH比H2稳定
C.反应中的能量变化与反应体系的温度和压强无关
D.CO2(g)+2H2(g)=CH3OH(g)+![]() O2(g) ΔH=+190kJ/mol
O2(g) ΔH=+190kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(气)+B(气)![]() 2C(气)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
2C(气)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
①用物质A表示的反应平均速率为0.3 mol·L-1·s-1
②用物质B表示的反应的平均速率为0.6 mol·L-1·s-1
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7 mol·L-1
其中正确的是:
A.①③B.①④C.②③D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】处理某废水时,反应过程中部分离子浓度与反应进程关系如下图,反应过程中主要存在N2、HCO3、ClO、CNO(C+4价,N-3价)、Cl等微粒。下列说法不正确的是

A.该废水呈强酸性
B.废水处理后转化为无害物质
C.反应的离子方程式:3ClO+2CNO+H2O == N2+2HCO3+3Cl
D.每处理1 mol CNO转移3 mol e
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用“锌”和“碳棒”作为导电材料,根据氧化还原反应H2SO4+Zn=ZnSO4+H2↑,设计如下原电池装置:
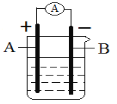
⑴该原电池电解质溶液中的溶质是________。
⑵电极A是________,该电极反应现象为_______。
⑶电极B是______,该电极反应现象为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com