
【题目】用“锌”和“碳棒”作为导电材料,根据氧化还原反应H2SO4+Zn=ZnSO4+H2↑,设计如下原电池装置:
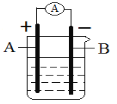
⑴该原电池电解质溶液中的溶质是________。
⑵电极A是________,该电极反应现象为_______。
⑶电极B是______,该电极反应现象为_________。
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:
【题目】已知:pBa=-lgc(Ba2+),Ksp(BaSO4)=1.0×10-10,Ksp(BaCO3)=3.0×10-9。常温下,用 0.1 mol·L-1Na2SO4溶液滴定 20 mL 0.1 mol·L-1BaCl2溶液的曲线如图所示,V0达到滴定终点,下列说法错误的是
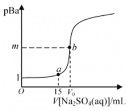
A.图像中,m=5,V0=20
B.若将c(BaCl2)从 0.1 mol· L-1变为 0.2 mol· L-1,m 值将减小
C.a 点溶液中离子浓度大小关系为:c(Cl-)>c(Na+)>c(Ba2+)>c(OH-)
D.向b点溶液中滴加Na2CO3溶液至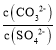 ≥30 时将生成BaCO3
≥30 时将生成BaCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某炼锌厂利用含ZnO的烟尘脱除硫酸工艺烟气中的SO2制ZnSO4。
已知:Ⅰ.ZnSO3·![]() H2O微溶于水,ZnSO4易溶于水。
H2O微溶于水,ZnSO4易溶于水。
Ⅱ.25℃时,溶液中S(+4价)各组分的物质的量分数随pH变化曲线如下图。
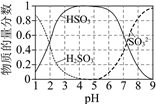
Ⅲ.O3为强氧化剂,1 mol O3被还原转移2 mol e,同时生成1 mol O2。
(1)SO2造成的环境问题主要是_____________________。
(2)ZnO将SO2转化为ZnSO3·![]() H2O的化学方程式是_____________________________。
H2O的化学方程式是_____________________________。
(3)将ZnSO3·![]() H2O悬浊液转化为ZnSO4时,因其被O2氧化的速率很慢,易造成管道堵塞,实验室模拟O3氧化解决该问题。初始时用盐酸将5% ZnSO3悬浊液调至 pH=3.5,以一定的进气流量通入O3,研究O3氧化ZnSO3·
H2O悬浊液转化为ZnSO4时,因其被O2氧化的速率很慢,易造成管道堵塞,实验室模拟O3氧化解决该问题。初始时用盐酸将5% ZnSO3悬浊液调至 pH=3.5,以一定的进气流量通入O3,研究O3氧化ZnSO3·![]() H2O,其中溶液pH随时间变化的曲线如下:
H2O,其中溶液pH随时间变化的曲线如下:

①pH=3.5的溶液中含S(+4价)的离子主要是____________________。
②一段时间后,溶液的pH减小,此过程中主要反应的离子方程式是________________。
③解释O3氧化可防止管道堵塞的原因:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有以下四种物质 ①22g二氧化碳;②5g氢气;③1.204╳1024个氮气分子; ④4℃时18g水,它们所含分子数最多的是_________________;质量最大的是____________;常温时体积最大的是_______________ (填序号)。
(2)V L Fe2(SO4)3溶液中含Fe3+mg,则溶液中SO42-的物质的量浓度为________mol·L-1
(3)标况下,mg 气体A和ng气体B具有相等的体积,则同温同压下的密度之比为________, 同质量的A、B的分子数目之比为________。
(4)在无土栽培中,配制1 L内含5 mol NH4Cl、1.6 mol KCl、2.4 mol K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需KCl、NH4Cl的物质的量分别为_____________、_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A.0.01molL-1KAl(SO4)2溶液中的SO42-数目为0.02NA
B.用浓盐酸分别与MnO2、KClO3反应制备1mol氯气,转移的电子数均为2NA
C.1molNH4NO3完全溶于稀氨水中,溶液呈中性,溶液中NH4+的数目为NA
D.9.0g葡萄糖和蔗糖的混合物中含碳原子的数目为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,意大利科学家使用普通氧分子和带正电的氧离子作用,制造了新型的氧分子O4,它的结构很复杂,可能具有与S4相似的长方形结构,是一种高能量分子。
⑴下列有关说法中,不正确的是________(填字母)。
A.O4分子内存在共价键
B.合成O4的反应可看做核聚变反应,即不属于化学变化
C.O4与O3、O2都是氧元素的同素形体
D.O4将来可用作更强有力的火箭推进的氧化剂
⑵制备O2-、O22-甚至O22+的化合物是可能的,通常它们是在氧分子进行下图所示的各种反应时生成。这些反应中,相当于氧分子的氧化的是_______(填序号);相当于氧分子的还原的是_______(填序号)。

⑶O22+中氧原子间形成3对共用电子对使氧原子达到稳定结构,写出O22+的电子式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式的书写正确的是
A.CO2通入饱和碳酸钠溶液中:CO2 +CO32- + H2O=2HCO3-
B.明矾溶液中加氢氧化钡至硫酸根恰好沉淀完全:Al3+ + 2SO42- + 2Ba2+ + 4OH- == 2BaSO4↓ + AlO2- + 2H2O
C.钠和冷水反应Na+ 2H2O =Na+ + 2OH- + H2↑
D.氯化铝溶液中加入过量的氨水Al3+ + 4NH3·H2O =AlO2- + 4NH4+ + 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一铁的氧化物样品,用140 mL 5 mol·L-1的盐酸恰好完全溶解,所得溶液还能与通入的0.56 L氯气(标准状况)反应,使Fe2+全部转化为Fe3+,则此氧化物为
A.Fe2O3B.Fe3O4C.Fe4O5D.Fe5O7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.已知: ,且A→B为加成反应,则B的结构简式是______________;B→C的反应类型是____________。
,且A→B为加成反应,则B的结构简式是______________;B→C的反应类型是____________。
II.叶酸是维生素B族之一,可以由下列甲、乙、丙三种物质合成。
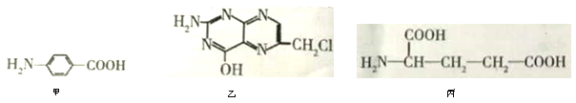
(1)甲中显酸性的官能团是______________(填名称)。
(2)下列关于乙的说法正确的是__________(填序号)。
a.分子中碳原子与氮原子的个数比是7∶5 b.属于芳香族化合物
c.既能与盐酸又能与氢氧化钠溶液反应 d.属于苯酚的同系物
(3)丁是丙的同分异构体,且满足下列两个条件,了的结构简式为______________.
a.含有![]() b.在稀硫酸中水解有乙酸生成
b.在稀硫酸中水解有乙酸生成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com