
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ͼ��ʾ��Ǧ������һ�ֵ��͵Ŀɳ���أ�����ܷ�ӦʽΪ��Pb+PbO2+4H++2SO42-
��ͼ��ʾ��Ǧ������һ�ֵ��͵Ŀɳ���أ�����ܷ�ӦʽΪ��Pb+PbO2+4H++2SO42-| �ŵ� |
| ��� |
| A���ŵ�ʱ��������Ӧ��Pb-2e-+SO42-=PbSO4 |
| B���ŵ�ʱ�����·�е�������������B��A |
| C���ŵ�ʱ��Ǧ���صĸ����������ӣ�����������С |
| D�����ʱ����װ���л�ѧ��ת��Ϊ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ȩ��Һ |
| B������Na2SO4��Һ |
| C�����ͣ�NH4��2SO4��Һ |
| D������Ǧ��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1�����з�Ӧ����������ԭ��Ӧ�����Ƿ��ȷ�Ӧ����
��1�����з�Ӧ����������ԭ��Ӧ�����Ƿ��ȷ�Ӧ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| �¶ȣ��棩 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| ͭ��ƽ���ܽ�����[��10-3 mol?��L?min��-1] | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


Ũ��/mol?L-1 ʱ��/min |
NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
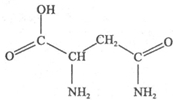 �춬�������ṹ��ͼ����«���к����ḻ��������������������Ĺ�Ч��
�춬�������ṹ��ͼ����«���к����ḻ��������������������Ĺ�Ч��| ��ѧʽ | ����/nm | ���� | �е�/�� |
| H2S | 1.34 | 92.3�� | -60.75 |
| H2Se | 1.47 | 91.0�� | -41.50 |
| ��� | I5/kJ?mol-1 | I6/kJ?mol-1 | I7/kJ?mol-1 | I8/kJ?mol-1 |
| A | 6990 | 9220 | 11500 | 18770 |
| B | 6702 | 8745 | 15455 | 17820 |
| C | 5257 | 6641 | 12125 | 13860 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�� ����100mL 0.1mol?L-1������ |
B�� ���հ�������ֹ���� |
C�� ��ȡ������ϩ���� |
D�� ��֤�����鷢����ȥ��Ӧ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com