
【题目】在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命.下表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
成分 | 质量(g) | 摩尔质量(gmol﹣1) |
蔗糖 | 25.00 | 342 |
硫酸钾 | 3.48 | 174 |
阿司匹林 | 0.17 | 180 |
高锰酸钾 | 1.58 | 158 |
硝酸银 | 0.02 | 170 |
(1)下列“鲜花保鲜剂”的成分中,属于电解质的是 .
A.蔗糖
B.硫酸钾
C.高锰酸钾
D.硝酸银
(2)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为 .
(3)配制上述“鲜花保鲜剂”用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少 , (填写所缺仪器的名称).
(4)配制溶液时有以下几个操作:①溶解 ②摇匀 ③洗涤 ④冷却 ⑤称量 ⑥转移溶液 ⑦定容,
正确的操作顺序是(填序号).
(5)若定容时俯视容量瓶刻度线,会使所配溶液浓度(填偏大、偏小、不变).
【答案】
(1)BCD
(2)0.1 mol/L
(3)500mL容量瓶;胶头滴管
(4)⑤①④⑥③⑦②
(5)偏大
【解析】解:(1)A.蔗糖含有蔗糖分子,在水溶液中,不能电离,只存在分子,不能导电,是非电解质,故A不选; B.硫酸钾,能电离出硫酸根离子和钾离子,能导电,是化合物,是电解质,故B选;C.高锰酸钾是盐,能在水溶液中和熔融状态下电离出自由移动的离子而导电,是电解质,故C选;D.硝酸银,溶于水溶液中或在熔融状态下就能够导电,是电解质,故D选;所以答案是:BCD;(2)K2SO4的物质的量为: ![]() =0.02mol,则K+的物质的量为0.04mol,KMnO4的物质的量为
=0.02mol,则K+的物质的量为0.04mol,KMnO4的物质的量为 ![]() =0.01mol,则K+的物质的量为0.01mol,所以溶液中的K+总共为0.05mol,其物质的量浓度为
=0.01mol,则K+的物质的量为0.01mol,所以溶液中的K+总共为0.05mol,其物质的量浓度为 ![]() =0.1mol/L,所以答案是:0.1 mol/L;(3)配制顺序是:计算→称量→溶解、冷却→移液→洗涤→定容→摇匀→装瓶→贴签,一般用天平称量(用到药匙)称量,在烧杯中溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀.所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,故缺少的玻璃仪器为胶头滴管、500mL容量瓶,所以答案是:500mL容量瓶;胶头滴管;(4)配制一定物质的量浓度的溶液的步骤是:计算、称量、溶解、移液、洗涤、定容、摇匀,故正确的操作顺序是⑤①④⑥③⑦②,所以答案是:⑤①④⑥③⑦②;(5)定容时俯视容量瓶刻度线,会导致溶液体积偏小,则浓度偏大,所以答案是:偏大.
=0.1mol/L,所以答案是:0.1 mol/L;(3)配制顺序是:计算→称量→溶解、冷却→移液→洗涤→定容→摇匀→装瓶→贴签,一般用天平称量(用到药匙)称量,在烧杯中溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀.所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,故缺少的玻璃仪器为胶头滴管、500mL容量瓶,所以答案是:500mL容量瓶;胶头滴管;(4)配制一定物质的量浓度的溶液的步骤是:计算、称量、溶解、移液、洗涤、定容、摇匀,故正确的操作顺序是⑤①④⑥③⑦②,所以答案是:⑤①④⑥③⑦②;(5)定容时俯视容量瓶刻度线,会导致溶液体积偏小,则浓度偏大,所以答案是:偏大.
【考点精析】本题主要考查了配制一定物质的量浓度的溶液的相关知识点,需要掌握配制物质的量浓度溶液时,先用烧杯加蒸馏水至容量瓶刻度线1cm~2cm后,再改用交投滴管加水至刻度线才能正确解答此题.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】区别CH4、CH2=CH2、CH≡CH的最简易方法是( )
A.分别通入溴水
B.分别通入酸性高锰酸钾溶液
C.分别在空气中点燃
D.分别通入盛有碱石灰的干燥管
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柠檬烯是一种食用香料,其结构简式为: ![]() 有关柠檬烯的分析正确的是( )
有关柠檬烯的分析正确的是( )
A.分子式为C10H14
B.一定条件下,柠檬烯可以发生加成、取代、氧化、还原反应
C.柠檬烯有属于苯的同系物的同分异构体
D.柠檬烯的分子中所有碳原子可能处在同一个平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是电解CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( ) 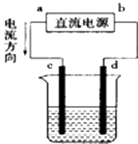
A.a为负极,b为正极
B.d为阳极,c为阴极
C.电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用盖斯定律可计算一些不易测定的反应的反应热.
(1)已知在298K时下述反应的有关数据:C(s)+ ![]() O2(g)=CO(g)△H1=﹣110.5kJmol﹣1 , C(s)+O2(g)=CO2(g)△H2=﹣393.5kJmol﹣1 . 则C(s)+CO2(g)=2CO(g) 的△H为 .
O2(g)=CO(g)△H1=﹣110.5kJmol﹣1 , C(s)+O2(g)=CO2(g)△H2=﹣393.5kJmol﹣1 . 则C(s)+CO2(g)=2CO(g) 的△H为 .
(2)火箭发射时可用肼(N2H4)为燃料,以二氧化氮作氧化剂,它们相互反应生成氮气和水蒸气.已知:N2(g)+2O2(g)=2NO2(g)△H=+67.7kJmol﹣l;N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=﹣534kJmol﹣l . 则N2H4和NO2反应生成氮气和水蒸气的热化学方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列除杂的离子方程式,括号内的物质为杂质.
物质(杂质) | 离子方程式 |
FeCl2 (FeCl3) | (1) |
CO2 (HCl) | (2) |
NaHC03 溶液(Na2C03) | (3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正丁醚常用作有机反应的溶剂.实验室制备正丁醚的反应和主要实验装置如下:
2CH3CH2CH2CH2OH ![]() (CH3CH2CH2CH2)2O+H2O
(CH3CH2CH2CH2)2O+H2O
反应物和产物的相关数据如下
相对分子质量 | 沸点/℃ | 密度/(gcm﹣3) | 水中溶解性 | |
正丁醇 | 74 | 117.2 | 0.8109 | 微溶 |
正丁醚 | 130 | 142.0 | 0.7704 | 几乎不溶 |
合成反应:
①将6mL浓硫酸和37g正丁醇,按一定顺序添加到A中,并加几粒沸石.
②加热A中反应液,迅速升温至135℃,维持反应一段时间.分离提纯.
③待A中液体冷却后将其缓慢倒人盛有70mL水的分液谝斗中,振摇后静置,分液得粗产物.
④粗产物依次用40mL水、20mL NaOH溶液和40mL水洗涤,分液后加入约3g无水氯化钙颗粒,静置一段时间后弃去氯化钙.
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚11g.
请回答:
(1)步骤①中浓硫酸和正丁醇的添加顺序为 .
(2)加热A前,需先从 (填“a”或“b”)口向B中通入水.
(3)步骤③的目的是初步洗去 , 振摇后静置,粗产物应从分液漏斗的(填“上”或“下”)口分离出.
(4)步骤③巾最后一次水洗的目的为 .
(5)步骤⑤中,加热蒸馏时应收集(填选项字母)左右的馏分.a.100℃b.117℃c. 135℃d.142℃
(6)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A.分水器中上层液体的主要成分为 , 下层液体的主要成分为 .
(7)本实验中,正丁醚的产率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
阳离子 | K+、Na+ 、Cu2+、 Al3+ |
阴离子 | SO |
为了鉴别上述化合物,分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,仅有B为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸酸化的硝酸钡溶液,只有A中放出无色气体,只有D中产生白色沉淀;
⑤将B、C两溶液混合,未见沉淀或气体生成.根据上述实验填空:
(1)写出B、D的化学式:B , D .
(2)C可用作净水剂,用离子方程式表示其净水原理 .
(3)将含0.01mol A的溶液与含0.02mol E的溶液反应后,向溶液中滴加0.1molL﹣1稀盐酸.下列图象能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是
(4)在mmL b molL﹣1 C溶液中,加入等体积a molL﹣1 的E溶液.当a≤3b时,生成沉淀的物质的量是 mol;当3b<a<4b件时,生成沉淀的物质的量是 mol.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com