
ЁОЬтФПЁПИпУЬЫсМиЪЧвЛжжЕфаЭЕФЧПбѕЛЏМСЁЃЭъГЩЯТСаЬюПеЃК
ЂёЃЎдкгУKMnO4ЫсадШмвКДІРэCu2SКЭCuSЕФЛьКЯЮяЪБЃЌЗЂЩњЕФЗДгІШчЯТЃК
Ђй MnO4Ѓ+ Cu2S + H+Ёњ Cu2+ + SO2Ёќ + Mn2+ + H2O(ЮДХфЦН)
Ђк MnO4Ѓ+ CuS + H+ Ёњ Cu2+ + SO2Ёќ + Mn2+ЃЋ H2O(ЮДХфЦН)
ЃЈ1ЃЉЯТСаЙигкЗДгІЂйЕФЫЕЗЈжаДэЮѓЕФЪЧ ЃЈбЁЬюБрКХЃЉЁЃ
aЃЎБЛбѕЛЏЕФдЊЫиЪЧCuКЭS
bЃЎбѕЛЏМСгыЛЙдМСЕФЮяжЪЕФСПжЎБШЮЊ8:5
cЃЎЛЙдадЕФЧПШѕЙиЯЕЪЧЃК Mn2+<Cu2S
dЃЎЩњГЩ2.24 L(БъПіЯТ) SO2ЃЌзЊвЦЕчзгЕФЮяжЪЕФСПЪЧ0.6mol
ЃЈ2ЃЉБъГіЗДгІЂкжаЕчзгзЊвЦЕФЗНЯђКЭЪ§ФПЃК MnO4Ѓ+ CuS
ЂђЃЎдкЯЁСђЫсжаЃЌMnO4ЃКЭH2O2вВФмЗЂЩњбѕЛЏЛЙдЗДгІ
бѕЛЏЗДгІЃКH2O2Ѓ2e-Ёњ 2H++O2Ёќ
ЛЙдЗДгІЃКMnO4Ѓ+5e-+8H+ЁњMn2++4H2O
ЃЈ3ЃЉЗДгІжаШєга0.5 mol H2O2ВЮМгДЫЗДгІЃЌзЊвЦЕчзгЕФИіЪ§ЮЊ ЁЃгЩЩЯЪіЗДгІЕУГіЕФЮяжЪбѕЛЏадЧПШѕЕФНсТлЪЧ >_________(ЬюаДЛЏбЇЪН)ЁЃ
ЃЈ4ЃЉвбжЊЃК2KMnO4+7H2O2+3H2SO4Ёњ K2SO4+2MnSO4+6O2Ёќ+10H2OЃЌдђБЛ1molKMnO4бѕЛЏЕФH2O2ЪЧ molЁЃ
ЁОД№АИЁПЃЈ1ЃЉd
ЃЈ2ЃЉ![]()
ЃЈ3ЃЉ6.02ЁС1023 ЃЛ KMnO4> H2O2(ЛђO2)
ЃЈ4ЃЉ2.5
ЁОНтЮіЁП
ЪдЬтЗжЮіЃКIЃЎЃЈ1ЃЉaЃЎЗДгІжаЭдЊЫиЛЏКЯМлДг+1МлЩ§ИпЕН+2МлЃЌСђдЊЫиЛЏКЯМлДг-2МлЩ§ИпЕН+4МлЃЌЛЏКЯМлЩ§ИпЕФдЊЫиБЛбѕЛЏЃЌЫљвдБЛбѕЛЏЕФдЊЫигаSЁЂCuЃЌЙЪaе§ШЗЃЛbЃЎУЬдЊЫиЛЏКЯМлНЕЕЭЃЌДг+7МлНЕЕЭЮЊ+2МлЃЌCu2SдЊЫиЛЏКЯМлЖМЩ§ИпзіЛЙдМСЃЌ1molMnO4-ЕУЕН5molЕчзгЃЌЗДгІжаЭдЊЫиЛЏКЯМлДг+1МлЩ§ИпЕН+2МлЃЌСђдЊЫиЛЏКЯМлДг-2МлЩ§ИпЕН+4МлЃЌ1molCu2SЪЇШЅ8molЕчзгЃЌдђбѕЛЏМСгыЛЙдМСЕФЮяжЪЕФСПжЎБШЮЊ8ЃК5ЃЌЙЪbе§ШЗЃЛcЃЎбѕЛЏЛЙдЗДгІжаЛЙдМСЕФЛЙдадДѓгкЛЙдВњЮяЕФЛЙдадЃЌдђЛЙдадЕФЧПШѕЙиЯЕЪЧЃКMn2+ЃМCu2SЃЌЙЪcе§ШЗЃЎdЃЎЩњГЩ2.24LLЃЈБъПіЯТЃЉSO2ЪБЃЌЮяжЪЕФСПЮЊ0.1molЃЛЗДгІЕФCu2SЮяжЪЕФСПЮЊ0.1molЃЌЗДгІжазЊвЦЕчзгЕФЮяжЪЕФСПЪЧЃК
Cu+ЁЋCu2+ЁЋe-ЃЛ S2-ЁЋSO2ЁЋ6e-ЃЛ
1 1 1 6
0.2mol 0.2mol 0.1mol 0.6mol
ЫљвдЕчзгзЊвЦЙВ0.8molЃЌЙЪdДэЮѓЃЛЙЪД№АИЮЊЃКdЃЛ
ЃЈ2ЃЉгЩЂкПЩЕУЃЌУЬдЊЫиЛЏКЯМлгЩ+7НЕЕН+2ЃЌСђдЊЫиЛЏКЯМлгЩ-2Щ§ЕН+4ЃЌИљОнЕУЪЇЕчзгЪиКуЕУЃК6MnO4-+5CuS+Ё ЃЌЛЙдМСЪЧCuSЃЌбѕЛЏМСЪЧMnO4-ЃЌЕчзгзЊвЦЕФЗНЯђКЫЭтЪ§ФПЮЊ![]() ЃЌЙЪД№АИЮЊЃК
ЃЌЙЪД№АИЮЊЃК![]() ЃЛ
ЃЛ
ЂђЃЎЃЈ3ЃЉH2O2жаOдЊЫигЩ-1МлБфГЩ0МлЃЌЗДгІжаШєга0.5 mol H2O2ВЮМгДЫЗДгІЃЌзЊвЦЕчзгЕФИіЪ§ЮЊ0.5 molЁСЃЈ1-0ЃЉЁС2ЁС6.02ЁС1023 = 6.02ЁС1023 ЃЌИљОнбѕЛЏМСЕФбѕЛЏадЧПгкбѕЛЏВњЮяЕФбѕЛЏадЃЌбѕЛЏадKMnO4> H2O2(ЛђO2)ЃЌЙЪД№АИЮЊЃК6.02ЁС1023 ЃЛ KMnO4> H2O2(ЛђO2) ЃЛ
ЃЈ4ЃЉKMnO4жаУЬдЊЫигЩ+7МлБфГЩ+2МлЃЌH2O2жаOдЊЫигЩ-1МлБфГЩ0МлЃЌИљОнЕУЪЇЕчзгЪиКуЃЌ1molKMnO4бѕЛЏЕФH2O2ЕФЮяжЪЕФСПЮЊ![]() =
=![]() molЃЌЙЪД№АИЮЊЃК
molЃЌЙЪД№АИЮЊЃК![]() ЁЃ
ЁЃ


 ЬьЬьСЗПкЫуЯЕСаД№АИ
ЬьЬьСЗПкЫуЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгаЮЛгкжмЦкБэжаЕФЦпжждЊЫиЃЌЪдАДЯТЪіЫљИјЕФЬѕМўЭЦЖЯЁЃ
ЂйAЁЂBЁЂCЪЧЭЌвЛжмЦкЕФН№ЪєдЊЫиЃЌвбжЊдзгКЫЭтга3ИіЕчзгВуЃЌAЕФдзгАыОЖдкЫљЪєжмЦкжазюДѓЧвдзгАыОЖAЃОBЃОCЁЃ
ЂкDЁЂEЪЧЗЧН№ЪєдЊЫиЃЌЫќУЧИњЧтЛЏКЯПЩЩњГЩЦјЬЌЧтЛЏЮяHDКЭHEЃЌдкЪвЮТЪБЃЌDЕФЕЅжЪЪЧвКЬхЃЌEЕФЕЅжЪЪЧЙЬЬхЁЃ
ЂлFдкГЃЮТЯТЪЧЦјЬхЃЌаджЪЮШЖЈЃЌЪЧГ§ЧтЦјЭтзюЧсЕФЦјЬхЁЃ
ЂмGЪЧГ§ЧтЭтдзгАыОЖзюаЁЕФдЊЫи(ВЛПМТЧЯЁгаЦјЬх)ЁЃ
ЃЈ1ЃЉAЕФУћГЦЪЧ________ЃЛBЮЛгкжмЦкБэжаЕк______жмЦкЃЌЕк________зхЃЛCЕФдзгНсЙЙЪОвтЭМЪЧ________ЁЃ
ЃЈ2ЃЉEЕЅжЪЕФбеЩЋЪЧ________ЁЃ
ЃЈ3ЃЉAдЊЫигыDдЊЫиаЮГЩЛЏКЯЮяЕФЕчзгЪНЪЧ___________ЁЃ
ЃЈ4ЃЉGЕФЕЅжЪгыЫЎЗДгІЕФЛЏбЇЗНГЬЪНЪЧ______________________________ЁЃ
ЃЈ5ЃЉFЕФдЊЫиЗћКХЪЧ________ЁЃ
ЃЈ6ЃЉдкЩЯЪіЦпжждЊЫижаЃЌзюИпМлбѕЛЏЮяЖдгІЕФЫЎЛЏЮяМюадзюЧПЕФЛЏбЇЪНЪЧ______ЃЛЦјЬЌЧтЛЏЮязюЮШЖЈЕФЛЏбЇЪНЪЧ______ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТБэЪЧдЊЫижмЦкБэЕФвЛВПЗжЁЃБэжаЫљСаЕФзжФИЗжБ№ДњБэвЛжжЛЏбЇдЊЫиЁЃ
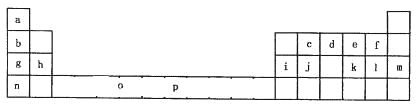
ЪдЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉдЊЫиpЮЊ26КХдЊЫиЃЌЧыЛГіЦфЛљЬЌдзгЭтЮЇЕчзгХХВМЭМ______________ЃЛ
ЃЈ2ЃЉeгыaЗДгІЕФВњЮяЕФЗжзгжажааФдзгЕФдгЛЏаЮЪНЮЊ________________ЃЛИУЗжзгЪЧ_________ЃЈЬюЁАМЋадЁБЛђЁАЗЧМЋадЁБЃЉЗжзгЁЃ
ЃЈ3ЃЉЩЯБэжадЊЫиЛљЬЌдзгЕФЕквЛЕчРызюДѓЕФдЊЫиЪЧ__________ЁЃЃЈгУдЊЫиЗћКХБэЪОЃЉ
ЃЈ4ЃЉoЁЂpСНдЊЫиЕФВПЗжЕчРыФмЪ§ОнСагкЯТБэЃК
дЊ Ыи | O | P | |
ЕчРыФм | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
БШНЯСНдЊЫиЕФI2ЁЂI3ПЩжЊЃЌЦјЬЌo2+дйЪЇШЅвЛИіЕчзгБШЦјЬЌp2+дйЪЇШЅвЛИіЕчзгФбЃЌЖдДЫЃЌФуЕФНтЪЭЪЧ______________ЃЛ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЁОМгЪдЬтЁПЙЄвЕжЦСђЫсЃЌРћгУДпЛЏбѕЛЏЗДгІНЋSO2зЊЛЏЮЊSO3ЪЧвЛИіЙиМќВНжшЁЃЧыЛиД№ЃК
ЃЈ1ЃЉФГЮТЖШЯТЃЌSO2(g)ЃЋO2(g)![]() SO3(g) ЃЛІЄHЃНЃ98 kJ ЁЄ mol-1ЁЃПЊЪМЪБдк100 LЕФУмБеШнЦїжаМгШы4.0 mol SO2(g)КЭ10.0 mol O2(g)ЃЌЕБЗДгІДяЕНЦНКтЪБЙВЗХГіШШСП196 kJЃЌИУЮТЖШЯТЦНКтГЃЪ§KЃН________ ЁЃ
SO3(g) ЃЛІЄHЃНЃ98 kJ ЁЄ mol-1ЁЃПЊЪМЪБдк100 LЕФУмБеШнЦїжаМгШы4.0 mol SO2(g)КЭ10.0 mol O2(g)ЃЌЕБЗДгІДяЕНЦНКтЪБЙВЗХГіШШСП196 kJЃЌИУЮТЖШЯТЦНКтГЃЪ§KЃН________ ЁЃ
ЃЈ2ЃЉвЛЖЈЬѕМўЯТЃЌЯђвЛДјЛюШћЕФУмБеШнЦїжаГфШы2 mol SO2КЭ1 mol O2ЃЌЗЂЩњЯТСаЗДгІЃК2SO2(g)ЃЋO2(g)![]() 2SO3(g)ЃЌДяЕНЦНКтКѓИФБфЯТЪіЬѕМўЃЌSO2ЁЂO2ЁЂSO3ЦјЬхЦНКтХЈЖШЖМБШдРДдіДѓЕФЪЧ________(ЬюзжФИ)ЁЃ
2SO3(g)ЃЌДяЕНЦНКтКѓИФБфЯТЪіЬѕМўЃЌSO2ЁЂO2ЁЂSO3ЦјЬхЦНКтХЈЖШЖМБШдРДдіДѓЕФЪЧ________(ЬюзжФИ)ЁЃ
AЃЎБЃГжЮТЖШКЭШнЦїЬхЛ§ВЛБфЃЌГфШы2 mol SO3
BЃЎБЃГжЮТЖШКЭШнЦїЬхЛ§ВЛБфЃЌГфШы2 mol N2
CЃЎБЃГжЮТЖШКЭШнЦїЬхЛ§ВЛБфЃЌГфШы0.5 mol SO2КЭ0.25 molO2
DЃЎБЃГжЮТЖШКЭШнЦїФкбЙЧПВЛБфЃЌГфШы1 mol SO3
EЃЎЩ§ИпЮТЖШ
FЃЎвЦЖЏЛюШћбЙЫѕЦјЬх
ЃЈ3ЃЉФГШЫЩшЯывдЯТЭМЫљЪОзАжУгУЕчЛЏбЇдРэЩњВњСђЫсЃЌаДГіЭЈШыSO2ЕФЕчМЋЕФЕчМЋЗДгІЪНЃК______ЁЃ
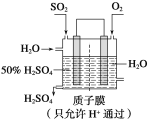
ЃЈ4ЃЉЯТСаЙигк2SO2(g)ЃЋO2(g)![]() 2SO3(g)ЗДгІЕФЭМЯёжаЃЌвЛЖЈе§ШЗЕФЪЧ________(ЬюађКХ)ЁЃ
2SO3(g)ЗДгІЕФЭМЯёжаЃЌвЛЖЈе§ШЗЕФЪЧ________(ЬюађКХ)ЁЃ
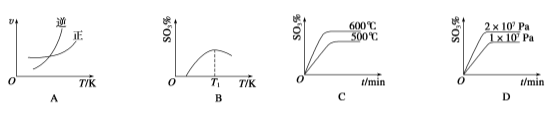
ЃЈ5ЃЉЂйФГЮТЖШЯТЃЌSO2ЕФЦНКтзЊЛЏТЪ(ІС)гыЬхЯЕзмбЙЧП(p)ЕФЙиЯЕШчЯТЭМЫљЪОЁЃЕБЦНКтзДЬЌгЩAБфЕНBЪБЃЌЦНКтГЃЪ§K(A)_______ K(B)(ЬюЁАЃОЁБЁЂЁАЃМЁБЛђЁАЃНЁБ)ЁЃ
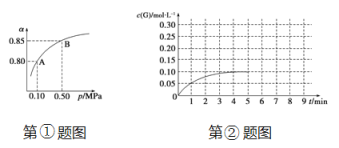
ЂкНЋвЛЖЈСПЕФSO2(g)КЭO2(g)ЗХШыФГЙЬЖЈЬхЛ§ЕФУмБеШнЦїжаЃЌдквЛЖЈЬѕМўЯТЃЌc(SO3)ЕФБфЛЏШчЯТЭМЫљЪОЁЃШєдкЕк5ЗжжгНЋШнЦїЕФЬхЛ§ЫѕаЁвЛАыКѓЃЌдкЕк8ЗжжгДяЕНаТЕФЦНКт(ДЫЪБSO3ЕФХЈЖШЮЊ0.25 molЁЄLЃ1)ЁЃЧыдкЯТЭМЛГіДЫБфЛЏЙ§ГЬжаSO3(g)ХЈЖШЕФБфЛЏЧњЯпЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊЃКHCN(aq)гыNaOH(aq)ЗДгІЕФЁїH=Ѓ12.1kJ /molЃЛHCl(aq)гыNaOH(aq)ЗДгІЕФЁїH =Ѓ55.6kJ/ molЁЃдђHCNдкЫЎШмвКжаЕчРыЕФІЄHЕШгк
A. Ѓ67.7 kJ /mol B. Ѓ43.5kJ /mol C. +43.5 kJ/ mol D. +67.7 kJ/ mol
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСагаЙиУКЁЂЪЏгЭЁЂЬьШЛЦјЕШзЪдДЕФЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ
AЃЎЪЏгЭСбНтЕУЕНЕФЦћгЭЪЧДПОЛЮя
BЃЎУКЕФЦјЛЏОЭЪЧНЋУКдкИпЮТЬѕМўгЩЙЬЬЌзЊЛЏЮЊЦјЬЌЃЌЪЧЮяРэБфЛЏЙ§ГЬ
CЃЎЬьШЛЦјЪЧвЛжжЧхНрЕФЛЏЪЏШМСЯ
DЃЎУКОЭЪЧЬМЃЌЪєгкЕЅжЪ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЁО2016НьКЊЕІвЛФЃЁПЁОЛЏбЇбЁао3ЃКЮяжЪНсЙЙгыаджЪЁП
аТаЭДЂЧтВФСЯЪЧПЊЗЂРћгУЧтФмЕФживЊбаОПЗНЯђЁЃ
ЃЈ1ЃЉTi(BH4)3ЪЧвЛжжДЂЧтВФСЯЃЌПЩгЩTiCl4КЭLiBH4ЗДгІжЦЕУЁЃ
ЂйЛљЬЌClдзгжаЃЌЕчзгеМОнЕФзюИпФмВуЗћКХЮЊ_________ЃЌИУФмВуОпгаЕФдзгЙьЕРЪ§ЮЊ________ЁЃ
ЂкLiBH4гЩLi+КЭBH4-ЙЙГЩЃЌBH4-ЕФСЂЬхНсЙЙЪЧ_________ЃЌBдзгЕФдгЛЏЙьЕРРраЭЪЧ________ЁЃ
LiЁЂBЁЂHдЊЫиЕФЕчИКадгЩДѓЕНаЁХХСаЫГађЮЊ________ЁЃ
ЃЈ2ЃЉН№ЪєЧтЛЏЮяЪЧОпгаСМКУЗЂеЙЧАОАЕФДЂЧтВФСЯЁЃ
ЂйLiHжаЃЌРызгАыОЖLi+_______H-(ЬюЁАЃОЁБЁЂЁА=ЁБЛђЁАЃМЁБ)ЃЎЂкФГДЂЧтВФСЯЪЧЕкШ§жмЦкН№ЪєдЊЫиMЕФЧтЛЏЮяЃЎMЕФВПЗжЕчРыФмШчБэЫљЪОЃК
I1/kJmol-1 | I2/kJmol-1 | I3/kJmol-1 | I4/kJmol-1 | I5/kJmol-1 |
738 | 1451 | 7733 | 10540 | 13630 |
MЪЧ________ (ЬюдЊЫиЗћКХ)ЁЃ
ЃЈ3ЃЉNaHОпгаNaClаЭОЇЬхНсЙЙЃЌвбжЊNaHОЇЬхЕФОЇАћВЮЪ§a=488pm(РтГЄ)ЃЌNa+АыОЖЮЊ102pmЃЌH-ЕФАыОЖЮЊ________ЃЌNaHЕФРэТлУмЖШЪЧ___________gЁЄcm-3(жЛСаЫуЪНЃЌВЛБиМЦЫуГіЪ§жЕЃЌАЂЗќМгЕТТоГЃЪ§ЮЊNA)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвдЕчЪЏдќ[жївЊГЩЗжЮЊCa(OH)2КЭCaCO3]ЮЊдСЯжЦБИKClO3ЕФСїГЬШчЯТЃК
![]()

ЃЈ1ЃЉТШЛЏЙ§ГЬПижЦЕчЪЏдќЙ§СПЃЌдк75ЁцзѓгвНјааЁЃТШЛЏЪБДцдкCl2гыCa(OH)2зїгУЩњГЩCa(ClO)2ЕФЗДгІЃЌCa(ClO)2НјвЛВНзЊЛЏЮЊCa(ClO3)2ЃЌЩйСПCa(ClO)2 ЗжНтЮЊCaCl2КЭO2ЁЃ
ЂйЩњГЩCa(ClO)2ЕФЛЏбЇЗНГЬЪНЮЊ ЁЃ
ЂкЬсИпCl2зЊЛЏЮЊCa(ClO3)2ЕФзЊЛЏТЪЕФПЩааДыЪЉга ЃЈЬюађКХЃЉЁЃ
AЃЎЪЪЕБМѕЛКЭЈШыCl2ЫйТЪ
BЃЎГфЗжНСАшНЌСЯ
CЃЎМгЫЎЪЙCa(OH)2ЭъШЋШмНт
ЃЈ2ЃЉТШЛЏЙ§ГЬжаCl2 зЊЛЏЮЊCa(ClO3)2ЕФзмЗДгІЗНГЬЪНЮЊ6Ca(OH)2+6Cl2ЃНCa(ClO3)2+5CaCl2+6H2OТШЛЏЭъГЩКѓЙ§ТЫЁЃ

ЂйТЫдќЕФжївЊГЩЗжЮЊ ЃЈЬюЛЏбЇЪНЃЉЁЃ
ЂкТЫвКжаCa(ClO3)2гыCaCl2ЕФЮяжЪЕФСПжЎБШn[Ca(ClO3)2] ЁУn[CaCl2] 1ЁУ5ЃЈЬюЁАЃОЁБЁЂЁАЃМЁБЛђЁАЃНЁБЃЉЁЃ
ЃЈ3ЃЉЯђТЫвКжаМгШыЩдЙ§СПKClЙЬЬхПЩНЋCa(ClO3)2зЊЛЏЮЊKClO3ЃЌШєШмвКжаKClO3ЕФКЌСПЮЊ100gL-1ЃЌДгИУШмвКжаОЁПЩФмЖрЕиЮіГіKClO3ЙЬЬхЕФЗНЗЈЪЧ ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПУОЪЧКЃЫЎжаКЌСПНЯЖрЕФН№ЪєЃЌУОЁЂУОКЯН№МАЦфУОЕФЛЏКЯЮядкПЦбЇбаОПКЭЙЄвЕЩњВњжагУЭОЗЧГЃЙуЗКЁЃ
ЃЈ1ЃЉMg2NiЪЧвЛжжДЂЧтКЯН№ЃЌвбжЊЃК
Mg(s) + H 2 (g)=MgH 2 (s) ЁїH 1 =Ѓ74.5kJЁЄmol Ѓ1
Mg 2 Ni(s) + 2H 2 (g)=Mg 2 NiH 4 (s) ЁїH 2 =Ѓ64.4kJЁЄmol Ѓ1
Mg 2 Ni(s)+2MgH 2 (s) = 2Mg(s)+Mg 2 NiH 4 (s) ЁїH 3
дђЁїH 3 = kJЁЄmol Ѓ1 ЁЃ
ЃЈ2ЃЉЙЄвЕЩЯПЩгУЕчНтШлШкЕФЮоЫЎТШЛЏУОЛёЕУУОЁЃЦфжаТШЛЏУОЭбЫЎЪЧЙиМќЙЄвежЎвЛЃЌвЛжже§дкЪдбщЕФТШЛЏУООЇЬхЭбЫЎЕФЗНЗЈЪЧЃКЯШНЋMgCl 2 ЁЄ6H 2 OзЊЛЏЮЊMgCl 2 ЁЄNH 4 ClЁЄnNH 3ЃЌШЛКѓдк700ЁцЭбАБЕУЕНЮоЫЎТШЛЏУОЃЌЭбАБЗДгІЕФЛЏбЇЗНГЬЪНЮЊ ЃЛЕчНтШлШкТШЛЏУОЃЌвѕМЋЕФЕчМЋЗДгІЪНЮЊ ЁЃ
ЃЈ3ЃЉДЂЧтВФСЯMg(AlH4) 2 дк110ЁЋ200ЁуCЕФЗДгІЮЊЃКMg(AlH4) 2 =MgH 2 +2Al+3H 2 ЁќУПЩњГЩ27gAlзЊвЦЕчзгЕФЮяжЪЕФСПЮЊ ЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com